UNIVERZA V LJUBLJANI PEDAGOŠKA FAKULTETA BIOTEHNIŠKA FAKULTETA FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO NARAVOSLOVNOTEHNIŠKA FAKULTETA
|
|
|
- Todd Daniels
- 6 years ago
- Views:
Transcription
1 UNIVERZA V LJUBLJANI PEDAGOŠKA FAKULTETA BIOTEHNIŠKA FAKULTETA FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO NARAVOSLOVNOTEHNIŠKA FAKULTETA DIPLOMSKO DELO NADA PUHALIĆ
2 UNIVERZA V LJUBLJANI PEDAGOŠKA FAKULTETA BIOTEHNIŠKA FAKULTETA FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO NARAVOSLOVNOTEHNIŠKA FAKULTETA Študijski program: Kemija in biologija ETANOL, OCETNA IN MLEČNA KISLINA KOT KLJUČNI DRAŽLJAJI ZA PREDELAVO HRANE V ČEBELJI DRUŽINI DIPLOMSKO DELO Univerzitetni študij ETHANOL, ACETIC AND LACTIC ACID AS KEY STIMULI FOR FOOD PROCESSING IN BEE COLONY GRADUATION THESIS University studies Mentor: prof. dr. Janko Božič Kandidatka: Nada Puhalić Ljubljana, 2015
3 II Diplomsko delo je zaključek Univerzitetnega študija Kemije in Biologije na Pedagoški fakulteti v Ljubljani. Laboratorijski poskusi so bili opravljeni na Katedri za etologijo na Oddelku za biologijo Biotehniške fakultete Univerze v Ljubljani, poskusi v panjih pa v panjih v bližini Oddelka za biologijo Biotehniške fakultete. Komisija za dodiplomski študij Oddelka za biologijo je za mentorja diplomskega dela imenovala prof. dr. Janka Božiča. Komisija za oceno in zagovor: Predsednik: prof. dr. Ivan Kos Univerza v Ljubljani, Biotehniška fakulteta, Oddelek za biologijo Član: prof. dr. Janko Božič Univerza v Ljubljani, Biotehniška fakulteta, Oddelek za biologijo Član: doc. dr. Gregor Belušič Univerza v Ljubljani, Biotehniška fakulteta, Oddelek za biologijo Datum zagovora: Delo je rezultat lastnega raziskovalnega dela. Podpisana se strinjam z objavo svojega dela v polnem tekstu na spletni strani Digitalne knjižnice Biotehniške fakultete. Izjavljam, da je delo, ki sem ga oddala v elektronski obliki, identično tiskani verziji. Nada Puhalić
4 III KLJUČNA DOKUMENTACIJSKA INFORMACIJA ŠD Dn DK : (043.2)=163.6 KG AV SA etanol/ocetna kislina/mlečna kislina/dražljaji/med/čebelja družina PUHALIĆ, Nada BOŽIČ, Janko (mentor) KZ SI-1000 Ljubljana, Večna pot 111 ZA Univerza v Ljubljani, Biotehniška fakulteta, Oddelek za Biologijo LI 2014 IN ETANOL, OCETNA IN MLEČNA KISLINA KOT KLJUČNI DRAŽLJAJI ZA PREDELAVO HRANE V ČEBELJI DRUŽINI TD OP IJ JI Diplomsko delo (univerzitetni študij) X, 82 str., 11 pregl., 25 sl., 2 pril., 85 vir. sl sl/en AI Temperatura in vlažnost v panju predstavljata optimalne pogoje za rast in razvoj mikroorganizmov, ki pri pridobivanju energije v procesu fermentacije iz sladkorjev v medu in cvetnem prahu, proizvajajo različne metabolite, med katerimi so etanol, ocetna in mlečna kislina. V prvem delu naše raziskave smo želeli ugotoviti, katere koncentracije ocetne in mlečne kisline čebele pijejo ter ali so sposobne na podlagi asociativnega učenja s pomočjo refleksa iztegovanja jezička med seboj razlikovati raztopine etanola, ocetne in mlečne kisline. Čebele so raje pile nižje koncentracije raztopin ocetne in mlečne kisline. Učenje se je izkazalo za neuspešno, saj čebele niso bile sposobne povezati pogojnega dražljaja z nepogojnim, pri čemer je bil pogojni dražljaj etanol oz. določena organska kislina v raztopini. V drugem delu eksperimenta smo raziskali vlogo naših testnih snovi pri predelavi medu v panju. Celice satja z etanolno raztopino so čebele odpirale, tiste z ocetno in mlečno kislino pa zapirale. Več zapiranja je bilo zabeleženo pri satnih celicah z raztopino ocetne kisline. Dokazali smo vpliv mehanskih poškodb satnih celic na odziv čebel, saj so v nasprotju z majhnimi luknjicami, čebele velike luknjice odpirale. Fermentacijski produkti imajo različno vlogo v panju in zato tudi različno vplivajo na predelavo medu. Etanol predstavlja dražljaj kvarjenja, ocetna in mlečna kislina pa delujeta kot prehranska dražljaja.
5 IV KEY WORDS DOCUMENTATION DN Dn DC : (043.2)=163.6 CX AU AA ethanol/acetic acid/lactic acid/stimuli/honey/bee colony PUHALIĆ, Nada BOŽIČ, Janko (supervisor) PP SI-1000 Ljubljana, Večna pot 111 PB University of Ljubljana, Biotehnical Faculty, Department of Biology PY 2014 TI ETHANOL, ACETIC AND LACTIC ACID AS KEY STIMULI FOR FOOD PROCESSING IN BEE COLONY DT NO LA AL Graduation Thesis (University studies) X, 82 p., 11 tab., 25 fig., 2 ann., 85 ref. sl sl/en AB Temperature and moisture in the hive represent optimal conditions for growth and development of microorganisms, which at obtaining energy in fermentation process from sugars in honey and pollen, produce different metabolites, that include ethanol, acetic and lactic acid. In the first part of our research we wanted to determine which concentrations of acetic and lactic acid the bees consume. We also tried to find out if they are capable of distinguishing ethanol, acetic and lactic acid solutions on the basis of associative learning with proboscis extension reflex. Bees preferred lower concentrations of acetic and lactic acid solutions. The learning turned out to be unsuccessful, because the bees were not able to connect the conditional stimulus with the unconditional stimulus, where the conditional stimulus was ethanol or specific organic acid solution. In the second part of the experiment, we studied the role of our test substances for honey processing in the hive. The bees tended to open the honeycomb cells with ethanol solution, but they closed those with acetic and lactic acid solutions. The closing of a bigger number of cells was noticed at the honeycomb cells with acetic acid solution. We have proved that the mechanical damage in honeycomb cells has an influence on the reaction of the bees. The bees were namely opening the bigger holes and not the smaller ones. Fermentation products have a different role in the hive and this is the reason why they also have a different impact on the honey processing. Ethanol is a stimulus of spoilage, whereas acetic and lactic acid work as food stimuli.
6 V KAZALO VSEBINE KLJUČNA DOKUMENTACIJSKA INFORMACIJA... III KEY WORDS DOCUMENTATION... IV KAZALO VSEBINE... V KAZALO SLIK... VIII KAZALO PREGLEDNIC... X 1 UVOD OPREDELITEV PROBLEMA NAMEN RAZISKAVE RAZISKOVALNE HIPOTEZE PREGLED OBJAV MED KOT GLAVNI ČEBELJI PRIDELEK Zorenje medičine in nastanek medu Kemične in fizikalne lastnosti medu Sestava medu Encimi v medu Kisline pomembne antimikrobne snovi v medu Kristalizacija in vrenje medu Nabiranje in pomen cvetnega prahu PROCES FERMENTACIJE V ČASU ZORENJA MEDU Nastanek biofilma Glukoza kot glavni vir energije mikroorganizmov in proces fermentacije Nastajanje metabolitov mikroorganizmov v panju NASTALI FERMENTACIJSKI PRODUKTI V PANJU Etanol Človek in alkohol Čebele kot izvrsten model za proučevanje vpliva alkohola Etanol kot del življenja čebel Ocetna kislina... 14
7 VI Ocetnokislinske bakterije Ocetna kislina kot del življenja čebel in njena uporaba v čebelarstvu Mlečna kislina Mlečnokislinske bakterije Mlečna kislina kot naravni konzervans Fermentacija cvetnega prahu ter mlečna kislina kot del življenja čebel Mlečna kislina v čebelarstvu UČENJE ČEBEL Asociativno učenje Neasociativne oblike učenja MATERIAL IN METODE ZAZNAVANJE NIZKIH KONCENTRACIJ RAZTOPIN ETANOLA, OCETNE IN MLEČNE KISLINE Opis poskusa Priprava poskusa Pitje raztopin v panju Privajanje čebel na umetno krmišče oz. sladkorno raztopino Priprava raztopin Priprava krmilnika za pitje raztopin ter tehtanje Učenje čebel s PER odzivom Imobilizacija čebel Priprava raztopin Izvedba poskusa Pitje raztopin v panju Učenje čebel Hranjenje s sladkorno raztopino in pitje vode Habituacija Klasično pogojevanje s PER odzivom Učenje z navidezno naključnim razporedom dražljajev Zbiranje in obdelava podatkov Pitje raztopin v panju... 34
8 VII Učenje čebel VPLIV RAZTOPIN NA PREDELAVO MEDU V CELICAH SATJA V PANJU Opis poskusa Priprava poskusa Priprava raztopin Izvedba poskusa Različni načini vbrizgavanja raztopin v celice satja Preverjanje vpliva mehanskih poškodb satnih celic v panju Zbiranje in obdelava podatkov REZULTATI ZAZNAVANJE NIZKIH KONCENTRACIJ RAZTOPIN ETANOLA, OCETNE IN MLEČNE KISLINE Pitje raztopin Učenje čebel VPLIV RAZTOPIN NA PREDELAVO MEDU V CELICAH SATJA V PANJU Preverjanje vpliva mehanskih poškodb satnih celic v panju RAZPRAVA IN SKLEPI RAZPRAVA Zaznavanje nizkih koncentracij raztopin etanola, ocetne in mlečne kisline Vpliv raztopin na predelavo medu v celicah satja v panju Uporabnost rezultatov za nadaljnje raziskave SKLEPI POVZETEK PRENOS PRIDOBLJENEGA ZNANJA NA POUK V OSNOVNI ŠOLI UVRSTITEV TEME DIPLOMSKEGA DELA V UČNI NAČRT ZA OŠ UČNA PRIPRAVA TER POTEK DELA VIRI ZAHVALA, PRILOGE
9 VIII KAZALO SLIK Slika 1a, b: Vpenjanje čebele v tulec Slika 2: Vpete čebele, pripravljene za učenje Slika 3: Pripravljeni krmilniki za pitje raztopin postavljeni v panju Slika 4: Čebele med pitjem kontrolne raztopine Slika 5: Hranjenje čebele s sladkorno raztopino preko filtrirnega papirčka Slika 6: Drugi vpogled dogajanja v satju, kjer je bila vbrizgana raztopina mlečne kisline. 37 Slika 7: Drugi vpogled dogajanja v satju, kjer je bila vbrizgana raztopina ocetne kisline.. 37 Slika 8: Volumen popitih raztopin dne Slika 9: Volumen popitih raztopin dne Slika 10: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z 2% raztopino etanola Slika 11: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z 2% raztopino etanola (ponovitev poskusa po 30 min) Slika 12: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino ocetne kisline Slika 13: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino ocetne kisline (ponovitev poskusa po 30 min) Slika 14: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino mlečne kisline Slika 15: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino mlečne kisline (ponovitev poskusa po 30 min) Slika 16: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z eteričnim oljem sivke Slika 17: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z eteričnim oljem sivke (ponovitev poskusa po 30 min)
10 IX Slika 18: Indeks stanja satnih celic v odvisnosti od časa v satu z 2% raztopino etanola Slika 19: Indeks stanja satnih celic v odvisnosti od časa v satu z 2% raztopino mlečne kisline Slika 20: Indeks stanja satnih celic v odvisnosti od časa v satu z 1% raztopino ocetne kisline Slika 21: Indeks stanja satnih celic z vbrizgano 2% raztopino mlečne kisline glede na kontrolo po 1 h 20 min (prvi vpogled snovi) ter naslednji dan Slika 22: Indeks stanja satnih celic z vbrizgano 1% raztopino ocetne kisline glede na kontrolo po 1h 20 min (prvi vpogled snovi) ter naslednji dan Slika 23: Indeks stanja satnih celic z vbrizgano 2% raztopino etanola glede na kontrolo po 1h 20 min (prvi vpogled snovi) ter naslednji dan Slika 24: Indeks stanja satnih celic z vbrizganimi raztopinami v primerjavi z različno velikimi luknjicami Slika 25: Pripravljeno krmišče za čebele v bližini panja
11 X KAZALO PREGLEDNIC Preglednica 1: Prikaz numeričnih vrednosti posameznih satnih celic Preglednica 2: Prikaz deleža popite testne raztopine glede na kontrolno raztopino dne Preglednica 3: Prikaz deleža popite testne raztopine glede na kontrolno raztopino dne Preglednica 4: Prikaz števila različnih stanj satnih celic s snovmi, razporejenimi po satih glede na čas Preglednica 5: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v prvem satu, kamor je bila na začetku dodana etanolna raztopina Preglednica 6: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v drugem satu, kamor je bila na začetku dodana raztopina mlečne kisline Preglednica 7: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v tretjem satu, kamor je bila na začetku dodana raztopina ocetne kisline Preglednica 8: Prikaz števila različnih stanj satnih celic po eni uri pri satnih celicah z vbrizgano vodo in posamezno testno raztopino Preglednica 9: Prikaz števila različnih stanj satnih celic po eni uri pri različno velikih luknjicah Preglednica 10: Porazdelitev frekvenc satnih celic po tretmanih glede na odpiranje Preglednica 11: Navzkrižni diagram izračunanih χ2 testov
12 1 1 UVOD 1.1 OPREDELITEV PROBLEMA Glavni proizvod medonosne čebele je nedvomno med, ki je lahko cvetlični ali gozdni, kar je odvisno od mesta nabiranja le-tega. Cvetlični med je med iz nektarja oz. medičine, ki jo čebele nabirajo na medonosnih rastlinah, gozdni med pa je med nastal iz mane oz. medene rose. Zaradi visoke vsebnosti ogljikovih hidratov predstavlja med čebelam glavni vir energije za njihovo delovanje. Pašne čebele nabrano medičino odnašajo v panj in jo predajo panjskim čebelam, te jo nato odlagajo v celice satja. Poleg večkratnega prelaganja medičine iz ene satne celice v drugo ter utripanja kril, pa čebele delavke tudi z encimi iz sline pripomorejo k še hitrejšemu zgoščevanju in zorenju medu, saj začetna medičina vsebuje veliko vode. Ko je med dozorel, začnejo čebele celice zapirati z voščenimi pokrovci (Winston, 1987). Pred tem pa je zgornji del vsake celice z medom v tankem sloju, ki ga imenujemo biofilm, izpostavljen različnim dejavnikom v panju, kot so toplota, vlažnost ter prisotnost kisika. Takšni pogoji so kot nalašč ustvarjeni za rast in razvoj mikroorganizmov, ki jih čebele lahko prenesejo v panj tudi s cvetlic (Snowdon in Cliver, 1996). Mikroorganizmi pri presnovi organske hrane proizvedejo različne metabolite, med katerimi so tudi organske kisline in alkoholi. Kvasovke izločajo encime, ki povzročajo alkoholno fermentacijo sladkorjev do etanola in ogljikovega dioksida. Pri nadaljnji fermentaciji etanola s pomočjo ocetnokislinskih bakterij oz. pri njegovi oksidaciji pride do nastanka ocetne kisline (Berg in sod., 2007). Tudi cvetni prah, položen v satnih celicah, kmalu fermentira ob prisotnosti mlečnokislinskih bakterij, pri tem nastaja mlečna kislina (Božnar, 2011). Torej sta obe kislini, tako mlečna kot ocetna, ter tudi alkohol etanol ves čas prisotni v panju in so del življenja čebelje družine. Te snovi predstavljajo čebelam ključne dražljaje za predelavo hrane v panju. Tudi med vsebuje poleg sladkorjev, beljakovin, rudninskih snovi, aminokislin, vitaminov, lipidov in ostalih snovi, primesi organskih kislin in alkoholov, ki mu dajo značilen vonj in okus.
13 2 1.2 NAMEN RAZISKAVE Naše raziskovanje je bilo usmerjeno k razlagi vloge fermentacijskih produktov mikroorganizmov v čebelji družini, in sicer predvsem, kako te posamezne snovi, ki delujejo kot ključni dražljaji v panju, vplivajo na predelavo hrane - medu. Sprva smo preverili, ali čebele sploh zaznajo nizke koncentracije raztopin etanola, ocetne in mlečne kisline, relevantnih za predelavo medu. Raziskavo smo nato nadaljevali z opredelitvijo vloge posameznih snovi, tako da smo poskušali ugotoviti, ali etanol, ocetna in mlečna kislina čebelam predstavljajo le prehranski dražljaj, ki povzroči takojšnje konzerviranje hrane in zapiranje satnih celic, ali pa delujejo kot dražeče kemične snovi, ki čebele spodbudijo k še večji predelavi medu. 1.3 RAZISKOVALNE HIPOTEZE Postavili smo si sledeče hipoteze: Predvidevamo, da so čebele sposobne zaznati in razlikovati nizke koncentracije raztopin etanola, ocetne in mlečne kisline. Predvidevamo, da etanol, ocetna in mlečna kislina različno vplivajo na predelavo medu v panju, saj se tudi vloga teh snovi v panju med seboj razlikuje. Etanol in ocetna kislina delujeta kot dražeči snovi in povzročata odpiranje satnih celic, mlečna kislina pa kot konzervans, ki pri čebelah privede do odzivnega vedenja, da pričnejo hrano konzervirati oz. celice satja zapirati.
14 3 2 PREGLED OBJAV 2.1 MED KOT GLAVNI ČEBELJI PRIDELEK Čebela nas je zaradi svojih proizvodov že od nekdaj zanimala, med pa je zagotovo eden izmed prvih znanih izkoriščenih čebeljih pridelkov s strani človeka. Bil je celo edino in najcenejše sladilo pred pojavom sladkorja (Ambrose, 1992). Med je gosto tekoča, naravna, sladka snov, ki jo čebele izdelajo iz medičine (nektarja), nabrane na cvetovih medonosnih rastlin ali pa iz mane/medene rose (Bokal in Gregori, 2008), ki je sladek izloček v obliki kapljic oz. predelan floemski sok nekaterih kljunatih žuželk živečih na smrekah in jelkah, mednje spadajo listne ušice, škržati in kaparji. Mana poleg sladkorjev glukoze, fruktoze in saharoze, ki prevladujejo v medičini, vsebuje še nekatere trisaharide, ki so za čebele težje razgradljivi sladkorji in jim lahko povzročajo celo prebavne motnje (Bogdanov in sod., 2004), lahko pa vsebuje tudi nekatere čebelam škodljive snovi. Prav tako so vir sladkih tekočin za čebele tudi nekateri drugi izločki živih rastlinskih delov ali pa celo sokovi poškodovanega sadja (Božič, 1998). Mesto nabiranja surovine za izdelavo medu določa njegovo vrsto, zato razlikujemo dve glavni kategoriji medu, to sta cvetlični med, ki je narejen iz medičine, ter gozdni med iz mane (Bokal in Gregori, 2008). Danes so številni čebelji pridelki del naše vsakdanje kulinarike, njihova uporaba pa se vedno bolj usmerja tudi v zdravstvene namene. Zaradi vsega tega je čebelarstvo tako pri nas, kjer je doživelo razcvet v 18. in 19. st., kot drugod po svetu zelo cenjeno. V Sloveniji gojimo našo avtohtono čebeljo raso Apis mellifera carnica (Pollmann, 1879) - kranjska čebela ali na kratko sivka. Naša čebela, ki je podvrsta medonosne čebele Apis mellifera, se od ostalih čebel razlikuje po intenzivnem spomladanskem razvoju, mirnem značaju, dolgoživosti, sposobnosti nabiranja medičine v različnih geografskih in podnebnih okoljih, izjemni delavnosti in orientaciji ter dobremu prezimovanju s skromno porabo zimske zaloge hrane. Na videz je vitka, ima sivkasto rjave dlačice in izrazito dolg jeziček (Winston, 1987). Čebela je socialna žuželka in sama ni sposobna preživeti, tako živi kot del homogene čebelje družine. Avtor knjige Čudežni svet čebel, Jürgen Tautz (2010), je mnenja, da delujejo vsi člani čebelje družine skupaj s satovjem kot nekakšen superorganizem, saj je organiziranost dela ter usklajenost in sposobnost same družine zanj ena izmed najbolj presenetljivih življenjskih oblik, kar jih poznamo. Čebele primerja celo z višje razvitimi vretenčarji sesalci. Manjšo čebeljo družino sestavlja približno čebel, med katerimi je ena plodna matica, nekaj sto začasnih trotov, ostalo so nereproduktivne čebele delavke, ki nagonsko, glede na svojo starost, ki določa razvoj različnih žlez, opravljajo določena dela v čebeljem gnezdu. Samo stanje žlez in s tem opravljanje posameznih nalog pa lahko variira, saj je pogojeno glede na potrebe čebelje
15 4 družine. Kljub stalni menjavi življenjskih pogojev znotraj panja čebele skrbijo za vzpostavljeno ravnotežje tako, da vzporedno s temi spremembami prilagodijo svoje vedenje, učenje in sam razvoj (Winston, 1987) Zorenje medičine in nastanek medu Izločanje medičine je odvisno od aktivnosti fotosinteze pri posamezni rastlini, saj takrat poteka sinteza sladkorjev, ki so poleg kisika glavni produkt tega avtotrofnega procesa. Pašna čebela v enem poletu s cvetov nabere približno 50 do 60 mg medičine, od tega porabi za svojo energijo 10%, ostalo shrani v svojem mednem želodčku in odnese v panj (Adamič in sod., 1984). Medičina vsebuje poleg vode in sladkorjev tudi rudninske snovi, vitamine, zrnca cvetnega prahu, eterična olja in organske kisline (White, 1975). V mednem želodčku čebele se medičina prepoji z izločki slinske in goltne (krmilne) žleze, kar pripomore k pričetku spreminjanja njegove kemijske sestave (Ball, 2007). Pašne čebele ob prihodu v panj nabrano medičino/mano oddajo čebelam delavkam, ki morajo začetno medičino zgostiti, saj le-ta vsebuje veliko količino vode in je kot taka neprimerna za shranjevanje v satnih celicah. Zgoščevanje medičine ter s tem nastajanje oz. dozorevanje medu se začne in konča v panju. Čebele v panju s posebni gibi iztisnejo medičino iz medne golše in jo na koncu svojega jezička v obliki kapljice sušijo na toplem in suhem zraku okrog 5-10 sekund. Nato jo ponovno vsrkajo v medno golšo ter celoten postopek ponovijo, vse skupaj traja približno 20 minut. Na ta način medičino še bolj prepojijo s svojimi izločki žlez. Ko postane dovolj gosta, jo odložijo v satno celico, kjer še naprej dozoreva. Postopoma se spreminja v med, kar v ugodnih razmerah traja od 3 do 4 dni. Čebele tako pripravijo med za svojo sezonsko zalogo ter za hrano ličinkam (Winston, 1987). Poleg večkratnega prelaganja medičine iz ene satne celice v drugo pa k hitrejšemu izhlapevanju vode pripomore tudi utripanje kril in s tem sušenje zraka v panju, kar povzroči znižanje relativne vlage na zgornjo mejo 66%. Prav tako pa imajo pri dozorevanju medu pomembno vlogo različni encimi invertaza, diastaza in glukozna oksidaza iz žlez čebel delavk (Winston, 1987). Surova medičina vsebuje različne količine ogljikovih hidratov in saharoze, ki med delovanjem hidrolitičnih encimov pri nastajanju medu razpadejo na enostavne sladkorje kot sta glukoza in fruktoza, lahko pa pride tudi do nastanka nekaterih drugih enostavnih sladkorjev. Zato je sladkorni spekter medu še kako pomemben pokazatelj določene vrste medu, vidno pa je tudi delovanje rastlinskih in živalskih invertaz (Božnar in Senegačnik, 1998). Uspešnost sušenja medičine oz. mane je odvisna od več dejavnikov, kot so jakost čebelje družine in število mladih čebel, intenzivnost paše, vsebnost vode oz. vsebnost sladkorjev v medičini, vlažnost in temperatura ter napolnjenost posameznih satnih celic. Za hitrejše zorenje medu čebele kapljice medičine pritrjujejo na zgornje stene celice ter satno celico polnijo do prve tretjine, kajti pri tako napolnjenih celicah je izparevanje vode celo 3x hitrejše kot pri
16 5 celicah, ki so skoraj do vrha zapolnjene (Meglič, 2004). Ko je med v satnih celicah zrel, čebele pokrijejo celice z voščenimi pokrovci. Pokrovci so, tako kot celotno satje, zgrajeni iz voska, ki nastaja v t.i. voskovnih žlezah na spodnji strani zadka mladih čebel, in so za vodo in zrak neprepustni. Maksimalna količina vode v zrelem medu je približno 18,6%, saj bi lahko v drugačnem primeru prišlo do vrenja (Božnar in Senegačnik, 1998). Tako je nastanek medu kombinacija procesa inverzije saharoze ter procesa izparevanja vode (Ball, 2007) Kemične in fizikalne lastnosti medu Sestava medu S pomočjo kemičnih analiz, ki so se v zadnjih letih še bolj razvile, lahko ugotovimo kakovost medu in tako omogočimo porabnikom čim bolj pristen med. Med je koncentrirana raztopina sladkorjev, med katerimi prevladujejo grozdni (glukoza ali dekstroza), sadni (fruktoza ali levuloza) in trsni sladkor (saharoza). Možen je pojav nekaterih drugih sladkorjev, poleg njih pa so prisotne še številne druge spojine: aminokisline, beljakovine, vitamini, encimi, rudninske in organske snovi. Sladkorja glukoza in fruktoza sta skupna vsem vrstam medu, snovi, ki se v medu nahajajo v manjših količinah, pa povzročajo razlike med posameznimi vrstami medu, kot so barva, vonj in okus. Mednje uvrščamo mineralne snovi, vitamine, encime, beljakovine, kisline, flavonoide, hormone, aromatične snovi in inhibine (Golob in sod., 2008). Med vsebuje torej največ monosaharidov, enostavno zgrajenih ogljikovih hidratov, in sicer 27 do 36% glukoze, 33 do 42% fruktoze ter 1 do 4% disaharida saharoze. Lahko rečemo, da vsebuje skupaj 76% sladkorjev, približno 18% vode ter 6% drugih snovi. Razmerje med posameznimi sladkorji in njihova količina določata tudi nekatere fizikalne lastnosti medu npr. kristalizacijo medu, k temu pa veliko prispeva tudi encim invertaza, ki raztopino saharoze cepi v izenačeno mešanico glukoze in fruktoze. Prebava glukoze in fruktoze v čebeljem telesu je hitra in poteka neposredno, zato predstavljata ta dva sladkorja glavni pogonski sestavini oz. glavni vir energije za delovanje telesa (Božnar in Senegačnik, 1998). Različne raziskave gozdnega medu nastalega iz mane kažejo, da lahko ta vsebuje še nekatere druge vrste sladkorjev, ki naj bi nastale kot posledica encimske pretvorbe sladkorjev floemskega soka v prebavnem traktu kljunatih žuželk (Bacon in Dickinson, 1957). Tako vsebuje manin med v nasprotju z medom iz nektarja več disaharidov in oligosaharidov, predvsem veliko melecitoze in rafinoze (Nazol in sod., 2005; Kmecl, 2006). Raziskava vsebnosti sladkorjev v 63 vzorcih slovenskega medu (letnik 2005) različnih vrst (cvetlični, akacijev, gozdni in smrekov med) s pomočjo anionsko izmenjevalne tekočinske kromatografije HPAEC-PAD je pokazala, da so poleg melecitoze in rafinoze, kjer je bila zabeležena največja povprečna količina obeh sladkorjev v
17 6 smrekovem medu (mel.: 2,72 g/100 g; raf: 2,23 g/100 g), manini medovi od trisaharidov vsebovali tudi več maltotrioze (smrekov: 0,97 g/100 g) ter erloze (gozdni: 2,54 g/100 g), medtem ko je bila količina sladkorja panoze v vseh medovih približno enaka. Pri disaharidih je gozdni med v primerjavi s cvetličnim vseboval več palatinoze, turanoze ter gentibioze z izomaltozo (Kasenburger, 2006) Encimi v medu K nastajanju medu iz medičine ogromno pripomorejo encimi, ki v največji meri izvirajo iz goltnih in slinskih žlez čebel delavk, zato so te snovi, ki so po izvoru beljakovine, v medu še kako pomembne. Omogočajo presnovo in pospešujejo hitrost kemijskih reakcij, tako da zmanjšajo aktivacijsko energijo, ki je potrebna, da neka reakcija sploh poteče. V medu so pomembni trije encimi: invertaza, amilaza in glukoza oksidaza (Božnar in Senegačnik, 1998). Encim invertaza, ki je dejansko α-glukozidaza, je prisoten že v medičini, njegova količina pa se pri predelavi medičine v med poveča, saj se dodatno izloči iz krmilnih žlez čebel delavk. Ta encim ima veliko specifičnost za saharozo in povzroča invertiranje medu, pri tem se saharoza razgradi na molekuli glukoze in fruktoze (invertni sladkor). Enostavni sladkorji lahko v nasprotju s saharozo prehajajo direktno v kri. Encim amilaza oz. diastaza cepi velike škrobne molekule do molekul maltoze in je pomemben pri analizi pristnosti medu. V nezrelem medu pa je prisoten tudi encim glukoza oksidaza, katerega aktivnost je največja, ko je koncentracija sladkorja od 25 do 30%. Njegova vloga je oksidacija sladkorja glukoze do glukonske kisline, ki velja za glavno kislino v medu, stranski produkt te reakcije pa je vodikov peroksid. V času spreminjanja medičine v med vodikov peroksid nastaja ter prav tako tudi pod vplivom encima katalaza razpada nazaj v vodo in kisik, zaradi tega ga uvrščamo med močne oksidante, saj kisik nastal ob razpadu vodikovega peroksida oksidira ostale anorganske in organske spojine. Z raziskavami so dokazali, da vodikov peroksid deluje baktericidno in daje medu posebne antimikrobne lastnosti (Kwakman in sod., 2010). Nekatere antimikrobne snovi v medu izvirajo že iz nabrane medičine oz. mane, največ pa se jih izloči iz čebeljih ustnih žlez med zgoščevanjem medičine (encim glukoza oksidaza, peptid defenzin) (Kwakman in sod., 2010). Med se je že od nekdaj uporabljal za celjenje odprtih ran, opeklin, kožnih razjed in vnetega grla. Lahko si razlagamo, da so terapevtske lastnosti medu posledica nastajanja vodikovega peroksida, pa tudi posebnih snovi, značilnih za medičino, kot so flavonoidi in fenolne kisline, od katerih je še posebej odvisna antioksidativna učinkovitost medu (Taormina in sod., 2001; Mato in sod., 2003). Ko med dozori in vsebuje minimalno količino vode, se delovanje encima glukoza oksidaza popolnoma ustavi, vendar pa takrat plazmolizo celic mikroorganizmov večinoma povzroči njegova visoka osmolarnost oz. velika količina sladkorjev (Baker H.G. in Baker I., 1982).
18 Kisline pomembne antimikrobne snovi v medu Glavni krivci za različen okus in vonj posameznih vrst medu so kisline, med katerimi sta od anorganskih pomembni predvsem fosforna in solna kislina, med pa vsebuje tudi številne organske kisline (ocetna, mlečna, mravljična, glukonska, jabolčna, oksalna, citronska, maslena, jantarna kislina itd.) (Adamič in sod., 1984). V medu so zelo nizke vrednosti organskih kislin, zavzemale naj bi le 0,5% delež medu. S pomočjo različnih tehnik, kot so encimska metoda ter nekatere vrste kromatografij (papirna, ionsko izmenjevalna ), so v medovih identificirali 19 različnih organskih kislin (Suárez-Luque in sod., 2002). V 30. letih prejšnjega stoletja so bili ljudje mnenja, da sta citronska in jabolčna kislina primarni organski kislini v medu. Šele leta 1960 so Stinson in sod. dokazali dominantnost glukonske kisline. Vse kisline izvirajo večinoma iz ustne slinavke čebele in medičine same, le malo z rastlin. Vrednost ph je merilo za kislost raztopine in je odvisna od koncentracije oksonijevih ionov (H 3 O + ) v njej. Raziskave različnih vrst medu so pokazale, da se ph vrednost medu giblje od 3,2 do 4,5, v povprečju okrog 3,9 (Ball, 2007). To pomeni, da kisline v medu vzdržujejo dokaj nizek ph in dokazano povečujejo njegovo obstojnost proti različnim mikroorganizmom (Kwakman in sod., 2010). Dosedanje študije kažejo tudi na to, da so za antibakterijske lastnosti medu presenetljivo pomembne le aromatske organske kisline (kavna in ferulna kislina ter derivati benzojske kisline) (Russsell, 1990). White in Landis Doner (1980) sta v vzorcih ameriškega medu maninega izvora potrdila prisotnost večjih količin mineralnih snovi, kot so soli natrija, kalija in kalcija, ki vrednost ph medu zvišajo, ter večjo količino prostih in skupnih kislin, a manjšo vsebnost laktonov (glukonoδ-lakton) v primerjavi z medom iz nektarja. Sama kislost medu služi kot pomemben pokazatelj primernosti shranjevanja medu, kaže na njegovo starost, čistost in pristnost (White, 1978) Kristalizacija in vrenje medu Med ima številne fizikalne in kemične lastnosti, tu bi bilo zanimivo izpostaviti kristalizacijo in vrenje. Kristalizacija je fizikalen in naraven pojav, ki se pojavi, ko začne glukoza v medu tvoriti kristale. Kljub temu, da glukoza ni več tekoča, pa ostaja fruktoza v tekočem stanju in okrog kristalov glukoze tvori tanek sloj. Če je v medu večja količina glukoze, med hitreje kristalizira in obratno. Ta proces je torej odvisen od razmerja glukoze in fruktoze v medu. Poleg tega so tu še dodatni razlogi, ki pripomorejo k strjevanju, to so nižja temperatura (10 20 C), razni tuji delci v medu ter njegovo mešanje in tresenje (Adamič in sod., 1984). Velik vpliv na ta fizikalen pojav ima tudi vsebnost trisaharida melecitoze, ki se v vodi slabo topi in hitro kristalizira, takšnemu medu pa pravimo cementni med, saj ga je včasih celo nemogoče iztočiti (Kmecl, 2006). Vsak med tako slej ko prej kristalizira, obstajajo le redke izjeme. Med lahko ponovno vrnemo v tekoče stanje, če ga segrejemo, vendar temperatura ne sme preseči 40 C, saj s tem uničimo nekatere zdravilne snovi ter mu na ta način zmanjšamo biološko in hranilno vrednost. Če je v medu
19 8 več vode, pride do nastanka vrenja ali fermentacije, pojava kemične narave. To se lahko zgodi tudi v kristaliziranem medu, ki vsebuje nekoliko več vode, saj je kristalizirana glukoza ne more v celoti vezati nase (Božnar in Senegačnik, 1998). Fermentacija medu poteka pod vplivom mikroorganizmov, ki za svoje razmnoževanje koristijo hranilne snovi iz okolice, v tem primeru so to sladkorji v medu. Kvasovke s pomočjo svojih encimov presnavljajo sladkorje do alkohola etanola in ogljikovega dioksida. Etanol pod vplivom mikroorganizmov še naprej razpade do ocetne kisline in vode, medtem ko preostali plin ogljikov dioksid izhlapi. Proces vrenja, ki je hitrejši v prisotnosti kisika in pri temperaturi med 13 in 21 C, povzroča kvarjenje in kislost medu. Če je v medu koncentracija sladkorjev visoka, kvasovke ne morejo delovati. Prav zaradi vsega tega je potrebno paziti in se izogibati shranjevanju medu v vlažnih prostorih, saj je med higroskopičen in nase veže vodo, zato lahko v takšnih razmerah pride hitro do razvoja kvasovk in posledično vrenja (Baker H. G. in Baker I., 1982) Nabiranje in pomen cvetnega prahu Prav tako kot medičino čebele na cvetovih nabirajo tudi cvetni prah, ki je poleg medu in vode njihova najpomembnejša hrana. Nabiranje opravijo s pomočjo posebnih naprav na zadnjih nogah, to sta košek in ščetka, ki sta obrasla z dlačicami, na katere se pelod sprime (Adamič in sod., 1984). Ko čebela zbira pelod, ga sproti vlaži s slino, medičino ali medom iz svojega mednega želodčka ter ga izoblikuje v posebne grudice, imenovane obnožina. Cvetni prah ima izredno bogato hranilno vrednost, predvsem lahko rečemo, da je glavni vir beljakovin, ki so nujno potrebne za rast ličink, pomemben pa je tudi za pravilno delovanje čebeljih voskovnih žlez. Vsebuje namreč 6 do 28% beljakovin ter tudi lipide, ki so prav tako bistven del čebelje prehrane (Winston, 1987). Ko čebela prinese pelod v panj, začne z njim polniti satne celice tako, da jih napolni le do 2/3 ter pokrije z medom. Takšen način shranjevanja cvetnega prahu omogoča njegovo zaščito pred kvarjenjem. Čebelja družina naj bi v enem letu porabila približno 70 kg medu in 20 do 30 kg cvetnega prahu (Javornik in sod., 1982). Ta podatek nam pove, da sta ti dve snovi poglavitni za življenje, rast in razvoj čebelje družine. S preletavanjem z enega cveta na drug cvet čebele prenašajo cvetni prah ter s tem pripomorejo k spolnemu razmnoževanju rastlin. Poleg čmrljev so ene izmed najpomembnejših opraševalcev in tako stalno vzdržujejo ravnovesje v naravi oz. biodiverziteto vegetacije. Vsaka rastlina ima cvetni prah, ki je zanjo specifičen, zato lahko na podlagi strukture pelodnih zrn, ki jih vsebuje med, ugotovimo, na kateri rastlini je čebela nabirala medičino ter tako določimo vrsto medu. Nabiranje medičine na različnih cvetovih je vzrok za različen okus, vonj in barvo medu (Adamič in sod., 1984).
20 9 2.2 PROCES FERMENTACIJE V ČASU ZORENJA MEDU Nastanek biofilma Dnevno obleti pašna čebela do 4000 cvetov in pri tem izleti iz panja 7 do 17-krat. V mednem želodčku lahko shrani 8 do 9 mg medičine, za kar potrebuje 20 minut. Do paše letajo čebele tudi do 2 km daleč, v primeru, da je paša bolj oddaljena, so donosi medičine ali peloda manjši (Javornik in sod., 1982). Z nabrano medičino in pelodom čebele v panj pogosto prenesejo tudi različne mikroorganizme ali pa le-ti izvirajo iz čebelje črevesne mikrobiote (Anderson in sod., 2011). Temperatura in vlažnost v panju predstavljata optimalne pogoje za rast in razvoj mikroorganizmov (Snowdon in Cliver, 1996). Poleg tega potrebujejo mikroorganizmi za svojo rast še hranila ter ustrezno podlago, na kateri začnejo kmalu tvoriti mikrokolonijo oz. biofilm. Gre za kompleksno zgrajen in dinamičen biološki sistem, ki ga večinoma sestavlja več različnih vrst mikroorganizmov, ki skupaj delujejo tako dovršeno, da so celo analogni večceličnim organizmom. V biofilmu okrog sebe ustvarijo zunajcelični matriks iz polimernih snovi (angl. extracellular polymeric substances EPS), ki jih drži skupaj in služi kot zaščitni sloj pred tujki, a hkrati omogoča prenos potrebnih hranil. Takšen sistem predstavlja ključni faktor preživetja v različnih okoljih, saj je na tak način povečana odpornost mikroorganizmov proti neugodnim vplivom iz okolja, lažja je dostopnost do hranil, mikroorganizmi postanejo bolj stabilni in prilagodljivi ter imajo večjo možnost širjenja svojih kolonij v nove niše (Lindsay in von Holy, 2006). Zaradi idealnih pogojev v še nepokritih satnih celicah v panju v času zorenja medu tudi tam pride do razvoja in diferenciacije mikroorganizmov oz. nastanka biofilma. Pri odpiranju panja ali pri prelaganju satov in s tem daljši izpostavljenosti še nepokritih satnih celic zraku, obstaja velika verjetnost neposredne okužbe takšnih celic z mikroorganizmi ali absorpcije vode iz zraka, s čimer se ustvari primerno vlažno okolje za njihov razvoj. Kvasovke in bakterije v panju so glavni povzročitelji fermentacije Glukoza kot glavni vir energije mikroorganizmov in proces fermentacije Organizmi za svojo rast in razvoj potrebujejo energijo, ki jo pridobijo s hranilnimi snovmi iz okolice. Glavni vir energije večine živih organizmov je glukoza. Do sproščanja energije pride pri oksidativni razgradnji tega monosaharida s pomočjo glikolitičnih encimov v citosolu celic oz. na kratko pri glikolizi (Boyer, 2005). Samo sproščanje energije je posledica sklopa redoks reakcij oz. oddajanja in sprejemanja elektronov med molekulami ter poteka v smeri od reducenta do oksidanta (Stušek, 1999). Energijsko bogata molekula glukoza se razcepi na dve molekuli piruvata s tremi ogljikovimi atomi (Stušek, 1999). Nadaljnji metabolizem piruvata, ki je glavni produkt razpada glukoze, je odvisen od
21 10 prisotnosti kisika. V aerobnih celicah je končni prejemnik elektronov kisik, to je proces celičnega dihanja. Mnogi mikroorganizmi, med katere uvrščamo med drugim tudi kvasovke in bakterije, pa energijo v obliki ATP-ja (adenozin trifosfata) pridobivajo tudi po anaerobni metabolni poti. Fermentacija ali vrenje je torej drugi način pridobivanja energije v okolju brez kisika, kjer je končni prejemnik elektronov organska snov (Boyer, 2005). Glede na končni produkt, ki je odvisen od vrste organizma, v katerem fermentacija poteče, ločimo več vrst fermentacije. Če je akceptor elektronov organska molekula s tremi ogljikovimi atomi, nastaja mlečna kislina, če pa se od ostankov glukoze s pomočjo encimov odcepita molekuli ogljikovega dioksida in postane akceptor elektronov organska snov z dvema ogljikovima atomoma, nastaneta molekuli alkohola etanola (Stušek, 1999). Na takšen način ločimo mlečnokislinsko in alkoholno vrenje. Proces vrenja ljudje izkoriščajo že več tisočletij, saj so kljub svoji nevednosti glede samega delovanja tega biokemijskega procesa, uvideli njegove pozitivne učinke. Predvsem ima velik pomen v živilski in kemični industriji ter medicini. Številni produkti kot so npr. industrijske kemikalije in zdravila nastajajo v biotehnoloških procesih, kjer uporabljajo izbrane mikroorganizme, s pomočjo katerih pod točno določenimi pogoji iz raznih surovin pripravijo posamezne nove snovi (Stušek, 1999). Ljudje so prišli do spoznanja, da nekateri nastali metaboliti mikroorganizmov pri procesu vrenja, lahko celo izboljšajo kakovost in obstojnost določenih snovi, zato jih že od nekaj uporabljajo za različne namene Nastajanje metabolitov mikroorganizmov v panju Mikroorganizmi pri presnovi organske hrane pod anaerobnimi pogoji izločajo encime, ki povzročijo fermentacijo te hrane, zato pride do nastanka različnih metabolitov oz. fermentacijskih produktov. Glavni vir organskih snovi so sladkorji v medu in cvetnem prahu. Pri alkoholni fermentaciji s pomočjo gliv kvasovk iz sladkorja nastane alkohol etanol in ogljikov dioksid, nadaljnje delovanje kvasovk oz. ocetnokislinskih bakterij v procesu ocetnokislinskega vrenja pa privede do oksidacije etanola v etanojsko kislino in vodo. Zaradi prisotnosti in delovanja mlečnokislinskih bakterij pa fermentira tudi cvetni prah, položen v satnih celicah, ki ga čebele obogatijo z izločki svojih žlez. Pri tem nastaja mlečna kislina, ki je prav tako sestavni del medu. Med samim procesom fermentacije pride do sproščanja energije v obliki molekul ATP, ki jo mikroorganizmi izkoristijo za rast in razmnoževanje svojih celic. Vsi ti fermentacijski produkti, kot so etanol, ocetna in mlečna kislina, so torej posledica presnove mikroorganizmov in so ves čas prisotni v panju. Metaboliti so del življenja čebelje družine in čebelam v panju predstavljajo ključne dražljaje za predelavo medu, saj nastajajo med njegovim zorenjem. Tudi zrel med vsebuje primesi organskih kislin ter alkoholov, ki so glavni razlog za določen vonj in okus medu. Mlečnokislinska in ocetnokislinska fermentacija tudi dodatno pripomoreta k povečanju naravne kislosti medu.
22 NASTALI FERMENTACIJSKI PRODUKTI V PANJU Etanol Etanol ali etil-alkohol s kemijsko formulo C 2 H 5 OH je pri sobni temperaturi brezbarvna, strupena tekočina značilnega vonja, ki se meša z vodo v vseh razmerjih, pa tudi z večino organskih raztopin. Gori z zelo vročim modrikastim plamenom (Perpar, 1948). Spada med prve znane organske spojine, saj njegovo pridobivanje temelji na alkoholnem vrenju ogljikovih hidratov, s katerim so se srečali že naši predniki (Kornhauser, 1998). Večino etanola, ki se uporablja za industrijske namene, pa proizvedejo na drugačen način, npr. s kislinsko katalizirano hidracijo etena (Solomons in Fryhle, 2008). Alkoholno fermentacijo povzročajo enocelične glive kvasovke, ki z encimom cimaza katalizirajo pretvorbo sladkorja v alkohol etanol in CO 2 (Šešek, 1978). Pri tem procesu glikolizi v anaerobnih celicah sledita še dve dodatni reakciji, kjer pride sprva do nehidrolitične cepitve piruvata, ki ga katalizira piruvat-karboksilaza skupaj s koencimom tiaminpirofosfatom, ter do nastanka acetaldehida. Tukaj se odcepi še molekula CO 2, nadaljnja redukcija karbonilne skupine v acetaldehidu s pomočjo alkohol-dehidrogenaze, pa vodi do nastanka etanola (Berg in sod., 2007). Izhodiščne in glavne surovine za proizvodnjo etanola so žito, sadje, krompir in riž, torej pridelki, ki vsebujejo velike količine sladkorjev ali škroba (Kornhauser, 1998). Razkroj škroba do sladnega sladkorja oz. maltoze katalizirajo diastatični encimi, ki se nahajajo v kalečem žitu (Perpar, 1948) Etanol je ključna sestavina alkoholnih pijač. Pri nastajanju etanola razlikujemo dve fazi, in sicer glavno vrenje, kjer se večino sladkorja pretvori v alkohol, ter povrevanje, ki je v nasprotju s prvim bolj počasno in pri katerem dokončno razpadejo še ostanki sladkorja. Zlasti pri povrevanju nastanejo poleg glavnih dveh produktov, etanola in ogljikovega dioksida, še druge snovi, kot so glicerol, višji alkoholi in razne kisline, ki vplivajo na okus alkoholne pijače (Šešek, 1978). Ko doseže koncentracija etanola v reakcijski zmesi 12%, se proces fermentacije zaustavi, saj višja koncentracija alkohola zavira delovanje encimov kvasovk (Solomons in Fryhle, 2008). Tako morajo žgane pijače z višjim odstotkom alkohola pripraviti z destilacijo fermentiranih zmesi ali pa z dodatkom čistega etanola. Starodavna ljudstva so že od nekdaj pripravljala vino na podlagi alkoholnega vrenja grozdnega soka, čeprav do prejšnjega stoletja ljudje sploh niso vedeli, kaj povzroča alkoholno vrenje in kako ta reakcija sploh poteka. Šele leta 1897 sta brata Eduard in Hans Buchner končno prišla do spoznanja, ki torej velja še danes, da sam biokemijski proces fermentacije omogoča skupek različnih encimov cimaza, ki ga proizvajajo celice gliv kvasovk. S kremenjakovim peskom sta namreč strla kvas in dobljeni sok skozi stiskalnico izolirala iz celic. Izkazalo se je, da je sok še vedno učinkovit in da vrenje ni vezano na življenjske procese živih celic, temveč da so vzrok neke druge snovi, ki so produkti teh
23 12 celic. Tako sta ovrgla teorijo znanega mikrobiologa Luisa Pasteurja, ki je bil mnenja, da lahko vrenje poteče le v prisotnosti živih celic kvasovk (Rixner in Wegner, 1977). Etanol pri zgorevanju sprošča veliko energije in ne povzroča saj, zato je vedno bolj v uporabi tudi kot nadomestno pogonsko gorivo gazohol, ki je zmes etanola in bencina (Boyer, 2005) Človek in alkohol Čeprav deluje alkohol na naše telo poživljajoče in nam sprva ponudi prijetne občutke kot sta sproščenost in brezskrbnost, pa negativno vpliva na vse organske sisteme. Med drugim zavira aktivnost višjih možganskih središč, tako da zmanjšuje delovanje sistema nevrotransmiterjev in živčnim celicam spremeni sposobnost sprejemanja in odzivanja na dražljaje (Solomons in Fryhle, 2008). Posledica je nihanje počutja in socialnega vedenja človeka, moteno je gibanje, zmanjšana je sposobnost koncentracije, podaljša se reakcijski čas, poveča se možnost pojava kognitivne disfunkcije in agresije (Giancola, 2004). Raziskave so pokazale, da zasvojenost z alkoholom vodi v depresijo in obratno. Daljše depresivno stanje lahko hitro privede do poseganja po alkoholu. Oba dejavnika sta torej tesno povezana, povzročata pa tudi tveganje za sekundarna psihična stanja, kar se posledično kaže v povečanem nasilnem vedenju in v vse številčnejših samomorih še posebej pri mlajši generaciji (Gilman in Abraham, 2001) Čebele kot izvrsten model za proučevanje vpliva alkohola Da bi čim bolje spoznali vpliv in delovanje etanola na posameznika ter njegovo vlogo v družbi, so začeli razvijati žuželčje modele alkoholizma. Najbolj primeren nevretenčarski živalski model za raziskave opijanja z alkoholom pa so prav čebele (Abramson in sod., 2000). Vzrok za to je predvsem njihov širok spekter vedenjskih vzorcev, sposobnost hitrega učenja in pomnjenja ter dobra orientacija (Božič in sod., 2006). V nasprotju z ostalimi socialnimi žuželkami so bile celo edine, ki so prenesle testiranja z relativno visokimi koncentracijami etanola (Abramson in sod., 2000). Poleg tega pa so poskusi s čebelami dodatno možni še zaradi dobrega poznavanja njihove fiziologije, vedenja ter genske zasnove. Ugotovili so, da ima etanol na čebele zelo podoben učinek kot na človeka (Abramson in sod., 2000, 2004). Vpliv alkohola na čebelji organizem je bil premo sorazmeren z njegovo koncentracijo. Raziskave so pokazale številne spremembe v socialnem vedenju pašnih čebel tako izven kot znotraj panja. Etanol dokazano zmanjša aktivnost zibajočega plesa čebel (angl. waggle dance), s katerim plesalke ostalim čebelam sporočajo smer, oddaljenost in kvaliteto paše, hkrati pa poveča aktivnost trepetavih plesov (angl. tremble dance), ki so tako del medsebojnega sporazumevanja kot spodbujanja k učinkovitosti paše čebelje družine (Thom, 2003; Božič in sod., 2006). Čebele so znane po tem, da slednji ples izvajajo, ko so
24 13 pod stresom, zato bi lahko tudi povečanje frekvence trepetavega plesa pripisali stiku s strupenim virom hrane (etanol), ki je v tem primeru deloval kot stresen dejavnik (Božič in sod., 2006). Zanimivo je tudi dejstvo, da so med trepetavim plesom čebel, ki ga predstavljajo vibracije telesa naprej in nazaj istočasno z njegovo rotacijo med hojo po satju, prvič opazili tudi izmenjavo hrane trofalakso (Seeley, 1992). Pitje alkohola povzroča upad števila izletavanj pašnih čebel iz panja, kar pomeni daljše zadrževanje znotraj panja, pri visokih koncentracijah alkohola kot je 10% raztopina etanola, pa je stanje čebel že dokaj kritično. Pojavi se nenavadno vedenje, pri katerem postane zelo oteženo tako letenje kot sama orientacija, definitivno je vidna zastrupitev z alkoholom (Božič in sod., 2006). Pri učenju čebel ob prisotnosti raztopine etanola različnih koncentracij so poskusi pokazali, da so koncentracije raztopin etanola, ki so bile višje od 5%, znatno zmanjšale klasično pogojevanje refleksa iztegovanja jezička (Abramson in sod., 2000). Nekateri ljudje postanejo pod vplivom alkohola veseli, drugi zaspani, veliko je pa takih, ki postanejo agresivni. Tako so začeli tudi pri čebelah proučevati njihovo občutljivost na hlape etanola v povezavi s prisotnostjo agresije. Sama agresija se pri čebelah kaže v primarnem napadalnem vedenju, kot so pikanje, straža ter preganjanje čebel stražark. Ko stražarke zaznajo grožnjo, začno izločati alarmne feromone in tako rekrutirajo ostale čebele v panju, da izletijo in napadejo sovražnika. Na sam postopek takega vedenja oz. odziva naj bi vplivali geni za napadalnost QTL (angl. quantitative trait loci) v povezavi s čutili in delovanjem živčnega sistema. Tako so vse te dejavnike proučevali v povezavi z alkoholom. Ammons A. D. in Hunt G. J. (2008) sta za poskuse uporabila dve skupini, in sicer napadalne ter mirnejše rase čebel, ter raziskovala ali je njihov odgovor na izpostavljenost hlapom 95% etanola napadalne narave. Rezultati so pokazali običajne znake občutljivosti na etanol, pri napadalnih čebelah je bilo moč opaziti zgodnejše in pogostejše iztegovanje jezička, mirnejše čebele pa so kasneje podlegle hlapom etanola. Izpostavljanje alkoholu pri nobeni rasi ni povzročilo iztegovanja žela, ki je glavni znak agresije Etanol kot del življenja čebel V naravi pridejo čebele pogosto v stik z etanolom pri srkanju sladkih sokov iz gnijočega sadja, v katerem zaradi prisotnosti kvasovk poteče alkoholno vrenje. Etanol pa ves čas nastaja tudi v panju. Med samim dozorevanjem medu v satnih celicah je med izpostavljen zraku in vlagi, zato pride hitro do razvoja gliv in raznih bakterij. Kvasovke, ki so glavni krivec za nastanek etanola, se lahko v panj prenesejo z nabrano medičino ali cvetnim prahom, preko tal skozi žrelo panja, lahko pa izvirajo iz čebelje mikroflore (Comi in sod., 1982; Crane, 1990). Te enocelične glive v procesu alkoholne fermentacije pretvarjajo sladkorje v medu v alkohol etanol in ogljikov dioksid.
25 14 Ker je med higroskopičen, lahko ob neprimernem shranjevanju zaradi razvoja kvasovk fermentira, kar privede do nastanka etanola, ogljikovega dioksida ter nekaterih kislin. Etanol pa je tudi, sicer v majhnih količinah, naravna sestavina medu (Duisberg, 1967). Huidobro in sod. (1994) so poskušali na podlagi encimske metode po Boehringer- Mannheimu določiti vsebnost etanola v medu. Pri tem so uporabili 33 vzorcev različnih medov s področja severozahodne Španije (Galicija), od tega je bilo 31 medov cvetličnega izvora, ostala 2 pa sta bila mešanici tako cvetličnega kot gozdnega medu. Rezultati so pokazali, da se je količina etanola gibala nekje med 13,5 in 50,1 mg/kg medu, v povprečju ga je bilo 27,8 mg/kg, s tem, da se pri tem vzorec z nekoliko odstopajočo vsebnostjo etanola (141,8 mg/kg) ni upošteval Ocetna kislina Etanojska kislina, kakor ji pravilno rečemo po nomenklaturi IUPAC, je brezbarvna hlapna tekočina ostrega vonja in spada med prve znane organske kisline, ki so jo odkrili pri kisanju vina (Kornhauser, 1998). Pri temperaturi pod 16,7 C začne tvoriti ledu podobne kristale in ji pravimo ledocet. Poznamo tri načine pridobivanja te karboksilne kisline, ocetnokislinsko vrenje pa je zagotovo najbolj znan proces pridobivanja, saj se je človek z njim srečal že v davni preteklosti. Pri tej vrsti fermentacije sodelujejo obligatorno aerobne ocetnokislinske bakterije, katerih encimi povzročajo oksidacijo etanola do ocetne kisline in vode, torej je kislina produkt mikrobnega metabolizma. Na tak način poteka tudi proizvodnja kisa, ki je 3 5% raztopina ocetne kisline in v živilstvu oz. prehrani zaradi svojega protimikrobnega delovanja služi kot naravni konzervans za konzerviranje živil, lahko pa se uporablja tudi kot aditiv ali kot začimba (Perpar, 1948). Poznamo več vrst kisa, ki se med seboj razlikujejo glede na surovino, metodo pridobivanja, končno vsebnost koncentracije ocetne kisline ter uporabo (Šešek, 1978). Kasneje je človek izkoriščal predelavo naravnih virov, kot je les, kjer je bil glavni namen pridobivanje oglja, in tako pri njegovi suhi destilaciji dobil ocetno kislino kot eno izmed razkrojkov v preostali vodni frakciji. Zadnji način pridobivanja je sintetično pridobivanje iz etina. Poleg kisa se ocetna kislina uporablja še pri sintezi zdravil in barvil ter v kemični in tekstilni industriji, prav tako pa se za različne namene uporabljajo tudi njene soli acetati oz. etanoati (Perpar, 1948) Ocetnokislinske bakterije Ocetnokislinske bakterije (OKB) pripadajo večinoma skupini gram negativnih bakterij in imajo elipsasto do paličasto oblikovane celice z aerobnim metabolizmom, kar pomeni, da je končni prejemnik elektronov kisik. V naravi so zelo razširjene, nahajajo se na različnih rastlinah, kot so trave, žito, sadje itd. Zaradi sposobnosti oksidacije različnih vrst sladkorjev in alkoholov do organskih kislin v procesu fermentacije so zelo pomembne v prehranski industriji (Sengun in Karabiyikli, 2011). Najpomembnejšo vlogo imajo
26 15 zagotovo pri proizvodnji kisa, kjer pri ocetnokislinskem vrenju z oksidacijo etanola tvorijo visoke koncentracije ocetne kisline. Oksidacijo povzročata encima alkohol-dehidrogenaza, ki oksidira etanol do acetaldehida ter aldehid-dehidrogenaza, ki povzroči nadaljnjo oksidacijo do etanojske kisline (Boyer, 2005). Sama uspešnost ocetnokislinskega vrenja je odvisna od različnih pogojev, kot so temperatura, koncentracija etanola, ph okolja ter dostopnost kisika. Tradicionalen proces fermentacije za proizvodnjo kisa tako vključuje tri med seboj neodvisne postopke, najprej hidrolizo oz. razpad sestavljenih ogljikovih hidratov do enostavnih sladkorjev z encimi plesni, nato sledi alkoholna fermentacija s kvasovkami ter zaključna faza ocetnokislinskega vrenja, ki ga povzročajo OKB (Wang in sod., 2013). OKB sodelujejo tudi pri proizvodnji celuloze ter sladkorja sorboze, ki nastane pri oksidaciji sorbitola in je poglaviten pri pridobivanju askorbinske kisline (vitamin C). Ti mikroorganizmi so pogosto prisotni na poškodovanem grozdju, zato moramo biti pazljivi pri predelavi mošta v vino in zagotoviti take pogoje, ki ne ustrezajo njihovemu razmnoževanju. Izjemna sposobnost oksidacije pri OKB ima namreč na nekatere produkte, kot je tudi vino, negativne učinke, saj nastajanje ocetne kisline povzroča kvarjenje oz. kisanje te alkoholne pijače (Sengun in Karabiyikli, 2011). V zadnjem času pa se vse več pozornosti posveča tudi simbiozi med OKB in žuželkami, ki so njihovi gostitelji. Čebele so bile prve, pri katerih so odkrili naseljevanje teh bakterij v prebavilih in drugih organih, njihovo prisotnost pa so kasneje potrdili tudi pri komarjih, mušicah in volnatih kaparjih. V čebelah se naseljujejo predvsem OKB rodu Gluconacetobacter, Acetobacter ter Gluconobacter, slednje predstavljajo glavno komponento čebelje mikroflore. Črevesje predstavlja OKB zaradi prisotnosti kisika in kislega ph-ja, ki dosega vrednosti od 4,8 do 7, optimalno okolje za uspešno razmnoževanje, hkrati pa dobijo potrebne sladkorje, saj jih čebele konstantno vnašajo s hrano. Prav tako pa imajo tudi čebele korist, kajti bakterije so vključene v njihov metabolizem, tako da jih oskrbujejo s potrebnimi hranili ali oksidirajo določene substrate ter jih z nižanjem vrednosti ph v črevesju varujejo pred škodljivimi mikroorganizmi, na vse te načine pa vzdržujejo celotno ravnovesje črevesne mikroflore (Crotti in sod., 2010; Anderson in sod., 2011) Ocetna kislina kot del življenja čebel in njena uporaba v čebelarstvu Ocetna kislina je zelo razširjena v naravi, lahko se nahaja v prosti obliki ali v obliki estrov. Tudi čebele prihajajo v stik s to organsko kislino. Zaradi etanola, ki ga proizvajajo glive kvasovke v panju, natančneje v predelu biofilma, prihaja v prisotnosti OKB v aerobnih razmerah do oksidacije tega alkohola in nastanka ocetne kisline. Prav tako nastaja pri oksidaciji fermentiranih sokov sadja.
27 16 Ta karboksilna kislina pa ima pomembno vlogo tudi v čebelarstvu. Virusi, bakterije in plesni lahko pri čebelah povzročijo številne nalezljive bolezni, ki lahko poleg umiranja čebeljih družin, naredijo tudi ogromno gospodarsko škodo čebelarjem. Ena izmed takih je nevarna kronična bolezen nosemavost ali nosemoza, ki jo povzroča zajedalec Nosema apis 1 (Zander, 1909), tako da se naseli v prebavila odraslih čebel in s tem krajša njihovo življenje. Sama okužba se prenaša skozi usta čebel, glavni izvor noseme pa so iztrebki že okuženih čebel. Znake bolezni je moč prepoznati tudi po tem, da se čebele iztrebljajo znotraj panja, kar za njih v normalnih razmerah ni značilno (Jenko-Rogelj in Strmole, 1998). Za preprečevanje bolezni čebel in uničevanje njihovih povzročiteljev je poleg stalne higiene v čebelnjaku pomembno razkuževanje rok, satja, panjev in ostale čebelarske opreme. Proti nosemavosti se izvaja kemijsko razkuževanje satja z ocetno kislino, ki uniči zelo odporne spore te praživali. Čebelarji satje zložijo v večji zaboj in ga dobro zaprejo za teden dni, pri tem je pomembno, da so sati med seboj nekoliko razmaknjeni. Na sate postavijo posodo z ocetno kislino, katere hlapi uhajajo navzdol, saj so težji od zraka. Na vsak liter prostornine je potrebno dati 2 ml 80% ocetne kisline, ki uniči spore v roku petih dni, enaka količina 100% ocetne kisline pa jih uniči že v treh dneh. Druga možna alternativa je uporaba formalina, vendar se ga čebelarji manj poslužujejo, saj je zelo strupen in je kljub njegovi strogi uporabi samo v praznem satju, možna zastrupitev še prisotnega cvetnega prahu in medu (Jenko-Rogelj in Strmole, 1998). Ocetna kislina zaradi svojega ostrega vonja draži čebele, zato se razredčena na dlaneh uporablja za njihovo odganjanje, ko je le-to potrebno pri določenih čebelarskih opravilih (Bokal in Gregori, 2008). Organske kisline se veliko uporabljajo proti raznim škodljivcem in boleznim čebel. Nevaren parazit, ki povzroča večjo škodo predvsem oslabelim čebeljim družinam, je mali panjski hrošč Aethina tumida. Ta eksotična vrsta škodljivca prihaja iz Južne Afrike, v kasnejših devetdesetih letih pa so ga našli tudi na številnih območjih Amerike ter Kanade, naselil se je tudi v Avstralijo, znani pa so tudi primerki iz Evrope, natančneje na Portugalskem (Gregori, 2004). Pred kratkim (11. sep. 2014) so poročali o pojavu malega panjskega hrošča v regiji Kalabrija na jugu Italije, ki naj bi tja najverjetneje zašel s kontejnerskimi prevozi. Italija že izvaja razne ukrepe, kot so uničevanje in razkuževanje panjev, kontrola premikov znotraj države ter monitoring, da bi preprečila nadaljnji razvoj in širjenje tega škodljivca (Sestanek, 2014). Da je stanje zelo resno, pričajo tudi zadnje novice (07. nov. 2014) o že prvem primeru Aethina tumide tudi na Siciliji v pokrajini 1 Danes je bolj prisoten mikrosporidijski zajedalec Nosema ceranae, čigar gostitelj je bila sprva čebela vrste Apis cerana v vzhodni Aziji (Fries in sod., 1996). Zaradi vse večje okužbe čebel Apis mellifera s sporami in velike umrljivosti čebeljih družin na območju Španije so s pomočjo posebnih molekularnih tehnik (PCR) preučevali sekvence gena rrnk v vzorcih ( ) in določili vrsto mikrosporidija ter razlike med vrstama N. apis in N. ceranae (Higes in sod., 2006). Potrdili so prisotnost novega zajedalca, prav tako pa so že leta 1998 pri vzorcih z juga Finske zabeleželi prvi primer Noseme ceranae, ta naj bi tja zašla zaradi uvoza številnih čebeljih matic iz južnih predelov Evrope (Paxton in sod., 2007).
28 17 Siracusa (Aethina..., 2014). Na celotno dogajanje se je z ozaveščanjem odzvala tudi ČZS, saj obstaja verjetnost pojava panjskega hrošča tudi pri nas. Samo širjenje tega hrošča je posledica trgovanja s čebeljimi družinami in maticami, zato so nekatere države prepovedale vnos takšnih okuženih čebel. Mali panjski hrošč se prehranjuje z zalego, pelodom in medom, hkrati pa povzroča tudi njegovo fermentacijo. Tako se začne med kvariti in postane neužiten tako za čebele kot za človeka. Afriške čebele so v nasprotju z evropskimi sposobne boljše obrambe, njihovo vedenje je prilagojeno sobivanju s tem vsiljivcem, zato je propadanje čebeljih družin pri evropskih vrstah pogostejše (Gregori, 2004). Schäfer in sod. (2009) so preučevali vpliv organskih kislin na malega panjskega hrošča ter na same kvasovke vrste Kodamaea ohmeri, ki se pojavijo zaradi vrenja medu. Izkazalo se je, da organske kisline zavirajo rast kvasovk, tukaj je bila poleg 60% mravljične kisline najuspešnejša 70% ocetna kislina. Prav tako so hlapi ocetne kisline zvišali umrljivost odraslih panjskih hroščev. Ocetna kislina deluje kot uspešno kemično sredstvo tudi proti vsem razvojnim oblikam velike voščene vešče lat. Galleria mellonella, ki je škodljivec, odvisen od čebeljih pridelkov (Jenko-Rogelj in Strmole, 1998) Mlečna kislina Iz strukturne formule mlečne kisline lahko razberemo, da gre za 2-hidroksipropanojsko kislino. Na videz je to gosta, brezbarvna tekočina kislega vonja in spada med šibke organske kisline, zaradi nesimetričnega C-atoma pa se predvsem pri kemijski sintezi pojavlja v racemični mešanici dveh izomer L(+) in D(-) (Kubicek in Karaffa, 2006). Dobro se meša z vodo ter etanolom in je higroskopična snov, saj nase veže vlago iz zraka (Perpar, 1948). Mlečno kislino je prvi izoliral iz kislega mleka švedski kemik Carl Wilhelm Scheele leta Do leta 1857 so poznali mlečno kislino le kot sestavino mleka, dokler ni Louis Pasteur odkril, da je ta kislina fermentacijski metabolit določenih mikroorganizmov (Ghaffar in sod., 2014). Mlečna kislina namreč nastaja iz glukoze po anaerobni metabolni poti v celicah številnih organizmov. Zaradi odsotnosti kisika gre torej za fermentacijski proces, ki sledi običajni glikolizi in kjer je končni akceptor elektronov snov s tremi ogljikovimi atomi mlečna kislina ali laktat. Pretvorbo piruvata, produkta glikolize, v laktat in obratno katalizira encim laktat-dehidrogenaza (Boyer, 2005). Do mlečnokislinske fermentacije in posledično nastanka mlečne kisline prihaja tudi v živalskih in naših skeletnih mišicah med intenzivnim delom. Za normalno delo in energijo porabljajo mišice kisik, ki je pomemben za potek aerobne metabolne poti piruvata. Med naporom porabijo mišične celice za celično dihanje več kisika, kot ga dobijo, zato se začne piruvat reducirati do mlečne kisline. Kopičenje laktata in hkrati povečana koncentracija H + povzroča znižanje vrednosti ph v mišičnih celicah, kar lahko tudi sami občutimo kot krče in bolečine v utrujeni mišici (Boyer, 2005). Pri mirovanju se del mlečne kisline pretvori nazaj
29 18 v piruvat za sintezo glukoze oz. glikogena, ostali del pa v srcu in jetrih oksidira v CO 2 in vodo (Perpar, 1948). Mlečno kislino večinoma pridobivajo iz krompirjevega in žitnega škroba ter iz sladkorne melase, glavni substrati za njeno proizvodnjo so tako sladkorne in škrobne surovine (Kornhauser, 1998). V Ameriki se je pojavila prva proizvodnja mlečne kisline na podlagi fermentacije že leta 1881 in od takrat se obsežno uporablja poleg v živilski tudi v tekstilni in kozmetični industriji, v farmaciji, kjer se še posebej uporabljajo njene soli t. i. laktati, ter v kemični industriji (Ghaffar in sod., 2014). Pomembno mesto zaseda tudi v industriji plastike, saj s polimerizacijo mlečne kisline pridobivajo polimlečno kislino ali polilaktid (PLA), za katerega se kaže izredno zanimanje na trgu, kajti gre za biorazgradljivo plastiko, narejeno na osnovi obnovljivega vira, hkrati pa ta biopolimer predstavlja alternativo plastiki, predelani iz surove nafte (Ghaffar in sod., 2014) Mlečnokislinske bakterije Mlečnokislinske gram pozitivne, nesporogene in nepatogene bakterije (MKB) izkoriščajo za svojo rast in delovanje celic mlečnokislinsko fermentacijo, tako da z encimi fermentirajo mlečni sladkor v mleku in mlečnih izdelkih do mlečne kisline. Mlečni sladkor ali laktoza je disaharid, sestavljen iz glukoze, vezane na molekulo galaktoze. Bakterije uvrščamo v dve kategoriji, in sicer so lahko homofermentativne ali heterofermentativne narave. Slednje poleg mlečne kisline proizvajajo še nekatere druge stranske produkte (Ghaffar in sod., 2014). Nastanek mlečne kisline pri fermentaciji mleka zniža vrednost ph, kar povzroči koagulacijo mlečne beljakovine kazein in kisanje mleka. Kulture različnih bakterij mlečnokislinskega vrenja, še posebej bakterije rodu Lactobacillus, ki štejejo celo preko 60 vrst, tako uporabljamo za proizvodnjo nekaterih živil, kot so jogurt, kefir, sir, kisla smetana, kisla repa, kislo zelje (Kubicek in Karaffa, 2006). Vinarji in pivovarji uporabljajo MKB za uravnavanje ph-ja, zaradi svojega prijetnega kiselkastega okusa pa mlečna kislina služi tudi kot aditiv pijačam in nekaterim živilom Mlečna kislina kot naravni konzervans Mlečna kislina deluje baktericidno, saj onemogoči razvoj in delovanje mikroorganizmov in je zato odličen naravni konzervans (Boyer, 2005). Z mlečnokislinskim vrenjem oz. kisanjem tako konzerviramo živila, prisotnost mlečne kisline v živilu poleg same obstojnosti živila izboljša tudi njegovo hranilno vrednost, okus ter vpliva na spremembo teksture. Ta organska kislina uničuje tudi škodljive mikroorganizme v prebavnem traktu in tako vzdržuje delovanje črevesne flore, pripomore k razgradnji beljakovin ter pospešuje izločanje prebavnih sokov, zato so tudi laktobacili največkrat uporabljeni probiotiki (Šešek, 1978). Prav tako so MKB prisotne v prebavnem traktu čebel in s proizvajanjem mlečne kisline uničujejo patogene organizme in vzdržujejo zdravo črevesno mikrobioto (Anderson in sod., 2011). Poleg tega, da se mlečna kislina uporablja za konzerviranje
30 19 hrane, jo uporabljajo tudi v kmetijstvu, in sicer za silažo, ki predstavlja postopek konzerviranja oz. kisanja krme za živino. Kmetje v silose nasujejo svežo krmo, ki jo enakomerno razporedijo, močno pretlačijo in posujejo s prstjo ali s posebnimi pokrovi ter nato silose dobro zatesnijo. V prsti se nahajajo MKB, ki se prehranjujejo s sladkorji iz sveže krme in tako povzročajo mlečnokislinsko vrenje ter nastajanje mlečne kisline. Nastala mlečna kislina je vzrok za padec vrednosti ph in odličen naravni konzervans, ki zaradi svojega antibakterijskega delovanja uničuje škodljive mikroorganizme in s tem preprečuje gnitje krme (Perpar, 1948). Za živino pomeni taka krma hrano z večjo hranilno vrednostjo in boljšim izkoristkom, saj zvišuje prebavljivost Fermentacija cvetnega prahu ter mlečna kislina kot del življenja čebel Medonosne čebele izletavajo na pašo z namenom, da bi nabrale medičino in cvetni prah, ki jim predstavljata glavni vir hrane. Medičina in mana sta bogat vir energije, saj vsebujeta velike količine ogljikovih hidratov, mana celo več kot 90% suhe snovi (Božnar in Senegačnik, 1998). S cvetnim prahom pa dobijo čebele potrebne rudninske in beljakovinske snovi za splošno delovanje svojega organizma, potreba po njegovem nabiranju je sorazmerna z obsegom zalege oz. je odvisna od razvojnega stadija celotne čebelje družine. Ko se čebela vrne v panj, nabrani cvetni prah v obliki obnožine postrga z zadnjih nog, pri tem si s sprednjimi nogami očisti še tipalnice, glavo in ustne predele, druge čebele zrnca peloda navlažijo s slino ter ga obogatijo z izločki svojih žlez. Nato ga položijo v satno celico, kamor ga natlačijo v več slojih ter prekrijejo s tanko plastjo medu (Anderson in sod., 2011). S takšnim postopkom shranjevanja pripomorejo k zaščiti peloda pred vremenskimi vplivi, ki bi povzročili njegovo kvarjenje. Zaradi medu vsebuje konzerviran cvetni prah še več sladkorja kot svež cvetni prah (Božnar, 2011). Tako začne tak shranjen pelod ob pomanjkanju kisika in visoki temperaturi v panju (33 C) zaradi prisotnosti mikroorganizmov, ki izvirajo iz nabranega peloda in čebelje črevesne mikroflore, fermentirati. Samo fermentacijo povzročajo predvsem MKB, dogajanje je podobno kot pri silaži živinske hrane, nastaja mlečna kislina. Fermentirani obnožini v satnih celicah, ki spremeni svojo kemično sestavo in hranilno vrednost, čebelarji zaradi načina pridobivanja pravijo izkopanec (Bokal in Gregori, 2008). V angleški literaturi zasledimo izraz»bee bread«(čebelji kruhek). Izkopanec je v nasprotju z osmukancem kvalitetnejši, saj vsebuje poleg veliko mlečne kisline tudi več vitaminov, hkrati pa manj vode (Rihar, 1998). Tako si čebele ustvarijo zaloge cvetnega prahu za čase, ko le-tega v naravi prične primanjkovati. Enako izkoriščajo MKB sladkorje v medu in tako v času njegovega zorenja v procesu mlečnokislinskega vrenja tvorijo metabolite, med katerimi je glaven produkt mlečna kislina. Mlečnokislinske bakterije izvirajo tudi z različnih cvetov, na katerih čebele nabirajo medičino, večinoma pa iz mednega želodčka čebel, kjer dominirata rodova Lactobacillus in Bifidobacterium, ki sta del bakterijske flore. Raziskave so pokazale, da
31 20 mlečnokislinske bakterije iz rodu Bifidobacterium proizvajajo poleg mlečne še ocetno kislino in so zato heterofermentativne narave (Olofsson in Vásquez, 2008). Medni želodček ali medna golša čebele je razširjen del požiralnika, ki služi začasnemu shranjevanju medičine. Konča se s podaljškom srednjega črevesja z zaklopnico (proventriculus), ki zagotavlja, da medičina ni nikoli kontaminirana z vsebino srednjega črevesja. Hkrati pa se tu medičina prepoji z različnimi encimi iz žlez čebel. Čebele živijo z mlečnokislinskimi bakterijami v simbiozi, saj imajo oboji korist. Medni želodček zaradi medičine, bogate s sladkorji in ostalimi hranili ter primerne temperature, predstavlja MKB optimalno nišo (Olofsson in Vásquez, 2008). Po drugi strani pa MKB proizvajajo veliko antibakterijskih snovi, kot so organske kisline, vodikov peroksid, diacetil, benzoat ter bakteriocini, ki ščitijo čebele pred patogeni ter krepijo njihov imunski sistem, poleg tega pa so te snovi koristne tako za ljudi kot za ostale živali (de Vuyst in Vandamme, 1994). Mlečna kislina je tako tudi sestavni del svežega medu, povprečno jo je 200 mg/kg medu (Meglič in Auguštin, 2007) Mlečna kislina v čebelarstvu Invertiranje medičine med zorenjem medu s pomočjo encima invertaza ali saharaza, ki ga izločajo krmilne žleze čebel delavk, povzroči razgradnjo saharoze v enostavna sladkorja glukoze in fruktoze. Z ugotavljanjem koncentracije saharoze v medu lahko predvidimo njegovo pristnost, kajti čebele trsnega sladkorja, s katerim jih velikokrat hranijo čebelarji, ne morejo invertirati v celoti (Plut, 2014). Invertni sladkor pa je možno dobiti na drug način, in sicer z dodajanjem kisline v segreto sladkorno raztopino. Leta 1968 se je bavarski čebelarski zavod lotil takšne izdelave invertnega sladkorja. Uporabili so več kislin, ki so jih testirali na ujetih čebelah ter na umetnih rojih. Opazovali so vpliv te snovi na dolžino življenja, razvoj čebel ter njihovo graditev satja. Najboljše rezultate je pokazal invertni sladkor, dobljen s pomočjo mlečne kisline, ki so ga dobili tako, da so kilogramu sladkorja dodali pol mililitra te kisline (Mayer, 1980). Dodajanje takšnega industrijsko invertiranega sladkorja v med, kjer je bila za invertiranje uporabljena določena kislina, poveča kislost medu, dodatek neinvertirane saharoze pa vpliva obratno, zato je takšen med manj kisel. Vse to kaže na njegovo ponarejanje, zato lahko tudi glede na kislost medu sklepamo o njegovi pristnosti (Božnar in Senegačnik, 1998). Mlečna kislina se uporablja za zatiranje varoje. Varroa destructor je pršica in je zunanji parazit čebel, ki povzroča kronično bolezen čebel varozo in v večjem številu uniči celotno čebeljo družino. Življenjski ciklus varoje poteka znotraj panja, v pokritih celicah zalege čebel delavk ali trotov. Zaradi sestave trotovske hemolimfe samice varoj večkrat izberejo trotovsko zalego, v trotovini pa naj bi bila tudi nekoliko nižja temperatura, ki jim bolj ustreza. Preživijo le mati varoja in njene oplojene hčere. Dokler ne preidejo v celice z zalego, se zadržujejo na čebelah krmilkah. Varoja se hrani s hemolimfo čebel, na tak način uničuje čebelje tkivo in njene telesne tekočine, saj vanje sprošča razne toksine, povzroča
32 21 tudi nepravilno rast in mehanske poškodbe čebele (Meglič in Auguštin, 2007). Kljub temu, da varoj v čebelji družini ni mogoče popolnoma uničiti, pa je pomembno, da čebelarji preprečujejo pretirano namnožitev števila varoj, ki bi začela čebele ogrožati. Včasih so čebelarji za zatiranje varoj uporabljali različna kemična sredstva, kot so npr. akaricidi, ki pa so se kmalu izkazala za neučinkovita in neprimerna, saj se je pojavila rezistenca s strani varoj, porabniki medu pa so začeli dvomiti o pristnosti medu, kajti sredstva so tako v njem kot v vosku puščala nedovoljene ostanke. Kmalu so prišla v uporabo nekatera alternativna sredstva, in sicer organske kisline in eterična olja, ki uničijo varoje, možnost rezistence z njihovo uporabo je majhna, hkrati pa v medu ne puščajo nobenih ostankov ali pa so ti minimalni (Imdorf in sod., 1996). Razlog za to je hidrofilna narava nearomatskih organskih kislin, kar preprečuje akumulacijo v vosku, zelo nizke koncentracije v medu pa niso toksične (Imdorf in sod., 1996). Poleg mravljične in oksalne kisline je v uporabi tudi mlečna kislina. Za ta namen čebelarji pršijo sate s 15 % vodno raztopino mlečne kisline, ta organska kislina pa ima pred ostalimi kislinami tudi nekaj več prednosti, njena učinkovitost naj bi bila podobna uporabi kumafosa (Kraus in Berg, 1994; Meglič in Auguštin, 2007).
33 UČENJE ČEBEL Volumen čebeljih možganov meri približno 1 mm 3, v njem se prepleta približno nevronov. Kljub tako majhni kapaciteti možganov, če jih primerjamo z možgani vretenčarjev, so le-ti sposobni izvesti številne vedenjske vzorce, kar čebelam omogoča prilagajanje v spremenljivem okolju ter posledično evolucijsko uspešnost. Sposobne so učenja novih ter izboljšave vedenj (Menzel in Giurfa, 2001). Karl von Frisch (1962) je izjavil, da tako majhni možgani čebel niso narejeni za razmišljanje, kajti vsa dejanja čebel so vodena preko njihovega nagona (Giurfa, 2007). Čebele imajo izjemno razvite čutilne in gibalne sposobnosti. Vidijo svet v barvah, zmožne so ločiti različne vzorce in oblike, vzorce polarizirane svetlobe na nebu izkoriščajo za svojo orientacijo, njihov vohalni čut jim omogoča zaznavanje različnih vonjav, prav tako je izvrstna njihova mehanosenzorična zaznava, hkrati pa si lahko različne vzorce neverjetno dobro zapomnijo (Menzel in Giurfa, 2001) Asociativno učenje Pašne čebele izletavajo iz panja in iščejo hrano na medovitih rastlinah, ki čebele vabijo s svojimi vonjavami, različnimi barvami in količino medičine. Le v primeru, da čebela najde hrano v cvetju, postane ta rastlina zanjo pogojena kot signal za nabiranje hrane, zato si tudi zapomni vonj, barvo in celo obliko tega cvetja (von Frisch, 1967). Vonj in barvo cvetov čebele zaznajo že na velikih razdaljah, samo obliko pa šele pred pristankom. V primeru, da neka rastlina preneha z medenjem, začnejo čebele iskati druge rastline z izločanjem medičine. Smer in oddaljenost paše sporočijo ostalim čebelam v panju s pomočjo plesnega sporazumevanja (von Frisch, 1967). Dobra nagrada, ki je v tem primeru medičina (hrana), je potrebna izkušnja, da se čebela nekaj nauči in določen cvet ohrani v spominu. Glavni organ, ki čebelam omogoča zaznavanje vonja, okusa, dotika, strukture neke snovi, vlažnosti in koncentracije CO 2 v panju ter na krajših razdaljah tudi zaznavanje zvoka, so tipalnice, ki nosijo več tisoč čutnic različnih vrst (Gregorc, 1998). Zgoraj opisana oblika učenja je asociativno učenje, kjer poteka asociacija oz. povezava med dvema raznovrstnima dražljajema, in sicer med pogojnim dražljajem CS (angl. conditional stimulus) in nepogojnim dražljajem US (angl. unconditional stimulus). Prav zaradi dejstva, da so medonosne čebele sposobne hitrega učenja in dobrega pomnjenja, veljajo kot izvrsten nevretenčarski model za učenje in spomin na vedenjski, celični in molekularni ravni. Da bi bolje raziskali te njihove sposobnosti, so razvili protokole učenja na podlagi različnih vrst dražljajev (Giurfa, 2007). Primer je asociativno mehanosenzorično pogojevanje refleksa iztegovanja jezička. Tukaj se vpete čebele učijo osnovne povezave med stimulacijo tipalnice s paličico (predmetom), ki predstavlja pogojni dražljaj ter ponujeno nagrado sladkorne raztopine, ki je nepogojni dražljaj. Pri tem se morajo naučiti samodejnega iztegovanja jezička le ob dotiku tipalnice oz. prisotnosti
34 23 pogojnega dražljaja (A+). Stegovanje jezička ali PER refleks (angl. proboscis extension reflex) je naravno pogojeni odziv na sladkorno raztopino primerne koncentracije. Zmanjšana koncentracija raztopine sladkorja naj bi poslabšala motivacijo za učenje. Torej, če s sladkorno raztopino dražimo tipalnico, ki je glavni kemosenzorični organ čebel, pride posledično do PER odziva. Čebele so bile tudi del diferencialnega učenja (A+, B-), tako da so raziskovalci izmenično dražili obe tipalnici, vendar pri drugem dražljaju čebela ni dobila nagrade. Ugotovili so, da je takšno asociativno učenje tudi uspešno, saj so čebele iztegnile jeziček le ob dotiku tiste tipalnice, pri kateri so bile kasneje nagrajene. V opisanem primeru gre za utrjevanje samo enega določenega dražljaja oz. za razlikovanje glavnega pogojnega dražljaja od ostalih podobnih. Odgovor na dražljaj je v vseh primerih odvisen le od mehanskega draženja tipalnice in ni v povezavi z vonjalnimi, vizualnimi in kontekstualnimi zaznavami. Asociativni spomin je ostal dejaven tudi 24 ur po pogojevanju (Giurfa in Malun, 2004). Če pri učenju preskočimo nepogojni dražljaj, pride sčasoma do ekstinkcije ali slabenja pogojnega odziva in končno do njegovega prenehanja. Poleg asociativnega mehanosenzoričnega pogojevanja so pri vpetih čebelah proučevali tudi vonjalno oz. olfaktorno pogojevanje s PER odzivom, ki je prikazalo podobne rezultate. Določen vonj je bil pogojni dražljaj, sladkorna raztopina pa nepogojni. Tako so začele čebele ob določenem vonju iztegovati jeziček. Ob postavljeni pregradi med tipalnicama je bilo tudi tukaj možno vonjalno pogojevanje le z določeno tipalnico. Izvedljive pa so tudi ostale, kompleksnejše oblike asociativnega učenja, kot je npr. negativno vzorčenje, kjer morajo čebele ločiti dva posamezna nagrajena dražljaja (A+, B+) od sestavljenega dražljaja, ki ni nagrajen (AB-). To je za čebele kar velik izziv, saj so posamezni elementi A in B številčno enako nagrajeni kot tudi nenagrajeni (Giurfa, 2007). Kontekstualno učenje predstavlja obratno nagrajevanje pri vsaki tipalnici, torej pri prvi sta vonjavi A+ in B-, pri drugi tipalnici pa A- ter B+. Poleg teh dveh protokolov učenja, torej mehanosenzoričnega in olfaktornega pogojevanja, sta v uporabi tudi pogojevanje z vidnimi dražljaji, kot so barve, oblike in vzorci pri prosto letečih čebelah, ter olfaktorno pogojevanje refleksa iztegovanja žela pri vpetih čebelah z električnim šokom kot nepogojnim dražljajem (Giurfa, 2007). Vzrok za podobnost med vonjalnim in mehanosenzoričnim pogojevanjem tiči v poteku obeh živčnih poti. Kemoreceptorji za voh se nahajajo vzdolž tipalnice, medtem ko so mehanoreceptorji razvrščeni le na določenih mestih tipalnice. Vohalni receptorji pošiljajo sporočila preko tipalnega živca do tipalničnega režnja v možganih, kjer se nato prenesejo do višjih možganskih središč, med katerimi so nedvomno pomembna gobasta telesa, ki omogočajo učenje sestavljenih zaznav okolja, kot je pašna aktivnost čebel (Gregorc, 1998). Gobasta telesa lahko sprejemajo tako vonjalne kot tudi vidne in mehanosenzorične dražljaje, prav tako so tudi njihovi izhajajoči nevroni večnamenski (Menzel in Giurfa, 2001). Mehanoreceptorji pa pošiljajo dražljaje v zadnji reženj možganov, ki je v povezavi
35 24 z motoričnimi središči. Med tipalničnim režnjem in dorzalnim režnjem poteka povezava preko internevronov, zato lahko v nekaterih primerih živčne celice odgovorijo tako na mehanski kot na vonjalni dražljaj (Giurfa in Malun, 2004). Asociativno učenje na podlagi dveh povezanih dražljajev je komponenta klasičnega Pavlovega pogojevanja (1927), ki je dokazal, da je povezovanje dražljajev ena izmed bistvenih kognitivnih sposobnosti organizma. Delal je raziskave pri psih, predvsem ga je zanimal proces slinjenja, ki se pojavi že ob samem pogledu na hrano. Ob zvoku so psi dobili hrano, kasneje so se naučili, da so se ob tem pogojnem dražljaju začeli sliniti. Druga oblika asociativnega učenja je operantno pogojevanje, ki ga je raziskoval B. F. Skinner (1938) pri golobih in podganah. Da je lačna žival v Skinnerjevem zaboju prišla do hrane, je morala pritisniti tipko, kasneje pa je začel uvajati še ostale dražljaje. Če so posledice določenega odziva pri tem učenju ugodne, se takšno vedenje utrdi. Samo vedenje organizma je tukaj v nasprotju s klasičnim pogojevanjem hoteno in ni refleksno, od njega je odvisna tudi nagrada (Kompare in sod., 2001). Čebele so dragocen model za boljše razumevanje vpliva alkohola na živčni sistem. Dosedanje raziskave so bile osredotočene predvsem na vedenje in motorične sposobnosti čebel pod njegovim vplivom. Mustard in sod. (2008) pa so na podlagi enostavnega in diferencialnega pogojevanja raziskali vpliv akutne doze etanola (2,5%, 5%, 10% in 25%) na zmožnost učenja oz. razlikovanja vonjav pri medonosni čebeli. Predvsem višje koncentracije etanola ( 5%) so vplivale na vonjalne procese, saj so poslabšale dojemanje, pomnjenje in razlikovanje posameznih vonjav, prav tako so začele čebele izgubljati motivacijo za pogojni dražljaj. Tako je zaužitje alkohola pred pogojevanjem zmanjšalo stopnjo asociativnega učenja. Vzrok za slabše učenje ni bil v povezavi z vplivom alkohola na okušalno občutljivost ali gibalne sposobnosti iztegovanja jezička. Če so dali čebelam piti alkohol po pogojevanju, to ni vplivalo na samo utrjevanje in ponoven priklic učenja po 24. urah. Le čebele, ki so spile visoke koncentracije etanolne raztopine, se niso mogle spomniti dejanj, ki so se jih naučile med olfaktornim pogojevanjem. Vse te poskuse je bilo možno izvesti, ker so čebele sposobne prefinjenih učnih nalog, hkrati pa so poleg njihovega učenja in pomnjenja dobro preučevani tudi njihovi možgani, celoten genom ter molekularni mehanizmi (Mustard in sod., 2008).
36 Neasociativne oblike učenja Med najpreprostejše oblike učenja, ki niso asociativne narave, spadata senzitizacija in habituacija. Če čebelje tipalnice preveč časa dražimo, lahko zaradi stalno ponavljajočega intenzivnega nepogojnega dražljaja pride do senzitizacije oz. preobčutljivosti, kar se kaže v vse bolj hitrejšem in močnejšem odzivu na dražljaje. Zato ne moremo reči, da je takojšnji pogojni odziv posledica asociativnega učenja, o tem se lahko prepričamo šele po nekaj minutah (Menzel, 1999). Pri habituaciji se zgodi ravno obratno kot pri senzitizaciji, saj se tu organizem zaradi ponavljajočega dražljaja začne vedno slabše odzivati, dokler se celotno odzivanje ne zaustavi. Habituacija mogoče nekoliko pripomore k hitrejšemu učenju, saj se na nepogojni dražljaj organizem slabše odziva. Ponoven PER odziv lahko izzovemo s stimuliranjem nasprotne tipalnice (Braun in Bicker, 1992).
37 26 3 MATERIAL IN METODE Laboratorijske poskuse in celotno obdelavo podatkov smo opravili v Laboratoriju za nevroetologijo Oddelka za biologijo Biotehniške fakultete, praktični poskusi s čebelami (Apis mellifera carnica Pollmann, 1879) pa so bili izvedeni v panju v bližini Oddelka za biologijo Biotehniške fakultete. Raziskovalni del diplomskega dela je potekal v času od 14. maja do 19. julija Našo raziskavo smo razdelili na dva dela. V prvem delu smo najprej preverili, katere koncentracije raztopin ocetne in mlečne kisline čebele sploh še pijejo ter ali so zmožne zaznati in razlikovati nizke koncentracije raztopin etanola, ocetne in mlečne kisline, drugi del raziskave pa je bil namenjen opazovanju vpliva določenih koncentracij raztopin teh snovi pri predelavi hrane/medu v panju. 3.1 ZAZNAVANJE NIZKIH KONCENTRACIJ RAZTOPIN ETANOLA, OCETNE IN MLEČNE KISLINE Opis poskusa S tem poskusom smo želeli ugotoviti, ali so čebele zmožne zaznati nizke koncentracije raztopin etanola, ocetne in mlečne kisline oz. ali lahko testirane raztopine uporabijo za učenje razlikovanja hrane. Izvedli smo asociativno učenje čebel (N=16), in sicer sprva mehanosenzorično, kasneje pa še olfaktorno pogojevanje s PER odzivom (proboscis extension reflex). Preden smo začeli z učenjem, pa smo morali preveriti oz. določiti koncentracije raztopin ocetne in mlečne kisline, ki jih čebele zaužijejo. V nasprotju s tem pa nam za etanol tega ni bilo potrebno storiti, saj smo zanj uporabili navedbe prejšnjih raziskav. Narejenih je namreč že veliko testiranj z različnimi koncentracijami etanola, s katerimi so dokazali, da čebele raje zaužijejo sladkorno raztopino z manjšim odstotkom alkohola. V primeru, ko so čebelam poleg 5% etanola v sladkorni raztopini ponudili samo sladkorno raztopino, je nekaj čebel pilo le slednje. Opazili so tudi razliko v stegovanju jezička oz. v času pitja raztopine, ki je upadal z večanjem koncentracije etanola v raztopini. Tudi pri poskusu, kjer so privajali čebele na 5% etanola v sladkorni raztopini, se je na postavljeno tarčo vračalo vse manj čebel. 1% etanola v sladkorni raztopini pa ni povzročil nobenih odstopanj v primerjavi s samo sladkorno raztopino brez dodanega etanola (Abramson in sod., 2004). Pri Pavlovem klasičnem pogojevanju so imele težave samo čebele, ki so spile 5% in več kot 5% etanolno raztopino (Abramson in sod., 2000). Glede na vse te rezultate raziskav smo tudi mi pri našem poskusu učenja čebel uporabili nižjo koncentracijo raztopine etanola, in sicer le 2% raztopino tega alkohola.
38 Priprava poskusa Pitje raztopin v panju Privajanje čebel na umetno krmišče oz. sladkorno raztopino Prvi dan našega eksperimentalnega dela smo poskušali čebele privaditi na umetno krmišče, ki jim je predstavljalo pašo. Približno 8 m od panja smo na mizico postavili dva navzdol obrnjena 200 ml kozarca s pokrovoma, v katera smo približno do polovice vlili 50% sladkorno raztopino. Vmes med kozarcem in pokrovom smo postavili majhno paličico, ki je omogočila vstop zraka v kozarec ter počasno iztekanje sladkorne raztopine v spodnji pokrovček (vakuumski napajalnik). Filtrirne papirčke smo pomočili v sladkorno raztopino ter odšli do panjskega žrela po čebele. Na ta način smo prenesli nekaj čebel do umetnega krmišča. Čebele so pile sladkorno raztopino ter se vračale v panj, pri tem je začelo na pašo prihajati vse več rekrutiranih čebel. Vsakih 10 min smo zabeležili število čebel na krmišču. Da bi čebele še bolj pritegnili, smo po določenem času sladkorni raztopini dodali še kapljico eteričnega olja sivke, kar se je izkazalo kot pozitiven dražljaj. Ko je zanimanje čebel za našo pašo, predvsem zaradi vremenskih razmer, dokončno upadlo, smo začeli čebele hraniti neposredno v nakladalnem panju, tako da smo na mrežo pritrdili 4 injekcijske brizge s po 10 ml sladkorne raztopine ter vsakih 30 min odmerili količino popite raztopine Priprava raztopin Vse raztopine, potrebne za poskuse, smo pripravljali v laboratoriju sproti na dan poskusa in jih hranili v hladilniku največ 3 dni. Pripravili smo različne koncentracije sladkornih raztopin ocetne in mlečne kisline, saj čebele pijejo raje sladkorne kot vodne raztopine, kar so dokazali tudi Abramson in sod. (2000) pri pitju etanolne raztopine. Raztopine etanola ni bilo potrebno pripraviti, saj smo glede na podatke prav te raziskave vedeli, kolikšne koncentracije te raztopine so primerne za učenje čebel. Najprej smo v erlenmajerici pripravili čisto sladkorno raztopino, tako da smo 480 g (1,5 mola) saharoze raztopili v 1 litru destilirane vode ter vse skupaj pustili približno 15 min na magnetnem mešalu, dokler nismo dobili dobro premešane homogene zmesi. Sladkorne raztopine ocetne in mlečne kisline smo pripravili v 50 ml bučkah. Pripravili smo 2% in 5% raztopino ocetne kisline ter 2% in 5% raztopino mlečne kisline. Da bi bile vse raztopine enako razredčene, smo k vsaki dodali toliko destilirane vode, kolikor je bila razlika med posamezno raztopino in tisto, ki smo jo dodali v tem primeru največ. Nato smo še do oznake 50 ml dolili sladkorno raztopino. Kontrola je vsebovala toliko destilirane vode, kot je bil najvišji volumen kisline (2,75 ml), preostali del je bila sladkorna raztopina. Čebele
39 28 smo s kontrolo in ostalimi pripravljenimi raztopinami hranili hkrati v dveh ponovitvah, zato smo vsako raztopino določene koncentracije vlili v 2 lončka po 25 ml in lončke z raztopinami označili Priprava krmilnika za pitje raztopin ter tehtanje Krmilnike za čebele smo pripravili tako, da smo vzeli 10 ml lončke, jih navzdol obrnjene postavili na filtrirni papir, zarisali obseg kroga ter za podlago uporabili zgornji del petrijevk. Za naš poskus smo potrebovali 10 krmilnikov (2 x kontrola, 2 x 2% ocetna kislina, 2 x 5% ocetna kislina, 2 x 2% mlečna kislina, 2 x 5% mlečna kislina). Vse posamezne dele smo sprva stehtali, torej vsak lonček posebej, vsak filtrirni papir ter zgornji del petrijevke. Nato smo v vsak lonček odmerili 10 ml raztopine določene koncentracije ter zaradi različne gostote raztopin in kasnejše lažje obdelave podatkov tudi to stehtali. Na lonček, napolnjen z raztopino, smo položili filtrirni papir in na to še zgornji del petrijevke ter vse skupaj hitro obrnili Učenje čebel s PER odzivom Za učenje čebel smo uporabili koncentracije raztopin, ki so jih čebele pile v prvem delu poskusa. Testiranja v zvezi z učenjem čebel smo izvedli v nevroetološkem laboratoriju Imobilizacija čebel Iz ependorfk s prostornino 1,5 ml smo naredili tulce za vpenjanje čebel. Z vsake smo odstranili pokrovček, ki smo ga z žebljem pritrdili na leseno desko v velikosti 60 x 10 x 3 cm. Spodnji del ependorfke smo z nožem diagonalno odrezali in na ta način pripravili tulec za imobilizacijo čebel. Kljub temu, da smo delali poskus le s 16 čebelami, smo jih vsakič ujeli nekaj več, saj je bilo treba misliti na to, da bodo nekatere čebele lahko zaradi stresa med poskusom umrle oz. da nekatere pri učenju sploh ne bodo sodelovale. Takšne čebele je bilo zato potrebno odstraniti iz našega eksperimenta. Tako smo naredili tudi 30 tulcev, ki smo jih v dveh vrstah po 15 pritrdili na leseno desko. Med vsakim tulcem je bilo vsaj 2 cm prostora, kar je preprečilo morebitne motnje med učenjem posamezne čebele. Pred vhodom v panj smo v erlenmajerico ujeli čebele in jo ob prihodu v laboratorij postavili na ledeno kopel. Čebele smo hladili toliko časa, dokler niso postale negibne. S pinceto smo čebelo prijeli za krila in jo dali v odrezano ependorfko ter njen zažetek med glavo in oprsjem prelepili z lepilnim trakom. Tako vpeto čebelo v tulcu smo postavili na pokrovček, pritrjen na leseni deski, ki je služil kod podstavek. Ko se je čebela nekoliko segrela, se je pričela ponovno premikati, pri tem pa je imela negibno oprsje.
40 29 Lepilni trak je moral biti dovolj dobro zatisnjen, da je čebela lahko kljub temu normalno iztegovala jeziček, a da ji hkrati z njim nismo preprečili normalnega pretoka hemolimfe in hrane v predelu vratu. Čebele smo vpeli v tulce v poznem popoldanskem času, z učenjem smo pričeli šele naslednji dan zjutraj. Slika 1a, b: Vpenjanje čebele v tulec. Slika 2: Vpete čebele, pripravljene za učenje.
41 Priprava raztopin Glede na rezultate prvega poskusa, kjer so čebele pile različne koncentracije raztopin ocetne in mlečne kisline, smo določili koncentracije raztopin teh snovi, ki smo jih uporabili pri učenju čebel. Predvsem z namenom, da bi čebele bolje zaznale hlape raztopin, uporabljene pri olfaktornem učenju, smo izbrali raje višje koncentracije testiranih raztopin. Čebele smo tako pogojevali z 2% vodno raztopino etanola, 5% vodno raztopino ocetne kisline ter 5% vodno raztopino mlečne kisline. Vse raztopine smo pripravili na dan poskusa v 50 ml bučkah in jih prelili v lončke ter preostalo shranili v hladilniku največ 3 dni. Poleg teh raztopin smo pripravili tudi sladkorno raztopino, tako da smo raztopili 25 g saharoze v 50 ml destilirane vode. Naša kontrolna tekočina je bila destilirana voda. Za učenje čebel z različnimi vonjavami smo pripravili tudi raztopino eteričnega olja sivke, v 50 ml destilirane vode smo kanili 2 kapljici tega eteričnega olja Izvedba poskusa Pitje raztopin v panju Pripravljene krmilnike za pitje raztopin smo postavili v panj in jih tam pustili stati vsaj 1 uro. Filtrirni papir je tekočino vpil in tako omogočil čebelam, da so lahko s pomočjo svojega jezička z njega srkale posamezne raztopine. Ta poskus smo večkrat ponovili, v enem primeru smo pustili krmilnike v panju stati toliko časa, dokler niso spile skoraj celotne kontrolne raztopine. Krmilnike s popitimi raztopinami smo po končanem poskusu odnesli v laboratorij in si zabeležili rezultate.
42 31 Slika 3: Pripravljeni krmilniki za pitje raztopin postavljeni v panju. Slika 4: Čebele med pitjem kontrolne raztopine.
43 Učenje čebel Učenje smo razdelili na tri stopnje. Prva stopnja je vključevala hranjenje čebel s sladkorno raztopino ter pitje vode za potešitev žeje, pri drugi smo izvedli habituacijo, zadnja stopnja pa je bila klasično pogojevanje z določeno raztopino kot pogojnim dražljajem Hranjenje s sladkorno raztopino in pitje vode Ko smo čebele vpeli v tulce, smo jih sprva dobro nahranili s sladkorno raztopino oz. smo jih začeli nanjo privajati, saj je le-ta kasneje pri učenju predstavlja nepogojni dražljaj. S filtrirnim papirčkom, pomočenim v 50% sladkorno raztopino, smo se dotaknili tipalnice vsake čebele, ta se je odzvala z iztegom jezička in pričela raztopino sesati. Čebele, ki že na ta dražljaj niso odgovorile, smo odstranili iz nadaljnjega poskusa. Čez noč smo čebele v tulcih pokrili z večjo preluknjano škatlo in z učenjem pričeli naslednje jutro. Da bi preprečili nehoten odziv čebel na kontrolo (vodo), smo jim dali naslednji dan najprej piti vodo, saj smo s tem potešili morebitno žejo. Na objektno stekelce smo za vsako čebelo s 50 µl Hamilton stekleno brizgo z iglo iztisnili 10 µl destilirane vode in ji dali piti. Ko smo dali piti vsem čebelam prvih 10 µl, smo vse še enkrat ponovili. Tako je dobila vsaka čebela 20 µl destilirane vode za žejo, hkrati pa smo si tudi zabeležili, koliko tekočine je približno spila vsaka čebela. Slika 5: Hranjenje čebele s sladkorno raztopino preko filtrirnega papirčka.
44 Habituacija Čebele smo pustili počivati 20 minut ter nato pričeli z drugo stopnjo poskusa, s habituacijo. S to vrsto neasociativnega učenja smo hoteli doseči, da se čebele prenehajo odzivati na kontrolo. S filtrirnim papirčkom, pomočenim v destilirano vodo, smo dražili vsako čebelo in si zabeležili njen PER odziv. Ko smo prišli do zadnje, šestnajste čebele, smo postopek habituacije ponovili. Da bi uspešno izvedli habituacijo, smo naredili vsaj šest ponovitev Klasično pogojevanje s PER odzivom Učenje smo opravili z vsako čebelo posebej, in sicer smo začeli z njim 15 minut po habituaciji. Čebele smo želeli naučiti na etanolno, ocetno in mlečno raztopino točno določenih koncentracij. Vsako klasično pogojevanje, ki je del asociativnega učenja, sestavljata dva pomembna člena, to sta pogojni in nepogojni dražljaj. Organizem mora dojeti povezavo med obema dražljajema, samo učenje je uspešno, ko se prične organizem samodejno odzivati na pogojni dražljaj, saj pri tem pričakuje nepogojni dražljaj, ki je tudi glavna motivacija za pogojni odziv. V našem primeru so predstavljale pogojni dražljaj vodne raztopine etanola, ocetne in mlečne kisline, nepogojni dražljaj pa sladkorna raztopina, ki je delovala kot nagrada za pogojni odziv. Za naše testne raztopine smo uporabili 2% raztopino etanola, 5% raztopino ocetne kisline ter 5% raztopino mlečne kisline. Sprva smo podražili tipalnico čebele s filtrirnim papirčkom, pomočenim v destilirano vodo, čemur ni sledila nobena nagrada. Destilirano vodo smo uporabili kot kontrolo. Čez približno 10 sekund smo podražili tipalnico čebele z določeno raztopino in čez 3 sekunde čebelo nagradili s 50% sladkorno raztopino. Hkrati smo si beležili število PER odzivov oz. kolikokrat so čebele iztegnile jeziček na določen dražljaj. Vsaka čebela je med vsakim učenjem počivala min, dokler nismo naredili enako še pri vseh ostalih čebelah. Celoten postopek učenja smo pri vsaki čebeli ponovili vsaj 5x Učenje z navidezno naključnim razporedom dražljajev Poleg mehanosenzoričnega pogojevanja smo poskusili čebele učiti še na podlagi olfaktornega oz. vonjalnega pogojevanja. Izbrali smo drugačen protokol učenja in hkrati zanesljivejšo metodo pogojevanja s pomočjo navidezno naključnega razporeda dražljajev»pseudo-random order«(abramson in sod., 2007). Pri tej metodi učenja je naš člen A predstavljala kontrola (destilirana voda), člen B pa določena testirana raztopina (pogojni dražljaj) skupaj s sladkorno raztopino kot nagrado (nepogojni dražljaj). Lahko bi rekli, da je šlo za tip diferencialnega učenja (A-, B+). Filtrirni papirček, pomočen v določeno testirano raztopino, smo s pomočjo pincete potisnili na dno injekcijske brizge in to (2,5 ml) čebeli pihnili na področje njenih tipalnic, saj so tipalnice pri čebelah glavni organ za zaznavanje vonjav.
45 34 Vseh 16 poskusnih čebel smo razdelili na polovico in jih učili po sledečem postopku/ zaporedju: -prvih 8 čebel: A B A A B A B B -preostalih 8 čebel: B A B B A B A A Kakor je zgoraj razvidno, smo drugo polovico čebel učili v obratnem zaporedju kot prvo polovico. Učenje smo pričeli tako, da smo prvim osmim čebelam ponudili A, preostalim osmim pa B, nato smo pričeli spet s prvo skupino čebel, ki smo jim dali tokrat B, drugi skupini pa A itd. Tako je vsaka čebela na svoj drugi dražljaj čakala celoten krog, približno kakih minut. Takšen postopek je omogočil tudi malo večji premor med posameznimi dražljaji. Ko smo končali s celotnim učenjem na podlagi učenja z navidezno naključnim razporedom dražljajev, smo pustili čebele počivati 30 minut, nato pa še enkrat ponovili celoten poskus. Čebele smo torej z vsako raztopino učili po tej metodi 2x. Ker je znano, da si čebele pri iskanju hrane poleg barve zapomnijo predvsem vonj cvetov, smo za lažjo primerjavo rezultatov naredili še učenje čebel z eteričnim oljem sivke, ki je predstavljalo pogojni dražljaj B. Pri tem učenju z različnimi vonjavami je bilo pomembno primerno prezračevanje prostora, s čimer smo preprečili mešanje dražljajev med seboj, ki bi povzročilo zmedo pri čebelah Zbiranje in obdelava podatkov Pitje raztopin v panju Po določenem času (minimalno 1 uri) smo odšli do panja po krmilnike in jih odnesli v laboratorij, kjer smo vseh 10 krmilnikov z različno popitimi raztopinami stehtali. Razlika med začetno in končno težo krmilnika nam je dala količino raztopine, ki so jo čebele spile. Vsi dobljeni podatki so bili v gramih, a smo lahko zato, ker smo pred pričetkom poskusa 10 ml vsake testirane raztopine stehtali, tudi končno popito količino raztopine iz gramov pretvorili nazaj v mililitre. Volumne različnih raztopin določenih koncentracij smo primerjali med seboj in ugotovili, kolikšne koncentracije naših testiranih raztopin čebele pijejo, preverili pa smo tudi delež popite raztopine v primerjavi s kontrolo Učenje čebel Pri učenju čebel z dotikom tipalnic smo označevali različne odzive čebel na določen dražljaj, znak + je pomenil PER odziv, znak pa da PER odziva ta dražljaj ni povzročil. Uspešno se je učila tista čebela, pri kateri se je pojavil odziv v zaporedju -+, kar je pomenilo, da se je čebela prenehala odzivati na kontrolo in da se je pravilno odzvala le na pogojni dražljaj, kateremu je sledil nepogojni dražljaj oz. nagrada (hrana). Takšno
46 35 zaporedje odzivov pa se je moralo pri čebeli pojaviti vsaj v dveh zaporednih ponovitvah poskusa, da smo lahko potrdili, da se čebela uči. Pri učenju z navidezno naključnim razporedom dražljajev je bila uspešna tista čebela, ki se ni odzvala na A dražljaj (kontrola), kar smo označili z -, odzvala pa se je na B dražljaj (določena raztopina + nagrada), kar smo označili z znakom +. Spremljali smo tudi čas, ki ga je posamezna čebela potrebovala, da se je priučila pogojnega odziva. 3.2 VPLIV RAZTOPIN NA PREDELAVO MEDU V CELICAH SATJA V PANJU Opis poskusa Pri drugem delu raziskave smo se lotili našega poglavitnega poskusa, kjer smo poskušali ugotoviti, kakšen vpliv imajo raztopine etanola, ocetne in mlečne kisline na predelavo medu v panju. Opazovali smo reakcijo čebel ob dodatku posameznih raztopin v celice satja, napolnjene z medom, ter končno stanje satnih celic. Naš cilj je bil torej, da opredelimo vlogo teh snovi v čebelji družini pri predelavi hrane v panju oz. da ugotovimo, ali te snovi čebelam predstavljajo le prehranski dražljaj, ki povzroči takojšnje konzerviranje hrane in zapiranje satnih celic, ali pa delujejo naše testne raztopine kot dražeče kemične snovi, ki bi lahko povzročile kvarjenje medu in zato spodbujajo čebele k še večji predelavi le-tega Priprava poskusa Priprava raztopin Za dodajanje raztopin etanola, ocetne in mlečne kisline v celice satja smo uporabili nižje koncentracije teh raztopin, saj smo želeli koncentracije čim bolj približati tistim, ki se običajno pojavljajo v panju in so del življenja čebel. V 50 ml bučkah smo tako pripravili 2% vodno raztopino etanola, 1% vodno raztopino ocetne kisline ter 2% vodno raztopino mlečne kisline. Naša kontrola je bila ponovno destilirana voda Izvedba poskusa Poskus smo izvedli tako, da smo v celice satja, napolnjene z medom in pokrite z voščenimi pokrovci, z iglo vbrizgali 5 µl posamezne raztopine. Pred tem smo posamezno zaprto celico na rahlo nekoliko predrli oz. odprli z žebljičkom. Da bi v vsako satno celico prodrli z iglo enako globoko, smo na iglo namestili paličico in s tem dosegli, da je bil spodnji del igle od paličice navzdol dolg 8 mm. Tako smo v vse celice satja, ki so globoke 12,5 mm, z iglo prodrli 8 mm globoko.
47 Različni načini vbrizgavanja raztopin v celice satja Sam eksperiment bi lahko razdelili na tri dele, saj smo pri vsakem izbrali drugačen pristop/ drugačen način ali vrstni red vbrizgavanja raztopin. Vbrizgavanje z raztopinami smo pričeli v opazovalnem panju v čebelarski hišici poleg Biotehniške fakultete Oddelka za biologijo. To smo izvajali preko vmesnega pleksi stekla, za katerim je bilo satje. S poskusom smo kmalu prekinili, saj so bile čebele še v fazi gradnje satja in so nam vse luknjice, narejene v pleksi steklu, zapirale s propolisom. Zato smo delo nadaljevali zunaj, v nakladalnem panju. Iz njega smo vzeli satje, ki je bilo v večini že napolnjeno z zrelim medom, z njega otresli čebele in ga odnesli v laboratorij. Z žebljičkom smo predrli voščene pokrovce, da smo lahko z iglo vbrizgali posamezne raztopine. Vsako testirano raztopino smo vbrizgali v 8 satnih celic, razporejenih v dveh stolpcih po 4 satne celice. Vmes smo spustili 4 satne celice in spet zapolnili naslednjih 8 satnih celic z drugo raztopino itd. Raztopine smo primerjali še s kontrolo (destilirana voda) ter z le nekoliko odprtimi satnimi celicami. Na okvir satja smo tudi označili zaporedje vbrizgavanja raztopin: O (raztopina ocetne kisline), M (raztopina mlečne kisline), E (raztopina etanola), V (destilirana voda) ter L (luknjica). Satje smo odnesli nazaj v panj in čez eno uro preverili rezultate. Naslednji dan smo poskusili z vbrizgavanjem raztopin v celice satja kar poleg panja. Iz nakladalnega panja smo vzeli 3 sate, saj smo vse testirane raztopine ločili med seboj. Vsako izmed raztopin smo primerjali s kontrolo (destilirana voda) in z odprto satno celico. Tako smo v prvem satju 8 satnih celic, napolnjenih z medom, le odprli, nato v naslednjih 8 vbrizgali vodo ter v zadnjih 8 še raztopino etanola. Na vsakem satju je bilo 24 opazovanih satnih celic. Na okvir satja smo to tudi zapisali v pravilnem zaporedju vbrizgavanja: L, V, E. Drugi sat je bil L, V, M, tretji pa L, V, O. Po končanem vbrizgavanju vseh naših testnih raztopin smo satje dali nazaj v panj in prve rezultate preverili čez 1 uro. Po tem času smo ponovno preverili stanje čez 20 min in si prav tako zabeležili rezultate ter vse skupaj pogledali še naslednji dan zjutraj. Po tem smo še enkrat v 3 nove sate vbrizgali posamezne raztopine in v času 80 min 2x preverili rezultate. Kasneje smo pričeli vsakemu satu dodajati druge raztopine, in sicer smo v prvo satje dodali še V in M, v drugo V in O in v tretje V in E. Za takšen protokol smo se odločili, da bi zmanjšali morebiten vpliv izpostavljenosti satov mikroorganizmom in vlagi izven panja. Po eni uri smo pogledali rezultate in vsakemu od treh satov dodali še preostale manjkajoče raztopine, torej prvi še V in O, drugi še V in E in tretji še V in M. Tako smo v vsakega od satov vbrizgali vse raztopine, v prvem so bili na začetku L,V in E, nato v sredini V in M in na koncu V in O itd. Po končanem delu smo počakali eno uro in preverili stanje satnih celic. Stanje vseh treh satov, kjer so bile v vsako satje vbrizgane vse raztopine, smo zabeležili tudi naslednji dan.
48 37 Slika 6: Drugi vpogled dogajanja v satju, kjer je bila vbrizgana raztopina mlečne kisline. Slika 7: Drugi vpogled dogajanja v satju, kjer je bila vbrizgana raztopina ocetne kisline.
49 Preverjanje vpliva mehanskih poškodb satnih celic v panju Iz nakladalnega panja smo vzeli sat, s satja odstranili čebele in ga odnesli v laboratorij. Raztopine smo tokrat vbrizgali na zgornjem delu satja v sledečem zaporedju: V, E, M, O, kjer je vsaka izmed raztopin obsegala 4 satne celice v stolpcu navzdol. Vmes smo spustili nekaj satnih celic, tako med posameznimi raztopinami, kot tudi med ponovnimi poskusi, saj smo to ponovili še 3x. Raztopine smo tokrat v satne celice vbrizgali neposredno, brez predhodnega odpiranja satnih celic z žebljičkom. V spodnjem delu pa smo z žebljičkom naredili le luknjice, in sicer 16 stolpcev po 3 luknjice različnih velikosti, od zelo majhne, srednje velike, do zelo velike luknjice. S tem smo želeli poleg vpliva raztopin na predelavo medu hkrati opazovati še vpliv poškodovanih satnih celic na čebele v panju. Celoten sat smo postavili nazaj v panj in čez 1 uro preverili rezultate Zbiranje in obdelava podatkov Preverili smo stanje satnih celic po vbrizgavanju naših testnih raztopin. Zabeležili smo si, ali so ostale satne celice, ki smo jih nekoliko odprli, nedotaknjene, ali so jih čebele še bolj odprle, ali so jih začele čebele zapirati, ali so čebele satne celice popolnoma odprle oz. jih popolnoma zaprle. Zabeležili smo si tudi količino medu v odprti satni celici, torej ali so čebele napolnjeno satno celico izpraznile oz. jo začele na novo polniti z medom ali pa se medu sploh niso dotaknile in ga v tem primeru niso ponovno predelovale. V primeru, da je bila satna celica odprta in napolnjena z medom, smo glede na čas lahko sklepali o sami predelavi medu. Potek ponovne predelave medu v satni celici poteka v sledečem vrstnem redu: odpiranje satne celice praznjenje satne celice z medom polnjenje satne celice s ponovno predelanim medom pokritje satne celice z voščenim pokrovcem. Stanje satne celice smo označili numerično po principu dvosmerne ordinalne skale DOS (Preglednica 1). V našem primeru je število 0 predstavljalo nedotaknjeno satno celico. Negativne vrednosti so vodile v odpiranje satnih celic, kjer je bila -1 popolnoma odprta izpita satna celica, ravno obratno pa so pozitivne vrednosti prikazovale zapiranje satnih celic, tako je število 1 definiralo popolnoma zaprto satno celico. S pomočjo teh numeričnih vrednosti smo lahko izračunali indeks stanja satnih celic (ISSC).
50 39 Preglednica 1: Prikaz numeričnih vrednosti posameznih satnih celic. Stanje satne celice Numerična vrednost (DOS) ZAPRTA 1 V ZAPIRANJU 0,5 NESPREMENJENA 0 V ODPIRANJU -0,25 DELNO ODPRTA -0,5 ODPRTA (POLNA) -0,75 ODPRTA (IZPRAZNJENA) -1 Primer izračuna indeksa stanja satnih celic, kjer je bila pred opazovanjem vbrizgana etanolna raztopina: 1) posamezno numerično vrednost stanja satne celice glede na DOS (npr. -1) smo množili s številom takih (npr. odprtih izpitih) satnih celic v točno določenem času 2) na ta način smo izračunali posamezne vrednosti za različne satne celice v tem času 3) vse te dobljene vrednosti smo sešteli in jih delili s številom celic, v katere smo vbrizgali etanolno raztopino Vbrizgana snov Odprta (izpraznjena) Odprta (polna) Delno odprta V odpiranju Nespremenjena E (etanol) 2 6 V zapiranju Zaprta Število celic, v katere smo vbrizgali etanolno raztopino: 8 Izračun: Odprta izpraznjena satna celica: -1 (numerična v.) x 0 (število takih celic)= 0 Odprta polna satna celica: -0,75 x 2= -1,5 Nespremenjena: 0 x 6= 0 Delno odprta satna celica: -0,5 x 0= 0 V zapiranju: 0,5 x 0= 0 V odpiranju: -0,25 x 0= 0 Zaprta satna celica: 1 x 0= 0
51 40 Indeks stanja satne celice (v tem primeru s prej vbrizgano etanolno raztopino): Seštevek dobljenih vrednosti, deljen s številom vbrizganih celic, kar pomeni: (0+ (-1,5) ) : 8= -0,1875 Pri zadnjem poskusu preverjanja mehanskih poškodb satnih celic, kjer smo zraven satnih celic z raztopinami naredili še luknjice različnih velikosti, pa smo poleg skupnega indeksa satnih celic pri vsaki snovi izračunali še pozitivno ter negativno vrednost ISSC-ja, in sicer na sledeč način (pri tem nismo upoštevali nespremenjenih s.c.): - pozitiven ISSC: seštevek pozitivnih dobljenih vrednosti snovi (število zaprtih s.c. in tistih v zapiranju), deljen s številom vseh vbrizganih celic s to snovjo - negativen ISSC: seštevek negativnih dobljenih vrednosti (število odprtih s.c, delno odprtih in tistih v odpiranju), deljen s številom vseh vbrizganih celic s to snovjo - skupni ISSC: seštevek pozitivnega in negativnega ISSC-ja Statistično obdelavo podatkov smo naredili na spletni strani kjer smo uporabili χ2 test z Yates-ovo korekcijo. S testom smo primerjali vse možne kombinacije tretmanov med seboj in tako preverili, če med njimi obstaja korelacija oz. če so prisotne značilne statistične razlike.
52 41 4 REZULTATI 4.1 ZAZNAVANJE NIZKIH KONCENTRACIJ RAZTOPIN ETANOLA, OCETNE IN MLEČNE KISLINE Pitje raztopin Naredili smo dvojno serijo poskusov, tako da smo za vsako testirano raztopino v panj postavili hkrati 2 krmilnika. Prvi dan poskusa (Slika 8) smo preverili rezultate po eni uri. Če pogledamo rezultate prvih krmilnikov oz. prvo serijo poskusa, so čebele pričakovano spile največ kontrolne raztopine. Kar se tiče naših testiranih raztopin, so pile raje nižje koncentracije, saj vidimo, da so spile več 2% raztopine mlečne kisline v primerjavi s 5%, pri raztopini ocetne kisline pa celo trikrat več te raztopine z nižjo koncentracijo. Če primerjamo nižje koncentracije mlečne in ocetne kisline, nam podatki kažejo, da so čebele spile v tem primeru celo več ocetne kisline, pri višjih koncentracijah pa jih je bolj pritegnila raztopina mlečne kisline. V primerjavi s kontrolo (Preglednica 2) so spile 47,1%, 2% raztopine ocetne kisline, kar je skoraj polovica, takoj za njo je sledila 2% raztopina mlečne kisline z 32,6%. Druga serija poskusa kaže na večinoma podobne rezultate kot prva, le da so tu čebele spile več 2% raztopine mlečne kot ocetne kisline (33,3% glede na kontrolo). Razlika v pitju med višjima koncentracijama raztopin mlečne in ocetne kisline je zelo majhna (0,043 ml). Podobno intenzivnost pitja raztopin smo opazili tudi pri poskusu narejenem v juniju (Priloga A), kjer so bili krmilniki v panju prav tako eno uro. 2,5 2 V(ml) 1,5 1 0,5 0 KONTROLA 2 % MLEČNA K. 5 % MLEČNA K. Vrsta raztopine 2 % OCETNA K. 5 % OCETNA K. Slika 8: Volumen popitih raztopin dne Prvi stolpec pri posamezni raztopini predstavlja prvi lonček, drugi stolpec pa drugi. Vsi lončki so bili v panj dodani ob istem času.
53 42 Preglednica 2: Prikaz deleža popite testne raztopine glede na kontrolno raztopino dne LONČEK 2. LONČEK RAZTOPINE V (ml) DELEŽ (%) popite raztopine glede na kontrolo V (ml) DELEŽ (%) popite raztopine glede na kontrolo KONTROLA 1,132 / 2,481 / 2% MLEČNA KISLINA 0,369 32,6 0,826 33,3 5% MLEČNA KISLINA 0,278 24,6 0,259 10,4 2% OCETNA KISLINA 0,533 47,1 0,584 23,5 5% OCETNA KISLINA 0,158 14,0 0,216 8,7 Pri naslednjem poskusu (Slika 9), ki smo ga izvedli tri dni za tem, smo pustili krmilnike v panju stati toliko časa, dokler niso čebele spile skoraj celotne kontrolne raztopine (približno 3 ure). Pri obeh serijah poskusa lahko s histograma razberemo podobne rezultate, kar pomeni, da so si po vrstnem redu od največ do najmanj spite raztopine sledile: kontrolna raztopina, 2% raztopina mlečne kisline, 2% raztopina ocetne kisline, 5% raztopina mlečne kisline ter nazadnje še 5% raztopina ocetne kisline. Zanimiv je pogled druge serije krmilnikov, kjer je bil delež popite 2% raztopine mlečne kisline glede na kontrolo celo 74%, 2% raztopina ocetne kisline pa je dosegla vrednost polovice popite kontrolne raztopine (Preglednica 3). V (ml) KONTROLA 2 % MLEČNA K. 5 % MLEČNA K. 2 % OCETNA K. 5 % OCETNA K. Vrsta raztopine Slika 9: Volumen popitih raztopin dne Prvi stolpec pri posamezni raztopini predstavlja prvi lonček, drugi stolpec pa drugi. Vsi lončki so bili v panj dodani ob istem času.
54 43 Preglednica 3: Prikaz deleža popite testne raztopine glede na kontrolno raztopino dne LONČEK 2. LONČEK RAZTOPINE V (ml) DELEŽ (%) popite raztopine glede na kontrolo V (ml) DELEŽ (%) popite raztopine glede na kontrolo KONTROLA 9,594 / 9,401 / 2% MLEČNA KISLINA 4,965 51,8 6,958 74,0 5% MLEČNA KISLINA 2,256 23,5 1,541 16,4 2% OCETNA KISLINA 3,630 37,8 4,754 50,6 5% OCETNA KISLINA 1,290 13,4 1,082 11,5 Iz rezultatov je razvidno, da so čebele pile vse naše testne raztopine, pri tem pa so pile raje nižje koncentracije teh raztopin. Najvišji volumen spite raztopine je pri 2% raztopini mlečne kisline, izjema je le prva serija poskusa narejena dne , kjer je najvišji volumen pri 2% raztopini ocetne kisline (Slika 8). Tako smo lahko pričeli z učenjem čebel, kjer je bil glavni namen zmožnost zaznavanja in razlikovanja nizkih koncentracij raztopin etanola, ocetne in mlečne kisline Učenje čebel Spodaj so prikazani rezultati olfaktornega oz. vonjalnega pogojevanja s PER odzivom po metodi učenja z navidezno naključnim razporedom dražljajev, kjer smo učili 16 čebel v dveh skupinah po 8 čebel. Pri vseh poskusih je bila člen A kontrola (voda), člen B pa posamezna testirana raztopina, ki je bila določena kot pogojni dražljaj skupaj s sladkorno raztopino kot nagrado. Pričeli smo z učenjem čebel z 2% raztopino etanola. Rezultati kažejo, da začetno učenje ni bilo ravno uspešno, saj je razlika med številom PER odzivov, tako na dražljaj A kot na dražljaj B, minimalna (d=1). Vidimo, da se število čebel s PER odzivom pri obeh dražljajih ves čas giblje med 7 in 8 (Slika 10). Pri tretjem zaporednem dražljaju s kontrolo se odziv poveča za eno čebelo, a nato pri sedmem zaporednem dražljaju ponovno zabeležimo enak odziv na kontrolo kot na začetku. Pogojni odziv skozi celoten poskus niha med 7 in 8 čebelami. Iz grafikona (Slika 11), ki prikazuje rezultate po 30 minutah, ko smo naš poskus ponovili, lahko razberemo, da so se čebele na začetku odzivale pričakovano, a se je pri četrtem zaporednem dražljaju ponovno zelo povečala odzivnost na kontrolo (7 čebel). V zadnjih dražljajih so bili odzivi kontrole in pogojnega dražljaja primerljivi.
55 44 Število čebel s PER odzivom A B Zaporedni dražljaj Slika 10: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z 2% raztopino etanola. Dražljaj A je bila kontrola (voda), pogojni dražljaj B pa je bila 2% raztopina etanola, ki ji je sledila sladkorna raztopina kot nagrada Število čebel s PER odzivom A B Zaporedni dražljaj Slika 11: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z 2% raztopino etanola (ponovitev poskusa po 30 min).
56 45 Učenje smo nadaljevali s 5% raztopino ocetne kisline. Začetni poskus (Slika 12) kaže, da se je veliko čebel kljub habituaciji, ki smo jo izvedli pred samim učenjem, odzivalo na kontrolo, od četrtega zaporednega dražljaja naprej smo zabeležili konstantno naraščanje števila čebel s PER odzivom. Odzivnost čebel na B dražljaj je bil v primerjavi z A dražljajem dokaj nizek, velik preskok je mogoče opaziti pri petem zaporednem dražljaju, ko je število čebel s PER odzivom naraslo z 2 kar na 6, a je temu kmalu ponovno sledil padec odziva na pogojni dražljaj. Ponoven poskus učenja po 30 minutah (Slika 13) prikazuje še zmeraj 7 čebel, ki so vztrajale pri odzivu na kontrolo do četrtega zaporednega dražljaja, ko smo zabeležili le 5 čebel, ki so se odzvale na vodo. Že pri šestem zaporednem dražljaju vidimo ponovno večje število čebel s PER odzivom. Na pogojni dražljaj se je v primerjavi s kontrolo, prav tako kot pri prvem poskusu, odzvalo manj čebel, saj je število variiralo med 3 in Število čebel s PER odzivom A B Zaporedni dražljaj Slika 12: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino ocetne kisline. Dražljaj A je bila kontrola (voda), pogojni dražljaj B pa je bila 5% raztopina ocetne kisline, ki ji je sledila sladkorna raztopina kot nagrada.
57 Število čebel s PER odzivom A B Zaporedni dražljaj Slika 13: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino ocetne kisline (ponovitev poskusa po 30 min). Naša zadnja testirana raztopina je bila 5% raztopina mlečne kisline. Rezultati iz prvega grafikona (Slika 14) prikazujejo preskok pri petem zaporednem dražljaju, ko je število čebel, ki se je odzvalo na A dražljaj, padlo s 7 na 5, število čebel pri odzivu na B dražljaj pa je glede na prvi zaporedni dražljaj takrat doseglo maksimum z odzivom osmih čebel. Po končnem, osmem zaporednem dražljaju, je število čebel s PER odzivom na oba naša dražljaja enako. Pri ponovnem poskusu učenja po 30 minutah lahko vidimo opazno razliko (Slika 15), še posebej pri drugem zaporednem dražljaju. Pri tem odziv na kontrolo nenadoma pade, saj se nanj odzove le še 5 čebel, medtem ko je odziv na pogojni dražljaj B visok (N=8). Tudi pri sedmem zaporednem dražljaju pride do manjšega števila čebel, ki so se odzvale na A dražljaj, ves čas pa ostaja v primerjavi z odzivom na kontrolo dokaj visok odziv na raztopino mlečne kisline.
58 47 Število čebel s PER odzivom A B Zaporedni dražljaj Slika 14: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino mlečne kisline. Dražljaj A je bila kontrola (voda), pogojni dražljaj B pa je bila 5% raztopina mlečne kisline, ki ji je sledila sladkorna raztopina kot nagrada Število čebel s PER odzivom A B Zaporedni dražljaj Slika 15: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju s 5% raztopino mlečne kisline (ponovitev poskusa po 30 min).
59 48 Za lažjo primerjavo rezultatov in s tem tudi za preverbo korektnosti celotnega testiranja smo čebele poleg naših testiranih raztopin pogojevali tudi z eteričnim oljem sivke, ki je ena izmed vonjav iz narave, s katero se čebele srečujejo in si jo morajo zapomniti, kajti sivka je prav tako kot druge rastline vir njihove hrane. Rezultati učenja (Slika 16) kažejo na začetku zelo nizek odziv na vodo, ki pa že pri drugem zaporednem dražljaju zelo naraste, nato pa lahko šele pri šestem zaporednem dražljaju vidimo ponoven drastičen padec števila čebel s PER odzivom. Takrat smo zabeležili tudi največjo razliko v številu odziva čebel na oba dražljaja (N A =1, N B =7). Pri dražljaju B pa z naraščanjem števila zaporednih dražljajev počasi narašča tudi število čebel s pogojnim odzivom. Pri ponovitvi poskusa (Slika 17) se odstopanja med odzivom na A in B dražljaj še nadaljujejo. Tu bi bilo potrebno izpostaviti peti zaporedni dražljaj, kjer je naglo padla odzivnost na kontrolo, hkrati pa se je povečala odzivnost na eterično olje sivke. Zaključek poskusa kaže visoko število čebel (N=6) s pogojnim odzivom, po drugi strani pa se je na kontrolo odzvala le ena čebela Število čebel s PER odzivom A B Zaporedni dražljaj Slika 16: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z eteričnim oljem sivke. Dražljaj A je bila kontrola (voda), pogojni dražljaj B pa je bila 5% raztopina mlečne kisline, ki ji je sledila sladkorna raztopina kot nagrada.
60 49 Število čebel s PER odzivom A B Zaporedni dražljaj Slika 17: Število čebel s PER odzivom v odvisnosti od števila zaporednega dražljaja pri učenju z eteričnim oljem sivke (ponovitev poskusa po 30 min).
61 VPLIV RAZTOPIN NA PREDELAVO MEDU V CELICAH SATJA V PANJU Uporaba različnih pristopov vbrizgavanja raztopin je dala drugačen potek opažene predelave medu v celicah satja, a pri vseh primerih dokaj podobne rezultate predelave za isto snov. Ob pogledu na rezultate (Slike 18, 19 in 20) prvega dne poskusa ( ) je po 1h 20 min viden zelo podoben potek predelave satnih celic z našimi testnimi raztopinami, vendar je bilo odpiranje največje pri celicah satja z etanolno raztopino. V prvem satu (Slika 18), kjer smo vbrizgali raztopino etanola, se je izkazalo, da so po eni uri čebele satne celice z etanolno raztopino začele odpirati in jih skoraj že delno odprle v primerjavi s kontrolama, ki v tem času kažeta pozitivne indekse. Luknjice so popolnoma zaprle, saj vidimo, da je indeks enak 1. Ponoven vpogled čez 20 minut kaže popolno odpiranje satnih celic z etanolno raztopino glede na vodo, kjer je bilo približno enako število odprtih in zaprtih satnih celic (ISSC=0), luknjice pa so začele nekoliko odpirati. Pri rezultatih naslednjega dne vidimo, da so začele čebele satne celice z etanolno raztopino, ki so jih izpraznile in jih napolnile z novim medom, ponovno zapirati v nasprotju s satnimi celicami z vodo, ki prikazujejo večji delež odpiranja (N=7). Če primerjamo satne celice etanola še z luknjicami, opazimo podobno dogajanje pri obeh, torej zapiranje satnih celic. 1 0,75 0,5 Indeks stanja satnih celic 0,25 0-0,25 1 h 1:20 h Naslednji dan Luknjice Voda Etanol -0,5-0,75-1 Čas Slika 18: Indeks stanja satnih celic v odvisnosti od časa v satu z 2% raztopino etanola.
62 51 V drugem satu, kjer smo vbrizgali raztopino mlečne kisline (Slika 19), so ostale po eni uri satne celice z raztopino mlečne kisline nespremenjene oz. nedotaknjene, tudi indeks luknjic je enak 0, vendar je bilo tu število odprtih in zaprtih satnih celic enako. Pri vodi je vidno odpiranje satnih celic. Po 1h 20 min od pričetka poskusa se pri luknjicah ni kaj veliko spremenilo, opazne pa so velike razlike pri ostalih dveh, kjer smo izračunali negativne vrednosti ISSC-ja. Čebele so satne celice, tako z vodo kot z raztopino mlečne kisline, odprle in jih začele prazniti, pri vodi je bila opažena le ena odprta izpita satna celica več (N=6) v primerjavi s satnimi celicami z raztopino mlečne kisline. Naslednji dan so začele čebele satne celice, v katere je bila vbrizgana mlečna kislina, na novo zapirati. Takrat smo zabeležili odstopanje obeh kontrol v primerjavi z mlečno kislino. Pri satnih celicah z vodo se ni nič posebnega zgodilo, saj so bile satne celice še zmeraj odprte (ISSC= -0,75), pri luknjicah pa vidimo popolno nasprotje in indeks 1, ki definira zaprte satne celice. 1 0,75 0,5 Indeks stanja satnih celic 0,25 0-0,25 1 h 1:20 h Naslednji dan Luknjice Voda Mlečna kislina -0,5-0,75-1 Čas Slika 19: Indeks stanja satnih celic v odvisnosti od časa v satu z 2% raztopino mlečne kisline.
63 52 V zadnjem satu smo opazovali vpliv raztopine ocetne kisline na stanje satnih celic in predelavo medu v primerjavi z obema kontrolama (Slika 20). Pri prvem beleženju rezultatov po eni uri vidimo, da so začele čebele luknjice zapirati, pri satnih celicah z raztopino ocetne kisline in z vodo pa je bil največji delež nespremenjenih satnih celic (N voda =5, N ocetna k. =4), ostale celice so čebele zapirale. Večja sprememba je vidna po 1h 20 min, ko so luknjice v primerjavi s satnimi celicami ostalih dveh snovi že skoraj vse zaprte. Podobno stanje zasledimo pri satnih celicah z raztopino ocetne kisline in tistimi z vodo, saj so tu čebele satne celice odpirale, pri vsaki od obeh snovi smo opazili tudi 2 odprte izpite satne celice. Naslednji dan so pri vseh treh naših opazovanih snoveh rezultati enotni in vsi trije dosegajo ISSC 1, kar pomeni, da so čebele vse satne celice popolnoma zaprle. 1 0,75 0,5 Indeks stanja satnih celic 0,25 0-0,25 1 h 1:20 h Naslednji dan Luknjice Voda Ocetna kislina -0,5-0,75-1 Čas Slika 20: Indeks stanja satnih celic v odvisnosti od časa v satu z 1% raztopino ocetne kisline. Rezultati poskusov (Slike 18, 19 in 20) prikazujejo največje odpiranje satnih celic z etanolno raztopino, nekoliko manjše pri celicah satja z raztopino mlečne kisline, satne celice z vbrizgano raztopino ocetne kisline pa so čebele v primerjavi s prvima dvema bolj zapirale.
64 Naslednji dan 1:20 h 1 h Puhalić, N. Etanol, ocetna in mlečna kislina kot ključni dražljaji za predelavo hrane v čebelji družini. 53 Preglednica 4: Prikaz števila različnih stanj satnih celic s snovmi, razporejenimi po satih glede na čas. Zajema čas raztopine v satju, sat z raztopinami, stanje satne celice in njegovo število ter izračunan ISSC vsake snovi v posameznem satu in ob določenem času. Čas razt. v satju Sat S1 S2 S3 S1 S2 S3 S1 S2 S3 Vbrizgana snov Odprta (izpr.) Odprta (polna) Stanje satne celice Delno odprta V odp. Nespr. V zap. Zaprta INDEKS L 8 1 V 3 5 0,438 E 6 2-0,438 L V 7 1-0,219 M 8 0 L ,344 V 5 3 0,188 O ,063 L ,125 V E 5 3-0,906 L ,031 V ,719 M ,656 L 1 7 0,844 V ,125 O ,250 L 3 5 0,344 V 7 1-0,688 E 7 1-0,688 L 8 1 V 8-0,750 M 6 2-0,313 L 8 1 V 8 1 O 8 1
65 54 Drugi dan poskusa, , smo izbrali drugačen način dela, saj smo v vseh treh satih uporabili različno zaporedje vbrizgavanja raztopin, vendar smo v vsakega izmed njih dodali vse raztopine (Slike 21, 22 in 23). Ker se je izkazalo, da so čebele luknjice večinoma zapirale, smo kasneje kot kontrolo uporabili le vodo. Rezultate smo preverili najprej čez 40 min, nato čez 1h 20 min, 2h 40 min, 3h 40 min ter naslednji dan. V prvi sat smo v satne celice dodali najprej etanolno raztopino skupaj z obema kontrolama in naredili v času 1h 20 min dva vpogleda, nato pa smo zraven dodali raztopino mlečne kisline skupaj z vodo kot kontrolo, čez 2 h 40 min pa še raztopino ocetne kisline prav tako z vodo kot kontrolo. Na grafikonu (Slika 21) so prikazani rezultati prvega vpogleda ter rezultati naslednjega dne prve naknadno dodane raztopine, ki je bila v tem primeru 2% raztopina mlečne kisline. Po 1h 20 min, kolikor je bila raztopina mlečne kisline skupaj s kontrolo v panju do prvega vpogleda, so čebele satne celice glede na kontrolo manj odpirale, največ je bilo nespremenjenih satnih celic (N=4). Naslednji dan so čebele satne celice, tako tiste, ki so bile napolnjene z raztopino mlečne kisline, kot tiste z vodo, zapirale. ISSC je pri kontroli višji kot pri raztopini mlečne kisline (0,563), kar pomeni da je bilo pri kontroli več zaprtih satnih celic. Iz preglednice (Preglednica 5), ki prikazuje različen potek predelave medu v prvem satu ob dodatku raztopine določene snovi, je možno razbrati, da so čebele hitreje odpirale in predelovale satne celice z vodo, kar pojasnjujejo tudi rezultati naslednjega dne, ki kažejo več zaprtih celic satja z vbrizgano vodo. Glede na čas in stanje satnih celic lahko predvidevamo, da so čebele med z raztopino mlečne kisline dlje časa predelovale. Pri kontroli je od prvega vpogleda snovi do naslednjega dne viden velik porast ISSC-ja. 1 0,75 0,5 Indeks stanja satnih celic 0,25 0-0,25 Prvi vpogled snovi Naslednji dan Voda Mlečna kislina -0,5-0,75-1 Čas Slika 21: Indeks stanja satnih celic z vbrizgano 2% raztopino mlečne kisline glede na kontrolo po 1 h 20 min (prvi vpogled snovi) ter naslednji dan.
66 SAT 1 Puhalić, N. Etanol, ocetna in mlečna kislina kot ključni dražljaji za predelavo hrane v čebelji družini. 55 Preglednica 5: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v prvem satu, kamor je bila na začetku dodana etanolna raztopina. Zajema čas vpogleda satnih celic, saj so bile raztopine v sat naknadno dodane, stanje satne celice in njegovo število ter izračunan ISSC vsake snovi ob določenem času. Siva barva označuje snovi, ki sta bili v sat dodani po 1h 20 min od pričetka poskusa, roza barva pa snovi, ki sta bili po 2h 40 min dodani zadnji. Čas vpogleda satnih c. Vbrizgana snov Odprta (izpr.) Odprta (polna) Delno odprta V odp. Nespr. V zap. Zaprta INDEKS 0:40 h 1:20 h 2:40 h 3:40 h Naslednji dan L ,375 V ,125 E ,125 L V 2 6-0,813 E ,406 V ,344 M ,031 L ,031 V ,375 E ,313 V ,469 M ,469 V ,188 O ,281 L 8 1 V ,156 E V 2 6 0,563 M ,281 V 6 2-0,313 O ,031
67 56 V drugi sat smo v satne celice dodali najprej raztopino mlečne kisline skupaj z obema kontrolama in naredili v času 1h 20 min dva vpogleda, nato pa smo zraven dodali raztopino ocetne kisline skupaj z vodo kot kontrolo, čez 2h 40 min pa še etanolno raztopino prav tako z vodo kot kontrolo. Na grafikonu (Slika 22) so prikazani rezultati prvega vpogleda ter rezultati naslednjega dne prve naknadno dodane raztopine, ki je bila v tem primeru 1% raztopina ocetne kisline. Dogajanje v satnih celicah s kontrolo in z vbrizgano raztopino ocetne kisline je bilo zelo podobno, kar nakazuje tudi minimalna razlika v ISSC-ju (le 0,032). Vrednosti ISSC-ja gredo pri obeh pod 0, kar pomeni, da so čebele satne celice odpirale. Prav tako je bilo tudi naslednji dan stanje satnih celic obeh snovi podobno, čebele so satne celice zapirale, čeprav je ostalo veliko satnih celic tudi odprtih, zato kaže grafikon tako nizke vrednosti ISSC-ja. Pri ocetni kislini vidimo, da je šlo zapiranje še nekoliko počasneje v primerjavi s kontrolo. Dodaten vpogled po 3h 40 min od nastavitve poskusa (Preglednica 6) pa prikazuje, tako pri satnih celicah z vbrizgano raztopino ocetne kisline kot pri tistih s kontrolo, odpiranje satnih celic in predelavo medu. Tukaj bi bilo zanimivo izpostaviti dogajanje v satnih celicah z raztopino mlečne kisline, kjer je bilo po 3h 40 min opaženih 5 odprtih izpitih satnih celic in je bil zato izračunan ISSC celo -0,844. Naslednji dan je ISSC že 0,375, kar nakazuje na končano predelavo medu in ponovno zapiranje celic. 1 0,75 0,5 0,25 Indeks stanja satnih celic 0-0,25 Prvi vpogled snovi Naslednji dan Voda Ocetna kislina -0,5-0,75-1 Čas Slika 22: Indeks stanja satnih celic z vbrizgano 1% raztopino ocetne kisline glede na kontrolo po 1h 20 min (prvi vpogled snovi) ter naslednji dan.
68 SAT 2 Puhalić, N. Etanol, ocetna in mlečna kislina kot ključni dražljaji za predelavo hrane v čebelji družini. 57 Preglednica 6: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v drugem satu, kamor je bila na začetku dodana raztopina mlečne kisline. Zajema čas vpogleda satnih celic, saj so bile raztopine v sat naknadno dodane, stanje satne celice in njegovo število ter izračunan ISSC vsake snovi ob določenem času. Siva barva označuje snovi, ki sta bili v sat dodani po 1h 20 min od pričetka poskusa, roza barva pa snovi, ki sta bili po 2h 40 min dodani zadnji. Čas vpogleda satnih c. Vbrizgana snov Odprta (izpr.) Odprta (polna) Delno odprta V odp. Nespr. V zap. Zaprta INDEKS 0:40 h 1:20 h 2:40 h 3:40 h Naslednji dan L 5 3 0,688 V ,188 M 3 5-0,344 L 8 1 V ,563 M ,719 V ,438 O ,406 L 8 1 V ,406 M ,844 V ,594 O ,719 V ,156 E ,375 L 8 1 V ,063 M ,375 V 4 4 0,125 O ,125 V 2 6 0,500 E ,188
69 58 V našem zadnjem, tretjem satu, pa smo začeli satne celice najprej polniti z raztopino ocetne kisline skupaj z obema kontrolama in naredili v času 1h 20 min dva vpogleda, nato pa smo zraven dodali etanolno raztopino skupaj z vodo kot kontrolo, čez 2h 40 min pa še raztopino mlečne kisline, prav tako z vodo kot kontrolo. Na grafikonu (Slika 23) so prikazani rezultati prvega vpogleda ter rezultati naslednjega dne prve naknadno dodane raztopine, ki je bila v tem primeru 2% raztopina etanola. Pri prvem vpogledu snovi vidimo razliko med satnimi celicami kontrole ter celicami z etanolno raztopino. Pri prvih je bilo nekaj zaprtih, večinoma pa so bile nespremenjene (N=5), druge celice pa so začele čebele malo odpirati. Naslednji dan so vse satne celice s kontrolo zaprle, saj je ISSC enak 1. Prav tako so zapirale satne celice z etanolno raztopino, zabeležili smo 6 zaprtih satnih celic, 1 delno ter 1 popolnoma odprto satno celico (Preglednica 7), kar je skupaj botrovalo nekoliko nižjemu ISSC-ju v primerjavi s kontrolo. 1 0,75 0,5 0,25 Indeks stanja satnih celic 0 Prvi vpogled snovi Naslednji dan Voda Etanol -0,25-0,5-0,75-1 Čas Slika 23: Indeks stanja satnih celic z vbrizgano 2% raztopino etanola glede na kontrolo po 1h 20 min (prvi vpogled snovi) ter naslednji dan.
70 SAT 3 Puhalić, N. Etanol, ocetna in mlečna kislina kot ključni dražljaji za predelavo hrane v čebelji družini. 59 Preglednica 7: Prikaz števila različnih stanj satnih celic s snovmi glede na čas v tretjem satu, kamor je bila na začetku dodana raztopina ocetne kisline. Zajema čas vpogleda satnih celic, saj so bile raztopine v sat naknadno dodane, stanje satne celice in njegovo število ter izračunan ISSC vsake snovi ob določenem času. Siva barva označuje snovi, ki sta bili v sat dodani po 1h 20 min od pričetka poskusa, roza barva pa snovi, ki sta bili po 2h 40 min dodani zadnji. Čas vpogleda satnih c. Vbrizgana snov Odprta (izpr.) Odprta (polna) Delno odprta V odp. Nespr. V zap. Zaprta INDEKS 0:40 h 1:20 h 2:40 h 3:40 h Naslednji dan L 8 0 V ,375 O ,313 L ,031 V ,594 O ,594 V 5 3 0,375 E 2 6-0,188 L ,031 V 4 4-0,625 O ,688 V ,063 E ,063 V M L 4 4 0,125 V ,094 O ,250 V 8 1 E ,594 V 1 7 0,875 M 3 5 0,344
71 Preverjanje vpliva mehanskih poškodb satnih celic v panju Iz spodnje preglednice (Preglednica 8) je razvidno, da so čebele skoraj vse satne celice z vodo zaprle (N=15), zabeležili smo le eno delno odprto satno celico. Pri etanolni raztopini je bila vrednost negativnega in pozitivnega ISSC-ja enaka, zato je bil tudi skupni indeks 0 (Slika 24). Čebele so tukaj različno odreagirale, število odprtih in zaprtih satnih celic je bilo enako (Preglednica 8). Pri satnih celicah z raztopino mlečne in ocetne kisline je bilo stanje podobno kot pri vodi, saj s histograma razberemo, da je skupni indeks pozitiven, kar pomeni, da so čebele večino satnih celic zaprle (Slika 24). Pri raztopini mlečne kisline je bilo zabeleženih nekoliko manj zaprtih celic v primerjavi s tistimi z raztopino ocetne kisline (Preglednica 8), pri kateri je bil izračunan skoraj 2x višji skupni ISSC (Slika 24). Med posameznimi luknjicami različnih velikosti so opazne velike razlike. Majhne luknjice so čebele zapirale, pri srednje velikih luknjicah je bilo stanje spremenljivo, saj vidimo tako odpiranje kot zapiranje, vendar je skupni indeks pozitiven, torej je bilo za malenkost več zaprtih luknjic te velikosti. Vse velike luknjice pa so čebele prepričljivo odprle (ISSC= -1) (Preglednica 9, Slika 24). Preglednica 8: Prikaz števila različnih stanj satnih celic po eni uri pri satnih celicah z vbrizgano vodo in posamezno testno raztopino. Vrsta raztopine Odprta (izpr.) Odprta (polna) Stanje satne celice Delno odprta V odp. Nespr. V zap. Zaprta SKUPNI INDEKS V ,906 E M ,391 O ,688 Preglednica 9: Prikaz števila različnih stanj satnih celic po eni uri pri različno velikih luknjicah. Velikost luknjice Odprta (izpr.) Odprta (polna) Stanje satne celice Delno odprta V odp. Nespr. V zap. Zaprta SKUPNI INDEKS Majhna ,703 Srednja ,172 Velika 16-1
72 61 1 Raztopine Luknjice 0,75 0,5 0,25 Indeks stanja satnih celic 0-0,25 V E M O Majhna Srednja Velika -0,5-0,75-1 Slika 24: Indeks stanja satnih celic z vbrizganimi raztopinami v primerjavi z različno velikimi luknjicami. Najtemneje obarvan stolpec pri vsaki snovi predstavlja odprte satne celice oz. negativni ISSC, najsvetleje obarvan stolpec zaprte satne celice oz. pozitivni ISSC, vmesni stolpec pa seštevek pozitivnega in negativnega ISSC-ja oz. skupni ISSC. Opažene frekvence naših tretmanov (Preglednica 10) smo uporabili za njihovo medsebojno primerjavo z χ2 testom (Preglednica 11). Predvsem smo se osredotočili na odpiranje satnih celic in v zvezi s tem ugotavljali prisotnost korelacije med satnimi celicami z etanolno raztopino, ki so jih čebele dokazano odpirale, ter med ostalimi tretmani. Rezultati kažejo (Preglednica 11), da so višji χ2 in s tem statistično značilne razlike prisotne med E in V (satne celice z etanolno raztopino in satne celice z vodo), kar je bilo pričakovati glede na izračunano vrednost ISSC-ja vode (0,906). Prav tako obstaja korelacija med E in O ter med E in majhnimi luknjicami, kar potrjuje nizka verjetnost, saj je p 0,05. Tudi pri nekaterih ostalih tretmanih je χ2 dokazano statistično pomemben, zato smo tudi pri teh povezavah zavrnili hipotezo neodvisnosti (glej Preglednico 11). Dobljene verjetnosti, manjše od 0,001, so ponovno dokazale ekstremne razlike med velikimi luknjicami v primerjavi z majhnimi, satnimi celicami z vodo ter raztopino ocetne kisline, kjer so največje statistično značilne razlike prisotne med velikimi luknjicami in satnimi celicami z vbrizgano vodo. V tem primeru ima namreč χ2 najvišjo vrednost tj. 24,596.
73 62 Preglednica 10: Porazdelitev frekvenc satnih celic po tretmanih glede na odpiranje. RAZTOPINE LUKNJICE Nespremenjena in do odprtja Zaprta in v zapiranju V 1 15 E 11 5 M 6 10 O 4 12 Majhna 4 12 Srednja 11 5 Velika 16 0 Preglednica 11: Navzkrižni diagram izračunanih χ2 testov. Odebeljeni izračuni prikazujejo statistično značilne razlike med dvema tretmanoma. Črno obarvano polje pomeni, da je p (verjetnost) teh dveh tretmanov manjši ali enak 0,001, pri črtastem polju pa je p večji od 0,001 in manjši ali enak 0,05. V E M O Majhna Srednja Velika V X E χ2=10,8 p=0,001 X M χ2=2,926 p=0,087 χ2=2,008 p=0,156 X O χ2=0,948 p=0,330 χ2=4,518 p=0,034 χ2=0,145 p=0,703 X Majhna χ2=0,948 p=0,330 χ2=4,518 p=0,034 χ2=0,145 p=0,703 χ2=0 p=1 X Srednja χ2=10,8 p=0,001 χ2=0 p=1 χ2=2,008 p=0,156 χ2=4,518 p=0,034 χ2=4,518 p=0,034 X Velika χ2=24,596 p<0,001 χ2=3,793 p=0,051 χ2=11,782 p=0,001 χ2=16,133 p<0,001 χ2=16,133 p<0,001 χ2=3,793 p=0,051 X
74 63 5 RAZPRAVA IN SKLEPI 5.1 RAZPRAVA Naš glavni cilj raziskave je bil opredeliti vlogo etanola, ocetne in mlečne kisline pri predelavi medu v panju. Te snovi nastanejo kot posledica procesa fermentacije različnih mikroorganizmov, ki lahko v panj oz. v sam med zaidejo na različne načine. Primarni viri kontaminacije mikroorganizmov so nabrana medičina ali pelod, prebavni trakt čebel, cvetlice ali preprosto zrak in umazanija (Snowdon in Cliver, 1996) Zaznavanje nizkih koncentracij raztopin etanola, ocetne in mlečne kisline V prvem delu naše raziskave smo testirali sposobnost zaznavanja nizkih koncentracij naših testnih raztopin. Ker težko napovemo motivacijo čebel za hranjenje v panju, je test bolje izvajati toliko časa, dokler čebele ne spijejo skoraj celotne kontrolne raztopine kot pa že vnaprej določiti čas pitja (primerjaj Sliki 8 in 9). Od vsega ponujenega so pričakovano spile največ kontrolne raztopine. Opažena variabilnost med ponovitvami poskusov je verjetno posledica drugačne izpostavljenosti posameznih lončkov z raztopinami čebelam na različnih mestih v panju. Testiranja z etanolno raztopino so bila že narejena in tudi zanje so prišli do podobnih rezultatov, da čebele pijejo raje sladkorno raztopino z nižjim odstotkom tega alkohola (Abramson in sod., 2004). Razlog za to, da so čebele pile raje nižje koncentracije naših testnih raztopin, bi lahko pripisali temu, da so vse te snovi, prav tako v nizkih koncentracijah, naravno prisotne v njihovem življenjskem okolju. Višje koncentracije teh snovi verjetno delujejo nanje že kot dražeči oz. odbijajoči dražljaji. Merilo za uspešno učenje je povezava pogojnega dražljaja z nepogojnim. Dokazali smo, da čebel ni mogoče učiti z raztopino etanola (2%), ocetne (5%) in mlečne kisline (5%), to pomeni, da v tem primeru čebele niso uspešno povezale pogojnega dražljaja z nepogojnim ter niso dojele razlike med A in B dražljajem. To bi pripisali dejstvu, da so tako etanol, ocetna kot mlečna kislina za čebele ključni dražljaji v panju, saj se čebele s temi snovmi neprestano srečujejo, prisotne so tako v medu kot v cvetnem prahu (mlečna kislina). Mikroorganizmi v panju za svoje delovanje in rast izkoriščajo proces fermentacije, pri tem pa nastajajo tudi vsi ti fermentacijski produkti. Čebele tako te snovi uporabljajo kot ključne prehranske dražljaje, saj je bilo učenje s temi snovmi neuspešno, vse skupaj pa dodatno utemeljujemo tudi z uspešno izvedenim pogojevanjem z eteričnim oljem sivke (Sliki 16 in 17). Pri učenju s to snovjo se je vedno bolj večal pogojni odziv, upadal pa odziv na kontrolo. Čebele prihajajo v stik z vonjem sivke tudi v naravi in jim predstavlja pomemben signal za vir hrane. Dobra nagrada pa je potrebna izkušnja, da se čebela nekaj nauči in to ohrani v spominu. Čebele si torej ta vonj v naravi, poleg barve in oblike cvetu, zapomnijo in informacije o paši posredujejo ostalim čebelam v panju (von Frisch, 1967).
75 64 Razlikovanje običajnih vonjav se pri čebelah preverja s poskusi z učenjem. S poskusi smo dokazali, da naši dražljaji pri čebelah niso izzvali učenja. Kljub temu pa bi lahko čebele te snovi med seboj še vedno razlikovale, a ne prek vonjalne zaznave. Etanol, ocetna in mlečna kislina čebelam morda ne predstavljajo vonjalnih dražljajev, vseeno pa obstaja verjetnost, da poteka ločevanje teh snovi na podlagi druge zaznavne poti, kot je okušanje. Pri okušanju ni nujno potreben neposreden stik čebele s snovjo, zaznavanje je možno tudi prek hlapov. Z vonjalnega in vizualnega vidika so čebele dobro raziskane, področje okušanja, ki je za čebele pri izbiri virov hrane ključnega pomena, pa je v veliki meri še neraziskano. Šele v zadnjih letih so, tako na vedenjski kot na elektrofiziološki ravni, opravili nekaj poskusov s čebeljimi tipalnicami, njihovimi ustnimi deli ter sprednjimi stopali, ki prestavljajo njihove pomembne kemosenzorične organe (de Brito Sanchez, 2011). Preverjali so sposobnost razlikovanja različnih snovi, sladkega, slanega in grenkega okusa. V čebeljem genomu so odkrili le 10 okušalnih receptorjev, kodiranih z receptorskimi geni za okus, v primerjavi z vinskimi mušicami vrste Drosophila melanogaster, ki imajo kar 68 okušalnih receptorjev za zaznavanje in razlikovanje snovi (de Brito Sanchez in sod., 2007). Robertson in Wanner (2006) navajata, da čebele za lociranje in prepoznavo hrane, ne potrebujejo veliko število okušalnih receptorjev, saj so rastline razvile mehanizme, s katerimi privlačijo in nagrajujejo čebele v zameno za njihovo opraševanje. Ti poskusi so tako pokazali, da so se čutnice na različnih delih telesa čebele odzvale drugače, s spremenljivo mero občutljivosti za sladkorje, soli, aminokisline, proteine in vodo (de Brito Sanchez, 2011). Čutne dlačice tipalnic so, v primerjavi s tistimi na stopalih sprednjih nog, prikazale večji odziv na sladkorno raztopino, saj je že 2,85% sladkorna raztopina izzvala PER odziv (stopalo: 34,23%), kar pojasnjuje tudi podatek, da imajo tipalnice 15 30x več okušalnih receptorjev. Tipalčne čutnice so bile pri tem poskusu celo bolj občutljive od tistih na jezičku. Čebele naj bi imele 2 receptorska gena za sladek okus, AmGr1 in AmGr2 (de Brito Sanchez, 2007, 2011). Poskusi z distalnimi deli sprednjih nog pri čebelah so prikazali velik odziv na že zelo nizke koncentracije raztopine soli KCl (0,1 mm), kar bi lahko pomenilo, da lahko te čutne dlačice vsebujejo celice za zaznavo vode, česar pri čutnicah tipalnic in ustnih delov niso odkrili. Izkazalo se je tudi, da okušalna čutnica stopala (lat. tarsus) nima receptorske celice za sladkor, medtem ko je bil odgovor čutnice stopalca (lat. pretarsus), natančneje na predelu krempeljca, 40-50x večji pri sladkorni raztopini kot pri raztopini KCl (de Brito Sanchez in sod., 2014). Grenke snovi (kinin, salicin in kofein) pri nobenem draženju niso povzročile odgovora. Pri poskusih na vedenjski ravni, in sicer pri stimulaciji z raztopino grenke snovi tako tipalnice kot stopala, so ugotovili, da grenka snov bistveno zmanjša kasnejši PER odziv na sladkorno raztopino, kar pri obratnem zaporedju dražljajev ni veljalo, prav tako pa je draženje z mešanico sladkorne raztopine in določene grenke snovi potrdilo, da slednje snovi na receptorske celice za sladkor delujejo zaviralno (de Brito Sanchez in sod., 2007, 2011, 2014).
76 65 V našem primeru bi lahko na sam potek učenja vplivalo več dejavnikov: pašna aktivnost čebel v tem obdobju in posledično sitost čebel, stanje vpete čebele (stres, utrujenost), mešanje vonjav ob nezadostnem prezračevanju prostora ter starost posamezne čebele, ki naj bi imela v času pašnega vedenja večjo sposobnost olfaktornega učenja (Ray in Ferneyhough, 1997). Odziv čebel takoj po pogojevanju je lahko posledica povečane senzitizacije, o sami povezavi med pogojnim in nepogojnim dražljajem oz. asociativnem učenju bi lahko govorili šele po izvedbi vsaj nekaj zaporednih dražljajev (Menzel, 1999). Raziskav glede učenja, tako z ocetno kot z mlečno kislino, s strani drugih nismo zasledili. Abramson in sod. (2000) pa so raziskali vpliv etanolne raztopine različnih koncentracij na sposobnost učenja čebel. Pri tem so opazovali, kolikšna je uspešnost učenja v primeru, če čebele spijejo etanolno raztopino določene koncentracije pred samim učenjem in ugotovili, da se odgovor čebel pri pitju višjih koncentracij etanolne raztopine ( 20%) vidno zmanjša. Prav tako pa so raziskali uporabo etanolne raztopine med klasičnim pogojevanjem s PER odzivom ter s tem poskusom dokazali, da se pri koncentracijah etanola, višjih od 1%, zmanjša pogojni odziv. To bi se lahko na nek način ujemalo tudi z našimi zaključki, saj smo pri učenju uporabili 2% etanolno raztopino, čeprav je šlo v našem primeru za olfaktorno pogojevanje s PER odzivom. Lahko pa potrdimo, da je bilo tudi klasično pogojevanje, ki smo ga izvedli pred to metodo, neuspešno Vpliv raztopin na predelavo medu v celicah satja v panju Pri drugem delu naše raziskave smo beležili odziv čebel ob dodatku 2% etanolne raztopine, 1% raztopine ocetne kisline in 2% raztopine mlečne kisline v celice satja v panju. Zanimalo nas je, kako etanol, ocetna in mlečna kislina kot ključni dražljaji v panju, vplivajo na predelavo medu pri čebelah. Pred vbrizganjem naših testnih raztopin v celice satja smo vsako satno celico, prekrito z voščenim pokrovcem, nekoliko predrli z žebljičkom. Rezultati prvega in drugega dne so pokazali nekaj medsebojnih razlik. Pri zadnjem poskusu smo poskušali z drugačnim načinom vbrizgavanja raztopin, in sicer z neposrednim vbrizganjem brez predhodne poškodbe satnih celic oz. voščenih pokrovcev. Želeli smo namreč preveriti tudi možnost vpliva mehanskih poškodb satnih celic na reakcijo čebel, saj smo sumili, da bi lahko velikost luknjic vplivala na naše rezultate. Da bi lahko to potrdili, smo tako pri tem zadnjem poskusu satne celice, vbrizgane z raztopinami, primerjali še z različno velikimi luknjicami. Naše domneve so se izkazale za pravilne, saj rezultati (Slika 24) kažejo, da so se čebele drugače odzvale na različno velikost luknjic. Zato smo bili mnenja, da nam je dal ta zadnji poskus najbolj točne in zanesljive rezultate, kajti le tukaj je bilo izvedeno neposredno vbrizgavanje raztopin z minimalno poškodbo satnih celic. S tem zadnjim poskusom bi bil še najbolj primerljiv poskus prvega dne, kjer smo na vsak sat vbrizgali drugačno raztopino skupaj z luknjico in vodo, ki sta predstavljali kontroli. Poskus drugega dne, kjer smo raztopine vbrizgavali naknadno, kaže največ odstopanj, razlog bi lahko bila različna velikost luknjic, ki sodeč po dobljenih rezultatih
77 66 vpliva na sam odziv čebel. Dejavnost čebel ter s tem raznolikost stanja celic satja je bilo v večini največje po 1h 20 min. Naslednji dan so bile načeloma vse satne celice zaprte oz. v stanju zapiranja, saj so čebele po tem času med že predelale. Z različnimi načini vbrizgavanja raztopin smo lahko naš problem proučili z več vidikov. Zaradi samega postopka vbrizgavanja smo tako zadnji poskus opredelili kot najbolj točen. Kar se tiče naše kontrole, 5 µl vode v satni celici, čebelam ni predstavljala posebnega dražljaja oz. možnosti za kvarjenje (Slika 24). Največja predelava medu je bila opažena pri etanolni raztopini. Različen odziv čebel na potek predelave medu ob dodatku naših raztopin bi lahko pripisali različni vlogi teh snovi v panju. Gre za fermentacijske produkte, ki so lahko posledica anaerobne ali aerobne metabolne poti različnih mikroorganizmov. Fermentacija je najpomembnejša biološka razgradnja, ki poteka v medu. Pod specifičnimi pogoji, kot so določena temperatura in vlaga, številne kvasovke iz sladkorjev v medu sintetizirajo etanol (Snowdon in Cliver, 1996). To bi bil lahko poglaviten razlog za večjo predelavo medu v satnih celicah, kjer je bila vbrizgana etanolna raztopina. Zaradi razvoja kvasovk etanol verjetno predstavlja čebelam prvi znak fermentacije ter posledično dražljaj kvarjenja medu. Zato čebele s svojimi izločki žlez in s ponovno predelavo lahko zmanjšajo koncentracijo te snovi v medu, kakor tudi ustavijo nadaljnjo aktivnost mikroorganizmov. Delež organskih kislin v medu je manjši od 0,5%, kljub temu pa te snovi pomembno prispevajo k organoleptičnim lastnostim, kot so barva in okus medu, ter določajo nekatere fizikalne in kemične lastnosti, med drugim vplivajo na njegovo kislost in električno prevodnost (Crane, 1990). Kisline so lahko pomemben indikator za botanični in geografski izvor medu. Tako se npr. koncentracija citronske kisline v medu uporablja kot zanesljiv parameter za razlikovanje cvetličnega in gozdnega medu, nižja koncentracija te kisline je znak medu cvetličnega izvora (Talpay, 1988). Glede na svoje številne lastnosti so organske kisline v medu premalo raziskane, podatka o koncentraciji ocetne kisline v medu praktično še ni. Satne celice z raztopino ocetne kisline so čebele, presenetljivo, zapirale. Sami smo bili mnenja, da bo ocetna kislina čebelam predstavljala kemični dražljaj oz. dražečo snov, ki jo bodo iz medu izločile in smo tu brez dvoma pričakovali večjo predelavo medu. Vemo tudi, da čebelarji raztopino ocetne kisline uporabljajo pri odganjanju čebel. Vendar so bile vbrizgane koncentracije naših raztopin nizke, saj smo se s tem želeli približati naravnim koncentracijam teh snovi v medu. Zato bi lahko njihov odziv oz. dejanje pripisali drugemu faktorju. Znano je, da sta glavna produkta alkoholne fermentacije etanol in ogljikov dioksid. Nadaljnja oksidacija alkohola s pomočjo OKB pa privede do nastanka ocetne kisline, ki bi jo lahko definirali kot sekundarni produkt tega biološkega procesa. Čeprav je ocetna kislina naravno prisotna v medu, pa večje koncentracije te kisline in hkrati višja kislost medu kažejo na možnost fermentacije (Mato in sod., 2003). Lahko, da so čebele
78 67 zaznale ocetno kislino kot dražljaj kvarjenja oz. fermentacije in so z zapiranjem satnih celic preprečile nadaljnjo oksidacijo ter nastajanje ocetne kisline, saj lahko ocetnokislinska fermentacija poteka le pod aerobnimi pogoji. Kot drugi razlog za takšen odziv čebel pa bi lahko preprosto pripisali dejstvu, da je ocetna kislina končni produkt fermentacije in tudi zavira nadaljnji razvoj mikroorganizmov. Čebele so prav tako zapirale satne celice z raztopino mlečne kisline. Čeprav je tukaj nekaj več odpiranja kot pri ocetni kislini, pa skupni indeks vseeno kaže na zapiranje celic. Mlečna kislina je naravni konzervans, saj deluje baktericidno in onemogoči razvoj in delovanje mikroorganizmov (Boyer, 2005). MKB izkoriščajo sladkorje v medu in cvetnem prahu za pridobivanje energije v procesu mlečnokislinske fermentacije. Ob pomanjkanju kisika in zaradi optimalne temperature v panju začne konzerviran pelod ob prisotnosti MKB fermentirati. Pri tem nastaja mlečna kislina, ki spremeni kemično sestavo cvetnega prahu, obenem pa izboljša njegovo hranilno vrednost (Božnar, 2011). Mlečna kislina je tudi naravna sestavina medu. Tako ta snov predstavlja čebelam prehranski dražljaj, ki povzroči konzerviranje hrane oz. zapiranje satnih celic. Prav tako pa čebele z zapiranjem pripomorejo k ustvarjanju okolja brez kisika in razvoju MKB. Naše testne snovi so pri čebelah sprožile specifično vedenje, kar smo zabeležili kot odpiranje oz. zapiranje celic satja. Poskusi kažejo na to, da so prisotne razlike v zaznavi vbrizganih raztopin etanola, ocetne in mlečne kisline, a tu ne gre za naučene vzorce, ampak te snovi delujejo kot ključni dražljaji v panju. O mehanizmih zaznave se na osnovi naših poskusov ne bi dalo sklepati Uporabnost rezultatov za nadaljnje raziskave Poskuse z vbrizgavanjem raztopin etanola, ocetne in mlečne kisline bi bilo potrebno še bolj raziskati in pri tem predvsem paziti na velikost luknjic ob vbrizgavanju, saj smo dokazali, da mehanske poškodbe celic satja vplivajo na dejanje čebel. Znano je, da pri predelavi medičine v med, čebele iz svojih žlez izločajo razne encime. Le-ti poleg tega, da pripomorejo k hitrejšemu zorenju medu, pomembno prispevajo tudi k nastajanju različnih snovi, ki določajo antimikrobne lastnosti medu. Tako se zaradi predelave poveča delež antimikrobnih snovi v medu. Z našimi poskusi smo pokazali, da je mogoče sprožiti dodatno predelavo že skladiščenega medu z mehanskimi poškodbami voščenih pokrovcev celic satja in dodajanjem etanola v celice, kar lahko spodbudi k razvoju tehnik za izboljšanje kvalitete pridelanega medu. 5.2 SKLEPI Čebele pijejo raje nižje koncentracije raztopin etanola, ocetne in mlečne kisline, saj so v panju te snovi tudi naravno prisotne v nizkih koncentracijah.
79 68 Predpostavili smo, da so čebele sposobne zaznati in razlikovati nizke koncentracije raztopin etanola, ocetne in mlečne kisline. Našo prvo hipotezo lahko le delno ovržemo, saj čebele, kljub verjetni zaznavi naših testnih raztopin, posameznih snovi med seboj ne razlikujejo kot vonjalne dražljaje, ločevanje snovi pa bi bilo vseeno možno, vendar prek druge zaznavne poti (okušanje). Razlog za neuspešno pogojevanje pa bi bil lahko preprosto ta, da so to vsakdanji ključni dražljaji v panju in se zato čebele na takšne dražljaje niso primorane naučiti. Njihov odziv na te dražljaje je nagonski. Druga hipoteza se je izkazala za pravilno, kajti raztopine etanola, ocetne in mlečne kisline različno vplivajo na odziv čebel in na samo predelavo hrane v panju. Vloga teh snovi v panju se med seboj razlikuje. Etanol v satnih celicah povzroča odpiranje satnih celic in večjo predelavo medu. Pri celicah satja z vbrizgano raztopino ocetne kisline so čebele celice zapirale. Tako etanol kot ocetna kislina naj bi bila znak za kvarjenje snovi. Zato smo tudi predvidevali, da bodo čebele ob vbrizgavanju raztopin teh dveh snovi, satne celice odpirale, a se je pri ocetni kislini presenetljivo izkazalo ravno obratno dejanje s strani čebel. Satne celice, kjer je bila vbrizgana raztopina mlečne kisline, so čebele zapirale, najverjetneje zato, ker je mlečna kislina naravni konzervans in tako čebele ob stiku s to snovjo celice nagonsko zapirajo. Glede na to, da je bilo zapiranje pri ocetni kislini celo večje kot pri mlečni kislini, lahko rečemo, da je imela tudi ocetna kislina v tem primeru lastnosti konzervansa. Voda (kontrola) v tako majhnih količinah pri čebelah ne pomeni dražljaj kvarjenja. Verjetno bi večja količina vode privedla do odpiranja celic satja, saj bi zaradi tega prišlo do razvoja kvasovk in posledično vrenja medu. Čebele bi začele takšen med ponovno gostiti. Mehanske poškodbe satnih celic vplivajo na reakcijo čebel. Velike luknjice so čebele prepričljivo odpirale (ISSC= -1), medtem ko so majhne zapirale. Majhna poškodba satne celice na čebelo nima vpliva. S pomočjo χ2 testa z Yates-ovo korekcijo smo dokazali statistično značilne razlike med posameznimi tretmani. V primerjavi s satnimi celicami z vbrizgano etanolno raztopino so čebele zaprle največ satnih celic z vodo (χ2=10,8; p=0,001). Zaradi vpliva mehanskih poškodb celic satja na čebele bi morali biti v prihodnje bolj pozorni na velikost luknjic pri vbrizgavanju raztopin, kajti le na ta način bi lahko zmanjšali verjetnost odstopanja rezultatov. Pri našem zadnjem poskusu z vbrizgavanjem raztopin bi bilo dobro, da bi naredili vsaj še dva vpogleda rezultatov.
80 69 6 POVZETEK Pašne čebele nabrano medičino s cvetov odnašajo v panj in jo predajo panjskim čebelam, ki le-to odlagajo v celice satja. Nato jo pričnejo zgoščevati, saj začetna medičina vsebuje veliko vode. Preden med dozori in preden čebele pokrijejo satno celico z voščenim pokrovcem, pa je zgornji del vsake celice z medom izpostavljen različnim dejavnikom v panju, kot so toplota, vlažnost ter prisotnost kisika. Takšni pogoji predstavljajo optimalno okolje za različne mikroorganizme, ki jih lahko čebele prenesejo v panj z nabrano medičino ali cvetnim prahom, lahko pa izvirajo tudi iz čebelje mikroflore (Snowdon in Cliver, 1996; Anderson in sod., 2011). Mikroorganizmi pri presnovi sladkorjev, tako tistih v medu kot v cvetnem prahu, izločajo encime in povzročijo fermentacijo ter s tem nastanek različnih metabolitov. Kvasovke povzročajo alkoholno fermentacijo sladkorjev do etanola in ogljikovega dioksida, nadaljnja fermentacija ob prisotnosti ocetnokislinskih bakterij privede do nastanka ocetne kisline (Berg in sod., 2007). Tudi cvetni prah zaradi posebnega shranjevanja v satnih celicah ob prisotnosti mlečnokislinskih bakterij kmalu fermentira, tu nastaja mlečna kislina (Božnar, 2011). Tako so etanol, ocetna in mlečna kislina fermentacijski produkti in ključni dražljaji za predelavo hrane v čebelji družini. Našo raziskavo smo razdelili na dva dela. V prvem delu smo najprej preverili, katere koncentracije raztopin ocetne in mlečne kisline čebele sploh še pijejo in ali so zmožne zaznati ter razlikovati nizke koncentracije raztopin etanola, ocetne in mlečne kisline, drugi del raziskave pa je bil namenjen opazovanju vpliva določenih koncentracij raztopin teh snovi pri predelavi hrane/medu v panju. Za pitje raztopin smo pripravili 10 krmilnikov (2 x kontrola z vodo, 2 x 2% ocetna kislina, 2 x 5% ocetna kislina, 2 x 2% mlečna kislina, 2 x 5% mlečna kislina), ki smo jih naredili iz 10 mililitrskih lončkov, filtrirnih papirčkov ter zgornjih delov petrijevk. Poskusa z etanolno raztopino nam ni bilo potrebno narediti, saj so testiranja s to raztopino že narejena in so tako koncentracije raztopine etanola, ki jo čebele še zaužijejo, že določene (Abramson in sod., 2000). Pripravljene krmilnike za pitje raztopin smo postavili v panj, pred tem pa smo posamezne dele ter tudi vsako raztopino določene koncentracije stehtali. Dokazali smo (Slika 8 in 9), da čebele pijejo raje nižje koncentracije raztopin ocetne in mlečne kisline, kar bi lahko pripisali dejstvu, da so prav nizke koncentracije teh snovi tudi naravno prisotne v panju. Ko smo ugotovili, da čebele zaznajo nizke koncentracije raztopin etanola, ocetne in mlečne kisline in določili koncentracije teh raztopin, ki jih čebele še pijejo, smo želeli ugotovili ali so sposobne še razlikovanja teh raztopin med seboj, kar smo preverili z asociativnim učenjem čebel. Čebele smo pogojevali z 2% vodno raztopino etanola, 5% vodno raztopino ocetne kisline ter 5% vodno raztopino mlečne kisline, saj smo zaradi boljše zaznave hlapov pri učenju uporabili raje višje koncentracije testiranih raztopin. Iz ependorfk s prostornino 1,5 ml smo naredili tulce za vpenjanje čebel. Pred vhodom v panj smo v erlenmajerico
81 70 ujeli čebele in jo ob prihodu v laboratorij postavili na ledeno kopel. Vsako otrplo čebelo smo s pomočjo pincete prijeli za krila in jo dali v odrezano ependorfko ter njen zažetek med glavo in oprsjem prelepili z lepilnim trakom. Tako vpeto čebelo v tulcu smo postavili na pokrovček, pritrjen na leseni deski, ki je služil kod podstavek. Učenje smo razdelili na tri stopnje. Prva je vključevala hranjenje čebel s sladkorno raztopino ter pitje vode za potešitev žeje, pri drugi smo izvedli habituacijo, zadnja stopnja pa je bila klasično pogojevanje z določeno raztopino kot pogojnim dražljajem. Z najbolj zanesljivimi rezultati se je izkazal protokol učenja na podlagi vonjalnega pogojevanja po metodi učenja z navidezno naključnim razporedom dražljajev. Čebele (N=16) so morale pogojni dražljaj (določena raztopina) povezati z nepogojnim (sladkorna raztopina). Izkazalo se je, da čebele raztopin etanola, ocetne in mlečne kisline niso sposobne razlikovati kot vonjalne dražljaje. Pri drugem delu raziskave smo izbrali nizke koncentracije naših testnih raztopin (2% etanolno raztopino, 1% raztopino ocetne kisline ter 2% raztopino mlečne kisline), da bi se s tem čim bolj približali naravnim koncentracijam teh snovi v panju, in jih na različne načine oz. po drugačnem zaporedju vbrizgali v celice satja ter pri tem opazovali njihov vpliv na predelavo medu pri čebelah. Z zadnjim poskusom (Slika 24) smo dokazali vpliv različno velikih luknjic na odziv čebel, kjer se je izkazalo, da majhne poškodbe satnih celic nimajo vpliva na njihovo dejanje, ravno nasprotno pa je pri velikih luknjicah ISSC, ki je dosegel vrednost -1, pokazal odpiranje satnih celic. Ker smo pri tem poskusu raztopine vbrizgali neposredno brez predhodne poškodbe celic satja, velikost luknjic ni vplivala na dobljene rezultate, zato smo tudi te rezultate sprejeli kot najustreznejše. Satne celice z etanolom so čebele odpirale, pri satnih celicah z vbrizgano mlečno ter ocetno kislino pa smo zabeležili pozitiven skupni indeks, kar kaže na zapiranje satnih celic. Zapiranje je bilo izrazitejše pri celicah z raztopino ocetne kisline. Največja predelava medu je bila pri etanolni raztopini. Glede na odpiranje satnih celic smo dokazali značilne statistične razlike med E in V (p=0,001), med E in O (p=0,034) ter med satnimi celicami z vbrizgano etanolno raztopino in majhnimi luknjicami (p=0,034). χ2 test je prikazal največje razlike med velikimi luknjicami in satnimi celicami z vodo (χ2=24,596). Specifičen odziv čebel ob dodanih snoveh v celice satja je posledica različne vloge etanola, ocetne in mlečne kisline v panju, ki nastajajo pri presnovi mikroorganizmov. Etanol predstavlja čebelam znak kvarjenja, saj je primarni produkt alkoholne fermentacije. Vzrok za tolikšno zapiranje satnih celic z raztopino ocetne kisline bi pripisali dejstvu, da je ocetna kislina končni produkt fermentacije oz. da so čebele z zapiranjem poskušale ustvariti okolje brez kisika in s tem preprečiti nadaljnjo oksidacijo etanola ter nastajanje ocetne kisline. Mlečna kislina je naravni konzervans in zato deluje na čebele kot prehranski dražljaj, ki povzroči zapiranje satnih celic.
82 71 7 PRENOS PRIDOBLJENEGA ZNANJA NA POUK V OSNOVNI ŠOLI 7.1 UVRSTITEV TEME DIPLOMSKEGA DELA V UČNI NAČRT ZA OŠ Čebelarstvo ima pri nas bogato tradicijo. Ljudje smo deležni številnih čebeljih pridelkov, bistven pomen čebel pa je opraševanje rastlin, kajti 80 % kmetijskih kultur je odvisnih prav od čebeljega dela. Čebele so socialne žuželke, celoten razvoj in medsebojno sporazumevanje članov čebelje družine veljata za nekaj posebnega. Učenci se pri pouku biologije učijo o številnih organizmih in ekosistemih v katerih le-ti živijo, dojeti pa morajo odnos med živimi bitji in njihovim okoljem. Poleg tega je pomembno, da poglobijo svoja spoznanja o nujnosti varovanja narave in živih bitij v njej in tako razumejo, na kakšen način se ohranja ravnovesje v naravi oz. delovanje prehranske verige. Vsebino diplomske naloge bi vključila v izbirni predmet Čebelarstvo pri pouku biologije v 9. razredu. Izbirni predmet obsega v celoti 32 ur, mojo vsebino pa bi predelala v okviru učne teme Hrana čebel in čebelje paše, kjer učenci spoznavajo prehrano čebel, pri tem pa se poskušajo naučiti hrano za čebele pripraviti tudi sami. Glede na to, da živijo čebele v antropogenem okolju, saj je človek postal gojitelj čebel, je potrebno učence opozoriti na pomembnost vplivov postopkov človeka na življenjsko okolje čebel, to pomeni, da človek zaradi svojih koristi in želja ne začne čebele na kakršenkoli način ogrožati. Samo učno vsebino bi izvedla v sodelovanju s centrom šolskih in obšolskih dejavnosti v povezavi z njihovimi učnimi vsebinami, ki jih izvajajo na dveh lokacijah, v Arboretumu ter v Čebelarskem centru Slovenije v Lukovici. Učno vsebino bi se lahko izvedlo kot dnevno dejavnost na terenu, ki bi časovno obsegala približno 4 ure, skupaj s poukom v šoli pa 6 ur, druga alternativa bi bila uporaba ter izpeljava vsebine v povezavi s celotnim tematskim sklopom Hrana čebel in čebelje paše pri tedenskih centrih šolskih in obšolskih dejavnosti s prilagojenim programom v tem času. Seveda bi bila celotna učna vsebina izvedena skladno z vsebino in cilji iz učnega načrta. Menim, da le sam frontalen pouk ne zadostuje za razvoj kognitivnih sposobnosti učencev, zato lahko takšen način pouka v naravi, kjer učenci teorijo povežejo z vsakdanjim življenjem oz. kjer določene stvari sami vidijo in jih tudi raziskujejo, veliko doprinese k njihovemu razumevanju, znanju in pomnjenju. Izbirni predmeti, kot je tudi Čebelarstvo, omogočajo učencem nadgradnjo osnovnega naravoslovnega znanja. Prednost vsebine diplomske naloge je medpredmetna povezava biologije, predvsem s kemijo.
83 UČNA PRIPRAVA TER POTEK DELA V diplomskem delu smo opredelili vlogo etanola, ocetne in mlečne kisline pri predelavi medu v panju. Učenci bi lahko raziskali vpliv teh snovi na prehranjevanje čebel, podobno kot smo v našem prvem poskusu čebelam dali piti različne koncentracije naših testnih raztopin. Nekaj o samih snoveh naj bi učenci predelali že pri pouku kemije pri vsebinskem sklopu Kisikova družina organskih spojin. Za lažjo predstavo bi pri poskusu uporabili vsakdanjo hrano ali pijačo, ki te snovi vsebuje. Učno snov bi izpeljala v obliki projektnega učnega dela, tako da bi pouk v šoli povezala z delom na terenu. Učenci bi bili predhodno razdeljeni v skupine, vsaka skupina pa bi morala ob zaključku učne vsebine predstaviti svoje rezultate. Poskus v naravi bi bilo potrebno izvesti v spomladanskem času, najbolje v aprilu ali maju, ko paša čebel še ni tako intenzivna. UČNA PRIPRAVA Predmet: Učna tema: Cilji: Učne metode: Učne oblike: Tip učne ure: Učna sredstva: Biologija, izbirni predmet Čebelarstvo Hrana čebel in čebelje paše Učenec: spozna s čim se prehranjujejo čebele ter pomen teh snovi za njihov razvoj in delovanje spozna, kaj so nektarne in kaj manine paše ter način komuniciranja med čebelami, ki je poglaviten za uspešno pašo se nauči, kako je potrebno pripraviti hrano za čebele razume, da so etanol, ocetna in mlečna kislina snovi, ki so tudi naravno prisotne v panju oz. v medu ugotovi, da so vloge etanola, ocetne in mlečne kisline v panju različne zna našteti vsaj nekaj primerov uporabe teh snovi v čebelarstvu Razlaga, razgovor, opazovanje (terensko delo), fotografiranje, poročanje, razprava Frontalna; individualno in skupinsko delo Projektno učno delo a) učila: delovni list za učence b) pripomočki v šoli: tabla, računalnik c) pripomočki pri delu na terenu: čebele, kozarci, pokrovi, pipete, sladkor, belo vino, kis, jogurt
84 73 Literatura: Učni načrt. Program osnovna šola. Biologija [Elektronski vir]. Ljubljana : Ministrstvo za šolstvo in šport : Zavod RS za šolstvo, 2011 Učni načrt. Izbirni predmet.: program osnovnošolskega izobraževanja. Čebelarstvo [Elektronski vir]. Ljubljana: Ministrstvo za šolstvo in šport: Zavod RS za šolstvo, 2005 Center šolskih in obšolskih dejavnosti. [Elektronski vir]. (10. oktober, 2014) Učitelj pri pouku v šoli najprej preveri predznanje učencev o prehrani čebel. Nato predstavi pomen posameznih snovi v čebelji prehrani ter način shranjevanja hrane v panju. Pove, da lahko različni produkti mikroorganizmov škodujejo medu, saj povzročajo njegovo kvarjenje. Z učenci ponovi proces vrenja. Etanol, ocetna in mlečna kislina so produkti vrenja in pri delu na terenu bi učenci opazovali in beležili odziv čebel ob dodatku teh snovi v pripravljeno hrano za čebele. Učenci podajo svoje domneve o vplivu teh snovi na prehranjevanje čebel. Učitelj se z učenci pogovarja tudi o paši, tako nektarni kot manini, ter poudari pomembnost plesnega sporazumevanja, ki omogoča uspešno pašo čebelje družine. Razloži, s čim čebelarji hranijo čebele v zimskem času. Do naslednjič, ko bo potekalo terensko delo, morajo učenci pregledati literaturo in dobiti podatke o uporabi etanola, ocetne in mlečne kisline v čebelarstvu, hkrati pa obnoviti svoje znanje o vseh teh snoveh. Učitelj na terenu sprva pripravi dva krmilnika s sladkorno raztopino, s katerima poskuša čebele privaditi na umetno krmišče (Slika 25). Krmilnika naredi s pomočjo kozarca in pokrova ter ju navzdol obrnjena postavi na mizico približno 80 m daleč od panja. Med kozarec in pokrov postavi majhno paličico, ki omogoči vstop zraka v kozarec in počasno iztekanje raztopine. Na začetku pomoči filtrirne papirčke v sladkorno raztopino ter odide do panja po čebele, saj s tem privabi njihovo zanimanje za pašo. Učenci delo učitelja opazujejo, vsaka skupina skuša pripraviti dva krmilnika. Prvi mora biti kontrola (samo sladkorna raztopina), v drugem kozarcu pa bi učenci v sladkorno raztopino dodali še določeno snov. Uporabili bi vodne raztopine belega vina (etanol), kisa (ocetna kislina) ter jogurta (mlečna kislina). Učenci bi opazovali odziv čebel ob stiku z določeno snovjo ter beležili število čebel, ki se vrača na pašo oz. število čebel na umetnem krmišču. Delež posamezne snovi v sladkorni raztopini bi čez določen čas ( približno vsakih 20 min) povečali in ponovno beležili rezultate, dokler ne bi čebele prenehale obiskovati krmišča. Učenci bi bili razdeljeni v tri skupine, saj bi vsaka skupina opazovala svojo snov. Rezultate bi si zabeležili na delovni list (Priloga B), skupaj z ostalimi učenci pa bi na koncu svoje zaključke med seboj tudi primerjali.
85 74 Projektno delo se zaključi s predstavitvijo rezultatov vseh treh skupin, učenci lahko izdelajo plakat, predstavitev s pomočjo Power Pointa ali pa predstavijo rezultate na nek svoj način, ki naj bo čim bolj izviren. Učenci morajo glede na dobljene rezultate podati tudi sklepe, saj na tak način prebudimo aktivno razmišljanje učencev. Učitelj podkrepi njihove ugotovitve z razlago, tako učenci pridobljeno znanje na terenu povežejo še s teorijo. Potrebno je opozoriti tudi na varnost učencev pri terenskem delu, saj se učenci ves čas nahajajo v bližini čebel. Predvsem tisti učenci, ki bi bili morebiti alergični na čebelje pike, bi nujno potrebovali kakšno zaščito, v tem primeru čebelarski klobuk in primerno dolgo oblačilo. Slika 25: Pripravljeno krmišče za čebele v bližini panja.
86 75 8 VIRI Abramson C. I., Stone S. M., Ortez R. A., Luccardi A., Vann K. L., Hanig K. D., Rice J The Development of an Ethanol Model Using Social Insects I: Behavior Studies of the Honey Bee (Apis mellifera L.). Alcohol Clin. Exp. Res., 24: Abramson C. I., Kandolf A., Sheridan A., Donohue D., Božič J., Meyers J. E., Benbassat D Development of an Ethanol Model Using Social Insects: III. Preferences for Ethanol Solutions. Psychological Reports, 94: Abramson C. I., Mixson T. A., Çakmak I., Wells H The use of honey bees to teach principles of learning. Uludag Bee Journal, 7: Adamič A. O., Vukmirovič V., Koch Verena Čebelji pridelki in njih uporaba. V: Moč medu. Skrt-Kos N. (ur.). Ljubljana, Založba centralnega zavoda za napredek gospodinjstva: Aethina tumida. Situazione epidemiologica. Istituto Zooprofilattico Sperimentale delle Venezie (09. nov. 2014) =article&id=1729&itemid=373 (09. nov. 2014) Ambrose, J Management for Honey Production. V: The Hive and the Honeybee. 22 th ed. Graham J. M (ed.). Hamilton, IL: Dadant & Sons: 1324 str. Ammons A. D., Hunt G. J Characterization of honey bee sensitivity to ethanol vapor and its correlation with aggression. Alcohol, 42: Anderson K. E., Sheehan T.H., Eckholm B. J., Mott B. M., DeGrandi-Hoffman G An emerging paradigm of colony health: microbial balance of the honey bee and hive (Apis mellifera). Insectes Sociaux, 58: Bacon J. S. D., Dickinson B The Origin of Melezitose: a Biochemical Relationship between the Lime Tree (Tilia spp.) and an Aphis (Eucallipterus tiliae L.). Biochem. J., 66: Baker H. G., Baker I Chemical Constituents of Nectar in Relation to Pollination Mechanisms and Phylogeny. V: Biochemical Aspects of Evolutionary Biology. Nitecki M.H. (ed.). Chicago, University of Chicago Press:
87 76 Ball D. W The Chemical Composition of honey. Journal of Chemical Education, 84, 10: Berg J. M., Tymoczko J. L., Stryer L Biochemistry. 6 th ed. 1st printing. New York, W. H. Freeman and company: 1026 str. Bogdanov S., Ruoff K., Oddo L.P Physico-chemical methods for the characterisation of unifloral honeys: a review. Apidologie, 35, Suppl. 1: S4 S17 Bokal L. (ur.), Gregori J. (ur.) Čebelarski terminološki slovar. Ljubljana, Založba ZRC SAZU: 261 str. Boyer R Temelji biokemije. Ljubljana, Študentska založba: 634 str. Božič J Nektarne paše. V: Od čebele do medu. Poklukar J. (ur.). Ljubljana, Kmečki glas: Božič J., Ambranson C.I., Bedencic M Reduced ability of ethanol drinkers for social communication in honeybees (Apis mellifera carnica Poll.). Alcohol, 38: Božnar A., Senegačnik J Med. V: Od čebele do medu. Poklukar J. (ur.). Ljubljana, Kmečki glas: Božnar A Cvetni prah. V: Slovensko čebelarstvo v tretje tisočletje 2. Zdešar P. (ur.). Lukovica, Čebelarska zveza Slovenije: Braun G., Bicker G Habituation of an appetitive reflex in the honeybee. J. Neurophysiol., 67, 3: Comi G., Beretta G., Traldi C Microbial spoilage of honey. Ristorazione Collettiva, 7: Crane E Bees and beekeeping. Science, Practice and World Resources. Oxford, U.K., Cornell University Press: 640 str. Crotti E., Rizzi A., Chouaia B., Ricci I., Favia G., Alma A., Sacchi L., Bourtzis K., Mandrioli M., Cherif A., Bandi C., Daffonchio D Acetic Acid Bacteria, Newly Emerging Symbionts of Insects. Appl. Environ. Microbiol., 76, 21:
88 77 de Brito Sanchez M. G., Ramalho Ortigao-Farias J., Gauthier M., Liu F., Giurfa M Taste perception in honeybees: just a taste of honey?. Arthropod-Plant Interactions, 1: de Brito Sanchez M. G Taste Perception in Honey Bees. Chem. Senses, 36, 8: de Brito Sanchez M. G., Lorenzo E., Su S., Liu F., Zhan Y., Giurfa M The tarsal taste of honey bees: behavioral and electrophysiological analyses. Front. Behav. Neurosci., 8, 25: 1 16 de Vuyst L., Vandamme E. J Bacteriocins of lactic acid bacteria: microbiology, genetics and applications. Oxford, UK: Blackie Academic and Professional: 539 str. Duisberg H Honey and Unspoiled Honey. Handb, Lebensmittelchem, 5: Fries I., Feng F., da Silva A., Slemenda S. B., Pieniazek N. J., Nosema ceranae n.sp. (Microspora, Nosematidae), morphological and molecular characterization of a Microsporidian parasite of the Asian honey bee Apis cerana (Hymenoptera, Apidae). Eur. J. Protistol, 32: Ghaffar T., Irshad M., Anwar Z., Aqil T., Zulifqar Z., Tariq A., Kamran M., Ehsan N., Mehmood S Recent trends in lactic acid biotechnology: A brief review on production to purification. Journal of Radiation Research and Applied Sciences xxx: 1 8 Giancola P. R Executive functioning and alcohol-related aggression. Journal of Abnormal Psychology, 113: Gilman S. E., Abraham H. D A longitudinal study of the order of onset of alcohol dependence and major depression. Drug and Alcohol Dependence, 63: Giurfa M., Malun D Associative Mechanosensory Conditioning of the Proboscis Extension Reflex in Honeybees. Cold Spring Harbor Laboratory Press, 11: Giurfa M Behavioral and neural analysis of associative learning in the honeybee: a taste from the magic well. J. Comp. Physiol. A., 193:
89 78 Golob T., Jamnik M., Kropf U., Bertoncelj J., Kandolf A Fizikalno-kemijski parametri ter senzorične in mikroskopske značilnosti slovenskega medu. V: Med: značilnosti slovenskega medu. Kandolf A. (ur.). Brdo pri Lukovici, Čebelarska zveza Slovenije: Gregorc A Zgradba in delovanje čebeljega telesa. V: Od čebele do medu. Poklukar J. (ur.). Ljubljana, Kmečki glas: Gregori J Panjski Hrošč vse večja grožnja. V: Slovenski čebelar. Zveza čebelarskih društev Slovenije, 106, 12: Higes M., Martín R., Meana A Nosema ceranae, a new microsporidian parasite in honeybees in Europe. Journal of Invertebrate Pathology, 92: Huidobro J. F., Estrella Rea M., Branquinho de Andrade P. C., Sánchez M. P., Teresa Sancho M., Muniategui S., Simal-Lozano J Enzymatic Determination of Primary Normal Alcohols as Apparent Ethanol Content in Honey. J. Agric. Food Chem., 42: Imdorf A., Charriere J. D., Maquelin C., Kilchenmann V., Bachofen B Alternative varroa control. Am. Bee J., 136: Javornik F., Kastelic L., Kranjc A., Mihelič J., Senegačnik E., Senegačnik J., Vidmar U Čebelarstvo. Ljubljana, Kmečki glas: 377 str. Jenko-Rogelj M., Strmole B Bolezni čebel. V: Od čebele do medu. Poklukar J. (ur.). Ljubljana, Kmečki glas: Kasenburger P Vsebnost sladkorjev ter prostih in skupnih kislin v različnih vrstah slovenskega medu. Diplomsko delo. Ljubljana, Biotehniška fakulteta, Oddelek za živilstvo: 73. str Kmecl V Kakovost slovenskega medu. Ljubljana, Kmetijski inštitut Slovenije: 23 str. Kompare A., Stražišar M., Vec T., Dogša I., Jaušovec N., Curk J Psihologija: spoznanja in dileme. 1. izd., 1. natis. Ljubljana, DZS: 414 str. Kornhauser A Organska kemija II. 9. izd. Ljubljana, DZS: 215 str.
90 79 Kraus B., Berg S Effect of a lactic acid treatment during winter in temperature climate upon Varroa jacobsoni Oud. and the bee (Apis mellifera L.) colony. Exp. Appl. Acarol., 18: Kubicek C. P., Karaffa L Organic acids. V: Basic biotehnology. 3 th ed. Ratledge C., Kristiansen B. (eds.). Cambridge, Cambridge University Press: Kwakman P. H. S., Te Velde A. A., De Boer L., Speijer D., Vandenbroucke-Grauls C. M. J. E., Zaat S. A. J How honey kills bacteria. The FASEB Journal, 24: Lindsay D., von Holy A Bacterial biofilms within the clinical setting: what healthcare professionals should know. Journal of Hospital Infection, 64: Mato I., Huidobro J. F., Simal-Lozano J., Sancho M. T Significance of Nonaromatic Organic Acids in Honey. Journal of Food Protection, 66, 12: Mayer J Dileme ob krmljenju čebel. V: Slovenski čebelar. Zveza čebelarskih društev Slovenije, 82, 12: 439 Meglič M Čebelji pridelki: pridobivanje in trženje. 1. izd. Brdo pri Lukovici, Čebelarska zveza Slovenije: 96 str. Meglič M., Auguštin V Varoja, čebela, čebelar. 1. izd. Lukovica, Čebelarska zveza Slovenije: 182 str. Menzel R Memory dynamics in the honeybee. J. Comp. Physiol. A., 185: Menzel R., Giurfa M Cognitive architecture of a mini-brain: the honeybee. Trends in Cognitive Sciences, 5, 2: Mustard J. A., Edgar E. A., Mazade R. E., Wu C., Lillvis J. L., Wright G. A Acute ethanol ingestion impairs appetitive olfactory learning and odor discrimination in the honey bee. Neurobiology of Learning and Memory, 90, 4: Nozal M. J., Bernal J. L., Toribio L., Alamo M., Diego J. C The Use of Carbohydrate Profiles and Chemometrics in the Characterization of Natural Honeys of Identical Geographical Origin. J. Agric. Food Chem., 53:
91 80 Olofsson T. C., Vásquez A Detection and Identification of a Novel Lactic Acid Bacterial Flora Within the Honey Stomach of the Honeybee Apis mellifera. Curr. Microbiol., 57: Paxton R. J., Klee J., Korpela S., Fries I Nosema ceranae has infected Apis mellifera in Europe sinceat least 1998 and may be more virulent than Nosema apis. Apidologie, 38: Perpar M Organska kemija. Ljubljana, DZS: 414 str. Plut S. Med Čebelarska zveza Slovenije. (08. jun. 2014) Ray S., Ferneyhough B The effects of age on olfactory learning and memory in the honey bee Apis mellifera. Neuroreport, 8,3: Rihar J Cvetni prah. V: Od čebele do medu. Poklukar J. (ur.). Ljubljana, Kmečki glas: Rixner W., Wegner G Kemija u službi čovjeka. Zagreb, Mladost: 324 str. Robertson H. M., Wanner K. W The chemoreceptor superfamily in the honey bee, Apis mellifera: expansion of the odorant, but not gustatory, receptor family. Genome Res., 16: Russell K. M., Molan P. C., Wilkins A. L., Holland P. T Identification of some antibacterial constituents of New Zealand manuka honey. J. Agric. Food Chem., 38: Schäfer M. O., Ritter W., Pettis J. S., Teal P. E. A., Neumann P Effects of organic acid treatments on small hive beetles, Aethina tumida, and the associated yeast Kodamaea ohmeri. J. Pest. Sci., 82: Seeley, T. D The tremble dance of the honey bee: message and meanings. Behav. Ecol. Sociobiol., 31: Sengun I. Y., Karabiyikli S Importance of acetic acid bacteria in food industry. Food control, 22:
92 81 Sestanek mali panjski hrošč Čebelarska zveza Slovenije (15. okt. 2014) (09. nov. 2014) Snowdon J. A., Cliver D. O Microorganisms in honey. Int. J. Food Microbiology, 31: 1 26 Solomons T. W. G., Fryhle C. B Organic chemistry. 9 th ed. Hoboken (NJ), John Wiley and company: 1191 str. Stinson E. E., Subers M. H., Petty J., White J. W. Jr The composition of honey. V. Separation and identification of the organic acids. Archives of Biochemistry and Biophysics, 89, 1: 6 12 Stušek P Celica: učbenik za strokovne in tehniške gimnazije. 1. izd., 1.natis. Ljubljana, DZS: 132 str. Suárez-Luque S., Mato I., Huidobro J. F., Simal-Lozano J., Sancho T Rapid determination of minority organic acids in honey by high-performance liquid cromatography. Journal of Cromatography A, 955: Šešek F Blagoznanstvo s tehnologijo za kadre v blagovnem prometu. 1. del. 7. izd. Ljubljana, DZS: 442 str. Talpay B Inhaltsstoffe des Honigs-Citronensäure (Citrat). Dtsch. Lebensm.- Rundsch, 84, 2: Taormina P. J., Niemira B. A., Beuchat L. R Inhibitory activity of honey against foodborne pathogens as influenced by the presence of hydrogen peroxide and level of antioxidant power. Int. J. Food Microbiol., 69: von Frisch K The Dance Language and Orientation of Bees. Cambridge, Massachusetts, London, Harvard University Press: Wang Z., Yan M., Chen X., Li D., Qin L., Li Z., Yao J., Liang X Mixed culture of Saccharomyces cerevisiae and Acetobacterpasteurianus for acetic acid production. Biochemical Engineering Journal, 79: White J. W. Jr Composition of honey. V: Honey: a comprehensive survey. Crane E. (ed.). London, Heinemann:
93 82 White J. W. Jr Honey. V: Advances in Food Research. New York, Academic Press, 24: 287 str. White J. W. Jr., Landis Doner W Honey composition and properties. Beekeeping in the United States, Agriculture handbook number 335: Winston M. L The Biology of the Honey Bee. Cambridge, Harvard University Press: 281 str.
94 ZAHVALA Velika zahvala gre mentorju prof. dr. Janku Božiču za vso strokovno in praktično pomoč, posredovano znanje, koristne nasvete, pomoč pri statistični obdelavi podatkov ter za prikaz povsem drugačnega, čudovitega sveta sveta čebel. Iskreno se zahvaljujem doc. dr. Gregorju Belušiču za vso pomoč, vloženi trud in popravke diplomskega dela, prav tako gre zahvala tudi prof. dr. Ivanu Kosu za končni pregled in potrditev diplomskega dela. Posebna zahvala je namenjena mojim staršem, ki so mi omogočili študij in mi ves čas stali ob strani. Hvala vama za vse spodbudne besede, razumevanje in potrpežljivost v času študija. Hvala bratu za vse polepšane dneve, smeh in pozitivno energijo. Zahvalila bi se mojemu dragemu Roku za neizmerno ljubezen in podporo tekom študija. Hvala tudi za pomoč in vztrajnost pri oblikovanju grafov. Hvala vsem prijateljicam in prijateljem, ki so mi popestrili študentske dni Prelepi trenutki z vami ne bodo nikoli pozabljeni. Our treasure lies in the beehive of our knowledge. We are perpetually on the way thither, being by nature winged insects and honey gatherers of the mind. Friedrich Nietzsche
95 PRILOGE Priloga A: Volumen popitih raztopin dne ,5 2 V (ml) 1,5 1 0,5 0 KONTROLA 2 % MLEČNA K. 5 % MLEČNA K. Vrsta raztopine 2 % OCETNA K. 5 % OCETNA K. Prvi stolpec pri posamezni raztopini predstavlja prvi lonček, drugi stolpec pa drugi. Vsi lončki so bili v panj dodani ob istem času.
Slika 1: Vzorci zemlje
 DELOVNI LIST INŠTITUT HAIDEGG Inštitut Haidegg je inštitut za raziskavo zemlje oz. tal. Bili so prvi, ki so leta 1987 pričeli z raziskavami. Od leta 2006 jemljejo vzorce na 1000 različnih mestih po Avstriji.
DELOVNI LIST INŠTITUT HAIDEGG Inštitut Haidegg je inštitut za raziskavo zemlje oz. tal. Bili so prvi, ki so leta 1987 pričeli z raziskavami. Od leta 2006 jemljejo vzorce na 1000 različnih mestih po Avstriji.
PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND. Pirjo-Liisa PENTTILÄ 1
 Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 28-33 Zreče, 4. 6. marec 2003 PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND Pirjo-Liisa PENTTILÄ 1 Ministry of
Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 28-33 Zreče, 4. 6. marec 2003 PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND Pirjo-Liisa PENTTILÄ 1 Ministry of
GINKGO BILOBA IN MISELNE SPOSOBNOSTI. Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015
 GINKGO BILOBA IN MISELNE SPOSOBNOSTI Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015 KLINIČNO VPRAŠANJE Ali uporaba standardiziranih pripravkov Ginkgo bilobe izboljšuje
GINKGO BILOBA IN MISELNE SPOSOBNOSTI Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015 KLINIČNO VPRAŠANJE Ali uporaba standardiziranih pripravkov Ginkgo bilobe izboljšuje
NUTRIENT INTAKE VARIABILITY INDUCED BY PROCESSING OF FOOD DIARY DATA: A PILOT STUDY
 COBISS: 1.01 Agris category code: S40, Q04 NUTRIENT INTAKE VARIABILITY INDUCED BY PROCESSING OF FOOD DIARY DATA: A PILOT STUDY Tamara PUŠ 1, Ksenija PODGRAJŠEK 2, Marjan SIMČIČ 3 Received October 10, 2012;
COBISS: 1.01 Agris category code: S40, Q04 NUTRIENT INTAKE VARIABILITY INDUCED BY PROCESSING OF FOOD DIARY DATA: A PILOT STUDY Tamara PUŠ 1, Ksenija PODGRAJŠEK 2, Marjan SIMČIČ 3 Received October 10, 2012;
ANALIZA MIKROBIOTE CVETNEGA PRAHU SKLADIŠČENEGA V SATNIH CELICAH V PANJIH KRANJSKE ČEBELE (Apis mellifera carnica Pollman)
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ MIKROBIOLOGIJE Mojca SEKIRNIK ANALIZA MIKROBIOTE CVETNEGA PRAHU SKLADIŠČENEGA V SATNIH CELICAH V PANJIH KRANJSKE ČEBELE (Apis mellifera carnica Pollman)
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ MIKROBIOLOGIJE Mojca SEKIRNIK ANALIZA MIKROBIOTE CVETNEGA PRAHU SKLADIŠČENEGA V SATNIH CELICAH V PANJIH KRANJSKE ČEBELE (Apis mellifera carnica Pollman)
KARAKTERIZACIJA MANJ ZNANIH VRST SLOVENSKEGA MEDU
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Katja STANKOVIČ KARAKTERIZACIJA MANJ ZNANIH VRST SLOVENSKEGA MEDU MAGISTRSKO DELO Magistrski študij 2. stopnja Živilstvo Ljubljana, 2016
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Katja STANKOVIČ KARAKTERIZACIJA MANJ ZNANIH VRST SLOVENSKEGA MEDU MAGISTRSKO DELO Magistrski študij 2. stopnja Živilstvo Ljubljana, 2016
Fiksacija dušika nitrogenaza
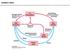 Dušikov ciklus Fiksacija dušika Ključna stopnja kroženja dušika je fiksacija N 2 iz atmosfere, ki jo katalizirajo nekatere bakterije, npr. talne bakterije iz rodov Rhizobia in Franka, ki živijo v simbiozi
Dušikov ciklus Fiksacija dušika Ključna stopnja kroženja dušika je fiksacija N 2 iz atmosfere, ki jo katalizirajo nekatere bakterije, npr. talne bakterije iz rodov Rhizobia in Franka, ki živijo v simbiozi
Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond s strength
 RMZ Materials and Geoenvironment, Vol. 55, No. 2, pp. 191-197, 2008 191 Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond
RMZ Materials and Geoenvironment, Vol. 55, No. 2, pp. 191-197, 2008 191 Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond
PROIZVODNJA OCETNE KISLINE*
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŽIVILSKA TEHNOLOGIJA PROIZVODNJA OCETNE KISLINE* Janez Zaviršek, Kristina Zidar, Veronika Zubin, Vesna Zupančič (študentje tretjega letnika študija Živilske tehnologije)
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŽIVILSKA TEHNOLOGIJA PROIZVODNJA OCETNE KISLINE* Janez Zaviršek, Kristina Zidar, Veronika Zubin, Vesna Zupančič (študentje tretjega letnika študija Živilske tehnologije)
Pripravki levkocitov. Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana
 Pripravki levkocitov Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana Razdelitev levkocitov Granulociti polimorfonuklearni levkociti Nevtrofilci Bazofilci Eozinofilci Agranulociti
Pripravki levkocitov Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana Razdelitev levkocitov Granulociti polimorfonuklearni levkociti Nevtrofilci Bazofilci Eozinofilci Agranulociti
Celični razdelki in transport proteinov
 Celični razdelki in transport proteinov Kompartmentalizacija celic Kompartmentalizacija celic Kompartmentalizacija celic Celične membrane Glavni celični organeli Evolucijski izvor topologije celic Topology
Celični razdelki in transport proteinov Kompartmentalizacija celic Kompartmentalizacija celic Kompartmentalizacija celic Celične membrane Glavni celični organeli Evolucijski izvor topologije celic Topology
MORTALITY OF Myzus persicae DEPENDING ON THE COMPONENTS OF SPRAY LIQUIDS ABSTRACT
 Zbornik predavanj in referatov 8. slovenskega posvetovanja o varstvu rastlin 267 Radenci, 6. 7. marec 7 MORTALITY OF Myzus persicae DEPENDING ON THE COMPONENTS OF SPRAY LIQUIDS Zdravko PEROVIĆ 1, Dušanka
Zbornik predavanj in referatov 8. slovenskega posvetovanja o varstvu rastlin 267 Radenci, 6. 7. marec 7 MORTALITY OF Myzus persicae DEPENDING ON THE COMPONENTS OF SPRAY LIQUIDS Zdravko PEROVIĆ 1, Dušanka
ANTIOKSIDATIVNA UČINKOVITOST IN SENZORIČNA SPREJEMLJIVOST MEDU Z DODATKI
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tanja JANEŽIČ ANTIOKSIDATIVNA UČINKOVITOST IN SENZORIČNA SPREJEMLJIVOST MEDU Z DODATKI DIPLOMSKO DELO Univerzitetni študij - 1. stopnja Živilstvo
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tanja JANEŽIČ ANTIOKSIDATIVNA UČINKOVITOST IN SENZORIČNA SPREJEMLJIVOST MEDU Z DODATKI DIPLOMSKO DELO Univerzitetni študij - 1. stopnja Živilstvo
Principi PET-CT preiskave. Marko Grmek
 Principi PET-CT preiskave Marko Grmek PET-CT PET pozitronska emisijska tomografija CT računalniška tomografija Fuzijska slika Detektor sevanja - PET skener - CT naprava PET-CT preiskava Radiofarmak - 18
Principi PET-CT preiskave Marko Grmek PET-CT PET pozitronska emisijska tomografija CT računalniška tomografija Fuzijska slika Detektor sevanja - PET skener - CT naprava PET-CT preiskava Radiofarmak - 18
Profilaktično zdravljenje hemofilije. Simpozij Bayer Maj 2011
 Profilaktično zdravljenje hemofilije Simpozij Bayer Maj 2011 Treatment schedules for adult hemophilia patients Prophylaxis Regular On demand Temporarily Načini zdravljenja krvavitev pri hemofiliji Poznamo
Profilaktično zdravljenje hemofilije Simpozij Bayer Maj 2011 Treatment schedules for adult hemophilia patients Prophylaxis Regular On demand Temporarily Načini zdravljenja krvavitev pri hemofiliji Poznamo
Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases
 Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases Avtor / Author Emina Hajdinjak 1, Andrej Markota 2, Alenka Strdin Košir 2, Simona Kirbiš 2,3
Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases Avtor / Author Emina Hajdinjak 1, Andrej Markota 2, Alenka Strdin Košir 2, Simona Kirbiš 2,3
Prioritetni dejavniki tveganja v živilih. Urška Blaznik, dr. Stanislava Kirinčič, mag. Viviana Golja, Irena Veninšek Perpar
 Prioritetni dejavniki tveganja v živilih Urška Blaznik, dr. Stanislava Kirinčič, mag. Viviana Golja, Irena Veninšek Perpar Svetovni dan zdravja 2015, nacionalni posvet o varnosti živil, 7. april 2015 Zakaj
Prioritetni dejavniki tveganja v živilih Urška Blaznik, dr. Stanislava Kirinčič, mag. Viviana Golja, Irena Veninšek Perpar Svetovni dan zdravja 2015, nacionalni posvet o varnosti živil, 7. april 2015 Zakaj
Analiza preživetja. Izbrana poglavja iz biomedicinske informatike 2011/2012, LBM2. Asist. dr. Igor Locatelli, mag. farm.
 Analiza preživetja Izbrana poglavja iz biomedicinske informatike 2011/2012, LBM2 Asist. dr. Igor Locatelli, mag. farm. Ljubljana, 16. 12. 2011 Analiza preživetja Survival analysis Proučevanje (modeliranje)
Analiza preživetja Izbrana poglavja iz biomedicinske informatike 2011/2012, LBM2 Asist. dr. Igor Locatelli, mag. farm. Ljubljana, 16. 12. 2011 Analiza preživetja Survival analysis Proučevanje (modeliranje)
Antikoagulantno zdravljenje
 Antikoagulantno zdravljenje (novosti s kongresa ASH 2010) Irena Umek Bricman Oddelek za interno medicino SB Slovenj Gradec Podčetrtek, 15.04.2010 Trajanje antikoagulantne terapije Priporočila: 8th ACCP
Antikoagulantno zdravljenje (novosti s kongresa ASH 2010) Irena Umek Bricman Oddelek za interno medicino SB Slovenj Gradec Podčetrtek, 15.04.2010 Trajanje antikoagulantne terapije Priporočila: 8th ACCP
COMPARISON OF CALCULATION METHODS OF DAILY MILK YIELD, FAT AND PROTEIN CONTENTS FROM AM/PM MILKINGS ABSTRACT
 Acta agriculturae Slovenica, suplement (september 8), 195. http://aas.bf.uni-lj.si Agris category codes: L1, Q4 COBISS Code 1.8 COMPARISON OF CALCULATION METHODS OF DAILY MILK YIELD, FAT AND PROTEIN CONTENTS
Acta agriculturae Slovenica, suplement (september 8), 195. http://aas.bf.uni-lj.si Agris category codes: L1, Q4 COBISS Code 1.8 COMPARISON OF CALCULATION METHODS OF DAILY MILK YIELD, FAT AND PROTEIN CONTENTS
PROPOLIS V PREHRANSKIH DOPOLNILIH
 Projekt sofinancirata Republika Slovenija in Evropska unija iz Evropskega socialnega sklada. PROPOLIS V PREHRANSKIH DOPOLNILIH Martina Puc Jerneja Kožar Karmen Treven Mojca Korošec Propolis v prehranskih
Projekt sofinancirata Republika Slovenija in Evropska unija iz Evropskega socialnega sklada. PROPOLIS V PREHRANSKIH DOPOLNILIH Martina Puc Jerneja Kožar Karmen Treven Mojca Korošec Propolis v prehranskih
Medcelična signalizacija. Lodish 4:
 Medcelična signalizacija Lodish 4: 20.1-20.4 Šest stopenj zunajceličnega signaliziranja Sinteza signalne molekule v signalizacijski celici Sproščanje signalne molekule iz signalizacijske celice Transport
Medcelična signalizacija Lodish 4: 20.1-20.4 Šest stopenj zunajceličnega signaliziranja Sinteza signalne molekule v signalizacijski celici Sproščanje signalne molekule iz signalizacijske celice Transport
Tracheal intubation using BLOOD the airtraq FLOW for moderately difficult airways
 Vstavitev SPREMLJANJE dihalne PRETOKA cevke z V uporabo MOŽGANSKIH airtraq laringoskopa pri bolnicah ARTERIJAH z zmerno oteženo S TCD TCD MONITORING vzpostavitvijo OF dihalne CEREBRAL poti Tracheal intubation
Vstavitev SPREMLJANJE dihalne PRETOKA cevke z V uporabo MOŽGANSKIH airtraq laringoskopa pri bolnicah ARTERIJAH z zmerno oteženo S TCD TCD MONITORING vzpostavitvijo OF dihalne CEREBRAL poti Tracheal intubation
NAJVAŽNEJŠE HORMONSKE ŽLEZE
 KAJ SO HORMONI? So naravne telesne snovi, ki jih izločajo endokrine žleze in se prenašajo po krvi ter nadzorujejo mnoge procese, kot so rast, izraba energije, ravnotežje tekočin v telesu in tvorba urina.
KAJ SO HORMONI? So naravne telesne snovi, ki jih izločajo endokrine žleze in se prenašajo po krvi ter nadzorujejo mnoge procese, kot so rast, izraba energije, ravnotežje tekočin v telesu in tvorba urina.
EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND ORGANOLEPTIC TRAITS OF EGGS
 Acta agriculturae Slovenica, suplement 2 (september 2008), 129 134. http://aas.bf.uni-lj.si Agris category codes: L02, Q04 COBISS Code 1.08 EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND
Acta agriculturae Slovenica, suplement 2 (september 2008), 129 134. http://aas.bf.uni-lj.si Agris category codes: L02, Q04 COBISS Code 1.08 EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND
 VPLIV KRMLJENJA S SLADKORNIMI SIRUPI NA DOLGOŽIVOST ČEBEL (Apis mellifera carnica) Maja Ivana SMODIŠ ŠKERL 1, Mitja NAKRST 2, Aleš GREGORC 3 IZVLEČEK Za krmljenje čebeljih družin se v času pomanjkanja
VPLIV KRMLJENJA S SLADKORNIMI SIRUPI NA DOLGOŽIVOST ČEBEL (Apis mellifera carnica) Maja Ivana SMODIŠ ŠKERL 1, Mitja NAKRST 2, Aleš GREGORC 3 IZVLEČEK Za krmljenje čebeljih družin se v času pomanjkanja
BAKTERIOCINI IZVEDLJIVA ALTERNATIVA ANTIBIOTIKOM?
 UNIVERZITETNI DOKTORSKI ŠTUDIJ BIOMEDICINA SEMINAR pri predmetu Temeljna medicinska mikrobiologija Petra Raspor Lainšček, dr. vet. med BAKTERIOCINI IZVEDLJIVA ALTERNATIVA ANTIBIOTIKOM? MODERATOR SEMINARJA
UNIVERZITETNI DOKTORSKI ŠTUDIJ BIOMEDICINA SEMINAR pri predmetu Temeljna medicinska mikrobiologija Petra Raspor Lainšček, dr. vet. med BAKTERIOCINI IZVEDLJIVA ALTERNATIVA ANTIBIOTIKOM? MODERATOR SEMINARJA
VPLIV DOLGOTRAJNEGA SKLADIŠČENJA TRAVNE SILAŽE NA NJENO HRANILNO VREDNOST IN KAKOVOST. Drago BABNIK a) in Jože VERBIČ b)
 Zb. Bioteh. Fak. Univ. Ljubl., Kmet. Zooteh., 82(december 2003)2, 109 117. http://www.bfro.uni-lj.si/zoo/publikacije/zbornik Izvirni znanstveni prispevek Original scientific article VPLIV DOLGOTRAJNEGA
Zb. Bioteh. Fak. Univ. Ljubl., Kmet. Zooteh., 82(december 2003)2, 109 117. http://www.bfro.uni-lj.si/zoo/publikacije/zbornik Izvirni znanstveni prispevek Original scientific article VPLIV DOLGOTRAJNEGA
ALI JE DOLGOTRAJNA UPORABA ZAVIRALCEV PROTONSKE ČRPALKE VARNA?
 ALI JE DOLGOTRAJNA UPORABA ZAVIRALCEV PROTONSKE ČRPALKE VARNA? Darja Logar, dr. med. Barbara Mazej Poredoš, dr. med. Ljubljana, 18. 10. 2012 Dandanes se izjemno povečuje poraba ZPČ, čemur smo priča tudi
ALI JE DOLGOTRAJNA UPORABA ZAVIRALCEV PROTONSKE ČRPALKE VARNA? Darja Logar, dr. med. Barbara Mazej Poredoš, dr. med. Ljubljana, 18. 10. 2012 Dandanes se izjemno povečuje poraba ZPČ, čemur smo priča tudi
HEMATURIJA PRI OTROCIH HAEMATURIA IN CHILDREN
 HEMATURIJA PRI OTROCIH HAEMATURIA IN CHILDREN - ABSTRACT - - UVOD IN OPREDELITEV POJMOV Hematurija je prisotnost krvi v urinu. - - - mesecev. Lahko je - - Hematurija je sicer lahko pomemben znak bolezni
HEMATURIJA PRI OTROCIH HAEMATURIA IN CHILDREN - ABSTRACT - - UVOD IN OPREDELITEV POJMOV Hematurija je prisotnost krvi v urinu. - - - mesecev. Lahko je - - Hematurija je sicer lahko pomemben znak bolezni
ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE?
 ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE? SPECIALIZACIJA IZ DRUŽINSKE MEDICINE MODUL: NA DOKAZIH TEMELJEČA MEDICINA 16. SKUPINA AVTORJI: MIRJANA NINKOV MILA MRŠIĆ OLIVER ILIĆ OPIS
ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE? SPECIALIZACIJA IZ DRUŽINSKE MEDICINE MODUL: NA DOKAZIH TEMELJEČA MEDICINA 16. SKUPINA AVTORJI: MIRJANA NINKOV MILA MRŠIĆ OLIVER ILIĆ OPIS
VPLIV METFORMINA NA RAKAVE CELICE V KULTURI V ODVISNOSTI OD RAZPOLOŽLJIVIH HRANIL
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Maruša BIZJAK VPLIV METFORMINA NA RAKAVE CELICE V KULTURI V ODVISNOSTI OD RAZPOLOŽLJIVIH HRANIL DOKTORSKA DISERTACIJA Ljubljana, 2018 UNIVERZA V LJUBLJANI BIOTEHNIŠKA
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Maruša BIZJAK VPLIV METFORMINA NA RAKAVE CELICE V KULTURI V ODVISNOSTI OD RAZPOLOŽLJIVIH HRANIL DOKTORSKA DISERTACIJA Ljubljana, 2018 UNIVERZA V LJUBLJANI BIOTEHNIŠKA
VPLIV Cr(VI) IONOV NA OKSIDATIVNE POŠKODBE LIPIDOV IN PROTEINOV
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Vida KOCBEK VPLIV Cr(VI) IONOV NA OKSIDATIVNE POŠKODBE LIPIDOV IN PROTEINOV DIPLOMSKO DELO Univerzitetni študij THE
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Vida KOCBEK VPLIV Cr(VI) IONOV NA OKSIDATIVNE POŠKODBE LIPIDOV IN PROTEINOV DIPLOMSKO DELO Univerzitetni študij THE
ANALIZA VNOSA MAKRO IN MIKRO HRANIL PRI PROFESIONALNIH IGRALKAH ROKOMETA Z RAČUNALNIŠKIM PROGRAMOM Prodi 5.0
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Špela CERAR ANALIZA VNOSA MAKRO IN MIKRO HRANIL PRI PROFESIONALNIH IGRALKAH ROKOMETA Z RAČUNALNIŠKIM PROGRAMOM Prodi 5.0 DIPLOMSKO DELO Univerzitetni
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Špela CERAR ANALIZA VNOSA MAKRO IN MIKRO HRANIL PRI PROFESIONALNIH IGRALKAH ROKOMETA Z RAČUNALNIŠKIM PROGRAMOM Prodi 5.0 DIPLOMSKO DELO Univerzitetni
Glukoza oksidaze potencialni encimi za beljenje tekstilnih vlaken Pregledni znanstveni članek
 16 Glukoza oksidaze potencialni encimi za beljenje tekstilnih vlaken Glucose Oxidases Potential Enzymes for Bleaching Textile Fibres January 2011 February 2011 Abstract Glucose oxidases catalyse the oxidation
16 Glukoza oksidaze potencialni encimi za beljenje tekstilnih vlaken Glucose Oxidases Potential Enzymes for Bleaching Textile Fibres January 2011 February 2011 Abstract Glucose oxidases catalyse the oxidation
ANTIOKSIDATIVNA UČINKOVITOST RŽENEGA SLADA
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Bojana KLEMENČIČ ANTIOKSIDATIVNA UČINKOVITOST RŽENEGA SLADA DIPLOMSKO DELO Univerzitetni študij - 1. stopnja Živilstvo in prehrana Ljubljana,
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Bojana KLEMENČIČ ANTIOKSIDATIVNA UČINKOVITOST RŽENEGA SLADA DIPLOMSKO DELO Univerzitetni študij - 1. stopnja Živilstvo in prehrana Ljubljana,
VALIDITY OF TEST OF OBJECT RELATIONS (TOR) BASIC INFORMATIONS FOR RESEARCHERS
 VALIDITY OF TEST OF OBJECT RELATIONS (TOR) BASIC INFORMATIONS FOR RESEARCHERS (unpublished and not lectured version work in progress) 2002 Gregor Zvelc, Institute for Integrative Psychotherapy and Counseling,
VALIDITY OF TEST OF OBJECT RELATIONS (TOR) BASIC INFORMATIONS FOR RESEARCHERS (unpublished and not lectured version work in progress) 2002 Gregor Zvelc, Institute for Integrative Psychotherapy and Counseling,
PREBAVNA MIKROBIOTA KOT DEJAVNIK PRI RAZVOJU DEBELOSTI
 DOI: 10.2478/v10014-010-0007-z COBISS: 1.02 Agris category code: S30 PREBAVNA MIKROBIOTA KOT DEJAVNIK PRI RAZVOJU DEBELOSTI Vesna JERMAN 1, Gorazd AVGUŠTIN 2 Delo je prispelo 12. aprila 2010, sprejeto
DOI: 10.2478/v10014-010-0007-z COBISS: 1.02 Agris category code: S30 PREBAVNA MIKROBIOTA KOT DEJAVNIK PRI RAZVOJU DEBELOSTI Vesna JERMAN 1, Gorazd AVGUŠTIN 2 Delo je prispelo 12. aprila 2010, sprejeto
AKTIVNOST ENCIMOV FENILPROPANOIDNE POTI, KOT ODZIV TKIVA NA OKUŽBO Z JABLANOVIM ŠKRLUPOM (Venturia inaequalis (Cooke) G. Wint.)
 Zbornik predavanj in referatov 9. slovenskega posvetovanja o varstvu rastlin z mednarodno udeležbo 447 Nova Gorica, 4. 5. marec 2009 AKTIVNOST ENCIMOV FENILPROPANOIDNE POTI, KOT ODZIV TKIVA NA OKUŽBO Z
Zbornik predavanj in referatov 9. slovenskega posvetovanja o varstvu rastlin z mednarodno udeležbo 447 Nova Gorica, 4. 5. marec 2009 AKTIVNOST ENCIMOV FENILPROPANOIDNE POTI, KOT ODZIV TKIVA NA OKUŽBO Z
UGOTAVLJANJE STABILNOSTI ANTOCIANOV MED SIMULACIJO PREBAVE SOKA GRANATNEGA JABOLKA (Punica granatum L.) IN VITRO
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tina KLEPAC UGOTAVLJANJE STABILNOSTI ANTOCIANOV MED SIMULACIJO PREBAVE SOKA GRANATNEGA JABOLKA (Punica granatum L.) IN VITRO MAGISTRSKO DELO STABILITY OF ANTHOCYANINS
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tina KLEPAC UGOTAVLJANJE STABILNOSTI ANTOCIANOV MED SIMULACIJO PREBAVE SOKA GRANATNEGA JABOLKA (Punica granatum L.) IN VITRO MAGISTRSKO DELO STABILITY OF ANTHOCYANINS
KAKOVOST LUCERNINIH SILAŽ PRIPRAVLJENIH Z DODATKOM RAZLIČNIH VRST TANINSKIH IZVLEČKOV
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Marko KOKALJ KAKOVOST LUCERNINIH SILAŽ PRIPRAVLJENIH Z DODATKOM RAZLIČNIH VRST TANINSKIH IZVLEČKOV MAGISTRSKO DELO Magistrski študij 2.
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Marko KOKALJ KAKOVOST LUCERNINIH SILAŽ PRIPRAVLJENIH Z DODATKOM RAZLIČNIH VRST TANINSKIH IZVLEČKOV MAGISTRSKO DELO Magistrski študij 2.
PRIMERJAVA METOD ZA DOLOČANJE PREHRANSKEGA STATUSA POSAMEZNIKA
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tamara PUŠ PRIMERJAVA METOD ZA DOLOČANJE PREHRANSKEGA STATUSA POSAMEZNIKA DOKTORSKA DISERTACIJA Ljubljana, 2013 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tamara
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tamara PUŠ PRIMERJAVA METOD ZA DOLOČANJE PREHRANSKEGA STATUSA POSAMEZNIKA DOKTORSKA DISERTACIJA Ljubljana, 2013 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Tamara
UČINKOVITOST RAZKUŽIL NA DELOVNIH POVRŠINAH EFFICIENCY OF DISINFECTANTS ON WORKING SURFACES
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Urška RIBIČ UČINKOVITOST RAZKUŽIL NA DELOVNIH POVRŠINAH DIPLOMSKO DELO Univerzitetni študij EFFICIENCY OF DISINFECTANTS ON WORKING SURFACES
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Urška RIBIČ UČINKOVITOST RAZKUŽIL NA DELOVNIH POVRŠINAH DIPLOMSKO DELO Univerzitetni študij EFFICIENCY OF DISINFECTANTS ON WORKING SURFACES
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO KATARINA MEHLE DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJSKI PROGRAM KOZMETOLOGIJA
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO KATARINA MEHLE DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJSKI PROGRAM KOZMETOLOGIJA Ljubljana, 2015 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO KATARINA MEHLE OCENA
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO KATARINA MEHLE DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJSKI PROGRAM KOZMETOLOGIJA Ljubljana, 2015 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO KATARINA MEHLE OCENA
Contents of sugars and organic acids in the cultivars of peach (Prunus persica L.) and nectarine (Prunus persica var. nucipersica Schneid.
 Acta agriculturae slovenica, 83-1, junij 2004 str. 53-61 Agrovoc deskriptors: Prunus persica, Prunus persica nucipersica, varieties, sugars, organic acids, quality, qualitative analysis, chemicophysical
Acta agriculturae slovenica, 83-1, junij 2004 str. 53-61 Agrovoc deskriptors: Prunus persica, Prunus persica nucipersica, varieties, sugars, organic acids, quality, qualitative analysis, chemicophysical
ANTIFEEDANT EFFECTS OF SEVERAL NATURAL SUBSTANCES ON SOME PHYTOPHAGOUS INSECT SPECIES
 Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 239-243 Zreče, 4. 6. marec 2003 ANTIFEEDANT EFFECTS OF SEVERAL NATURAL SUBSTANCES ON SOME PHYTOPHAGOUS INSECT SPECIES
Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 239-243 Zreče, 4. 6. marec 2003 ANTIFEEDANT EFFECTS OF SEVERAL NATURAL SUBSTANCES ON SOME PHYTOPHAGOUS INSECT SPECIES
Presence of Nonylphenols in Plastic Films and Their Migration Into Food Simulants
 127 Scientific paper Presence of Nonylphenols in Plastic Films and Their Migration Into Food Simulants Marjetka Alfirevi}, 1, * Bo{tjan Kri`anec, 2, * Ernest Von~ina 2 and Darinka Brodnjak Von~ina 1 1
127 Scientific paper Presence of Nonylphenols in Plastic Films and Their Migration Into Food Simulants Marjetka Alfirevi}, 1, * Bo{tjan Kri`anec, 2, * Ernest Von~ina 2 and Darinka Brodnjak Von~ina 1 1
zbornik zbranih povzetkov vsebin projekta Zgodnje naravoslovje
 zbornik zbranih povzetkov vsebin projekta Zgodnje naravoslovje TEMELJ za trajnostni razvoj Ekošola kot način življenja avgust 2010 ZBORNIK zbranih povzetkov vsebin projekta Zgodnje naravoslovje temelj
zbornik zbranih povzetkov vsebin projekta Zgodnje naravoslovje TEMELJ za trajnostni razvoj Ekošola kot način življenja avgust 2010 ZBORNIK zbranih povzetkov vsebin projekta Zgodnje naravoslovje temelj
IZOLACIJA DNK IZ SADJA IN ZELENJAVE
 IZOLACIJA DNK IZ SADJA IN ZELENJAVE Raziskovalna naloga AVTOR: Marcel Hribernik MENTORICA: Irena Drofenik, univ. dipl. kem. Celje, marec 2013 Kazalo IZOLACIJA DNK IZ SADJA IN ZELENJAVE... 1 Kazalo... 2
IZOLACIJA DNK IZ SADJA IN ZELENJAVE Raziskovalna naloga AVTOR: Marcel Hribernik MENTORICA: Irena Drofenik, univ. dipl. kem. Celje, marec 2013 Kazalo IZOLACIJA DNK IZ SADJA IN ZELENJAVE... 1 Kazalo... 2
FARMACEVTSKI VESTNIK št. 2
 Farm Vestn 2015; 66: 125 229; UDK 615 CODEN FMVTA, SLO ISSN 0014-8229 maj 2015, letnik 66 FARMACEVTSKI VESTNIK št. 2 OSREDNJA TEMA: OKSIDATIVNI STRES ZDRAVLJENJE PSIHOZ TABU MOŠKE TEME STROKOVNO GLASILO
Farm Vestn 2015; 66: 125 229; UDK 615 CODEN FMVTA, SLO ISSN 0014-8229 maj 2015, letnik 66 FARMACEVTSKI VESTNIK št. 2 OSREDNJA TEMA: OKSIDATIVNI STRES ZDRAVLJENJE PSIHOZ TABU MOŠKE TEME STROKOVNO GLASILO
Osnove prehrane športnikov
 Osnove prehrane športnikov povzeto po: Fred Brouns, Essentials of sports nutrition John Wiley & Sons Ltd. 2002 (1993) Andrej N. September 2010 1 1 UVOD 6 1.1 Metabolizem 7 1.1.1 Prebava 7 1.1.2 Energija
Osnove prehrane športnikov povzeto po: Fred Brouns, Essentials of sports nutrition John Wiley & Sons Ltd. 2002 (1993) Andrej N. September 2010 1 1 UVOD 6 1.1 Metabolizem 7 1.1.1 Prebava 7 1.1.2 Energija
PROTIMIKROBNO DELOVANJE NITRITA NA BAKTERIJE VRSTE Listeria monocytogenes
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tina GERBEC PROTIMIKROBNO DELOVANJE NITRITA NA BAKTERIJE VRSTE Listeria monocytogenes DIPLOMSKO DELO Univerzitetni študij ANTIMICROBIAL ACTIVITY
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tina GERBEC PROTIMIKROBNO DELOVANJE NITRITA NA BAKTERIJE VRSTE Listeria monocytogenes DIPLOMSKO DELO Univerzitetni študij ANTIMICROBIAL ACTIVITY
Virus mozaika pepina gospodarsko pomemben virus paradižnika. Prof. dr. Maja Ravnikar mag. Nataša a Mehle
 Virus mozaika pepina gospodarsko pomemben virus paradižnika Prof. dr. Maja Ravnikar mag. Nataša a Mehle Lisavost ali degenerativne spremembe plodov paradižnika mnogokrat povzročajo različni rastlinski
Virus mozaika pepina gospodarsko pomemben virus paradižnika Prof. dr. Maja Ravnikar mag. Nataša a Mehle Lisavost ali degenerativne spremembe plodov paradižnika mnogokrat povzročajo različni rastlinski
THE OCCURRENCE OF OLIVE KNOT DISEASE CAUSED BY Pseudomonas savastanoi IN THE NORTHWEST REGION OF ISTRIAN PENINSULA ABSTRACT
 Zbornik predavanj in referatov 9. slovenskega posvetovanja o varstvu rastlin z mednarodno udeležbo 467 Nova Gorica, 4. 5. marec 2009 THE OCCURRENCE OF OLIVE KNOT DISEASE CAUSED BY Pseudomonas savastanoi
Zbornik predavanj in referatov 9. slovenskega posvetovanja o varstvu rastlin z mednarodno udeležbo 467 Nova Gorica, 4. 5. marec 2009 THE OCCURRENCE OF OLIVE KNOT DISEASE CAUSED BY Pseudomonas savastanoi
ANJA ŽMAVC DOLOČANJE AKTIVNOSTI PANKREATINA TER IN VITRO LIPOLIZE NA LIPIDIH OSNOVANIH SISTEMOV S PH-STAT METODO
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANJA ŽMAVC DOLOČANJE AKTIVNOSTI PANKREATINA TER IN VITRO LIPOLIZE NA LIPIDIH OSNOVANIH SISTEMOV S PH-STAT METODO DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJ FARMACIJE
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANJA ŽMAVC DOLOČANJE AKTIVNOSTI PANKREATINA TER IN VITRO LIPOLIZE NA LIPIDIH OSNOVANIH SISTEMOV S PH-STAT METODO DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJ FARMACIJE
1 Introduction. COBISS: 1.01 Agris category code: M40
 COBISS: 1.01 Agris category code: M40 Fluctuating asymmetry in diploid female and sterile triploid rainbow trout (Oncorhynchus mykiss) Jurij POHAR 1, Klavdija STRGAR 2 Received November 05, 2010; accepted
COBISS: 1.01 Agris category code: M40 Fluctuating asymmetry in diploid female and sterile triploid rainbow trout (Oncorhynchus mykiss) Jurij POHAR 1, Klavdija STRGAR 2 Received November 05, 2010; accepted
MODUL: NA DOKAZIH TEMELJEČA MEDICINA. ZD SLOV.KONJICE Lucija Kračun, dr.med Loče,
 MODUL: NA DOKAZIH TEMELJEČA MEDICINA ZD SLOV.KONJICE Lucija Kračun, dr.med Loče, 30.1.2010 Opis problema vključno z opisom populacije, na katero se problem nanaša Ali je bolnike starejše od 80 let smiselno
MODUL: NA DOKAZIH TEMELJEČA MEDICINA ZD SLOV.KONJICE Lucija Kračun, dr.med Loče, 30.1.2010 Opis problema vključno z opisom populacije, na katero se problem nanaša Ali je bolnike starejše od 80 let smiselno
Examination of Colour Emotions on a Sample of Slovenian Female Population Proučevanje čustvenega odziva na barve na vzorcu ženske populacije Slovenije
 311 Andreja Guzelj, Aleš Hladnik, Sabina Bračko University of Ljubljana, Faculty of Natural Sciences and Engineering, Department of Textiles, Graphic Arts and Design, 1000 Ljubljana, Snežniška 5, Slovenia
311 Andreja Guzelj, Aleš Hladnik, Sabina Bračko University of Ljubljana, Faculty of Natural Sciences and Engineering, Department of Textiles, Graphic Arts and Design, 1000 Ljubljana, Snežniška 5, Slovenia
ACTA BIOLOGICA SLOVENICA LJUBLJANA 2017 Vol. 60, Št. 1: 89 99
 ACTA BIOLOGICA SLOVENICA LJUBLJANA 2017 Vol. 60, Št. 1: 89 99 Lower secondary school students interest and emotions regarding dissection in schools - a pilot study Interes in čustva osnovnošolcev v povezavi
ACTA BIOLOGICA SLOVENICA LJUBLJANA 2017 Vol. 60, Št. 1: 89 99 Lower secondary school students interest and emotions regarding dissection in schools - a pilot study Interes in čustva osnovnošolcev v povezavi
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE. Diana DRAKSLER
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Diana DRAKSLER VPLIV GOJIŠČA NA SESTAVO DOLGOVERIŽNIH MAŠČOBNIH KISLIN IN MAŠČOBNIH ALDEHIDOV PRI VAMPNIH BAKTERIJAH
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Diana DRAKSLER VPLIV GOJIŠČA NA SESTAVO DOLGOVERIŽNIH MAŠČOBNIH KISLIN IN MAŠČOBNIH ALDEHIDOV PRI VAMPNIH BAKTERIJAH
VPLIV KANABINOIDOV NA VEDENJE, PROBLEMATIKA UPORABE V NAJSTNIŠKIH LETIH TER PRIMERJAVA UČINKOV KONOPLJE Z ALKOHOLOM
 UGRIN ZAKLJUČNA NALOGA 2017 UNIVERZA NA PRIMORSKEM FAKULTETA ZA MATEMATIKO, NARAVOSLOVJE IN INFORMACIJSKE TEHNOLOGIJE ZAKLJUČNA NALOGA VPLIV KANABINOIDOV NA VEDENJE, PROBLEMATIKA UPORABE V NAJSTNIŠKIH
UGRIN ZAKLJUČNA NALOGA 2017 UNIVERZA NA PRIMORSKEM FAKULTETA ZA MATEMATIKO, NARAVOSLOVJE IN INFORMACIJSKE TEHNOLOGIJE ZAKLJUČNA NALOGA VPLIV KANABINOIDOV NA VEDENJE, PROBLEMATIKA UPORABE V NAJSTNIŠKIH
 VSEBNOST SEČNINE V MLEKU KRAV V SLOVENIJI Jože VERBIČ 1, Janez JENKO 2, Jože GLAD 3, Drago BABNIK 4, Tomaž PERPAR IZVLEČEK Na podlagi rezultatov 69.66 določitev v obdobju -8 podajamo stanje na področju
VSEBNOST SEČNINE V MLEKU KRAV V SLOVENIJI Jože VERBIČ 1, Janez JENKO 2, Jože GLAD 3, Drago BABNIK 4, Tomaž PERPAR IZVLEČEK Na podlagi rezultatov 69.66 določitev v obdobju -8 podajamo stanje na področju
HIV/AIDS UPDATE Janez Tomažič Klinika za infekcijske bolezni in vročinska stanja Katedra za infekcijske bolezni in epidemiologijo
 HIV/AIDS UPDATE 2017 Janez Tomažič Klinika za infekcijske bolezni in vročinska stanja Katedra za infekcijske bolezni in epidemiologijo Patogeneza okužbe s HIV 1. Sesutje imunskega sistema KLINIČNE OPREDELITVE
HIV/AIDS UPDATE 2017 Janez Tomažič Klinika za infekcijske bolezni in vročinska stanja Katedra za infekcijske bolezni in epidemiologijo Patogeneza okužbe s HIV 1. Sesutje imunskega sistema KLINIČNE OPREDELITVE
SULPHUR AND CHLORINE CONTENT IN FORAGES FROM DEFINED REGION ABSTRACT VSEBNOST ŽVEPLA IN KLORA V VOLUMINOZNI KRMI Z DOLOČENEGA OBMOČJA IZVLEČEK
 Original scientific paper Izvirni znanstveni prispevek SULPHUR AND CHLORINE CONTENT IN FORAGES FROM DEFINED REGION Marija RAJČEVIČ a), Anton ILC b), Peter KUMP c) and Marijan NEČEMER c) a) Poslovni sistem
Original scientific paper Izvirni znanstveni prispevek SULPHUR AND CHLORINE CONTENT IN FORAGES FROM DEFINED REGION Marija RAJČEVIČ a), Anton ILC b), Peter KUMP c) and Marijan NEČEMER c) a) Poslovni sistem
UGOTAVLJANJE CITOTOKSIČNOSTI RDEČEGA BARVILA BAKTERIJE Vibrio sp. ZA PRIMARNE MIŠJE LIMFOCITE B
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Urška KLADNIK UGOTAVLJANJE CITOTOKSIČNOSTI RDEČEGA BARVILA BAKTERIJE Vibrio sp. ZA PRIMARNE MIŠJE LIMFOCITE B DIPLOMSKO DELO Univerzitetni
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Urška KLADNIK UGOTAVLJANJE CITOTOKSIČNOSTI RDEČEGA BARVILA BAKTERIJE Vibrio sp. ZA PRIMARNE MIŠJE LIMFOCITE B DIPLOMSKO DELO Univerzitetni
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO JASMINA PUTANEC DIPLOMSKA NALOGA. Univerzitetni študij farmacije
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO JASMINA PUTANEC Univerzitetni študij farmacije Ljubljana, 2012 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO JASMINA PUTANEC VREDNOTENJE OKSIDATIVNE NESTABILNOSTI
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO JASMINA PUTANEC Univerzitetni študij farmacije Ljubljana, 2012 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO JASMINA PUTANEC VREDNOTENJE OKSIDATIVNE NESTABILNOSTI
Sladkorna bolezen in kirurški poseg
 Sladkorna bolezen in kirurški poseg Doc.dr.Vilma Urbančič, dr.med. UKC Ljubljana KO EDBP, Diabetološki oddelek 1.12.2010 10. Podiplomski tečaj iz hospitalne diabetologije Ljubljana, 24.11. -2.12.2010 Noordzij
Sladkorna bolezen in kirurški poseg Doc.dr.Vilma Urbančič, dr.med. UKC Ljubljana KO EDBP, Diabetološki oddelek 1.12.2010 10. Podiplomski tečaj iz hospitalne diabetologije Ljubljana, 24.11. -2.12.2010 Noordzij
PROTEINSKE TARČE EKSTRAKTA MORSKE ALGE Fucus vesiculosus
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Sabina OTT PROTEINSKE TARČE EKSTRAKTA MORSKE ALGE Fucus vesiculosus MAGISTRSKO DELO Magistrski študij - 2. stopnja Biotehnologija Ljubljana,
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ŠTUDIJ BIOTEHNOLOGIJE Sabina OTT PROTEINSKE TARČE EKSTRAKTA MORSKE ALGE Fucus vesiculosus MAGISTRSKO DELO Magistrski študij - 2. stopnja Biotehnologija Ljubljana,
Abstract. Izvleček. Avtor / Author Zalika Klemenc Ketiš 1,2
 Klinična Pregledni študija ~lanek / Clinical / Impressum Review study Učinki ambulantne SPREMLJANJE fizikalne PRETOKA terapije V MOŽGANSKIH pri bolnikih s kronično ARTERIJAH bolečino v S križu TCD Outcomes
Klinična Pregledni študija ~lanek / Clinical / Impressum Review study Učinki ambulantne SPREMLJANJE fizikalne PRETOKA terapije V MOŽGANSKIH pri bolnikih s kronično ARTERIJAH bolečino v S križu TCD Outcomes
STABILNOST POPULACIJE LAKTOBACILOV IN KVASOVK V KEFIRNEM ZRNU IN KEFIRJU
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Gašper VOZEL STABILNOST POPULACIJE LAKTOBACILOV IN KVASOVK V KEFIRNEM ZRNU IN KEFIRJU DIPLOMSKO DELO Univerzitetni študij Ljubljana, 2016
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Gašper VOZEL STABILNOST POPULACIJE LAKTOBACILOV IN KVASOVK V KEFIRNEM ZRNU IN KEFIRJU DIPLOMSKO DELO Univerzitetni študij Ljubljana, 2016
PONUDBA HRANE ZA PSE NA SLOVENSKEM TRGU
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Mitja ŠAVORN PONUDBA HRANE ZA PSE NA SLOVENSKEM TRGU DIPLOMSKO DELO Univerzitetni študij THE OFFER OF DOG FOODS ON SLOVENE MARKET GRADUATION
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Mitja ŠAVORN PONUDBA HRANE ZA PSE NA SLOVENSKEM TRGU DIPLOMSKO DELO Univerzitetni študij THE OFFER OF DOG FOODS ON SLOVENE MARKET GRADUATION
FITNESS AS DETERMINANTS OF BODY BALANCE IN ELDERLY MEN
 Kinesiologia Slovenica, 12, 1, 39 47 (2006) Faculty of Sport, University of Ljubljana, ISSN 1318-2269 39 Janusz Maciaszek BODY COMPOSITION AND MOTOR FITNESS AS DETERMINANTS OF BODY BALANCE IN ELDERLY MEN
Kinesiologia Slovenica, 12, 1, 39 47 (2006) Faculty of Sport, University of Ljubljana, ISSN 1318-2269 39 Janusz Maciaszek BODY COMPOSITION AND MOTOR FITNESS AS DETERMINANTS OF BODY BALANCE IN ELDERLY MEN
VPLIV SPANJA NA KONSOLIDACIJO SPOMINA
 ZAKLJUČNA NALOGA UNIVERZA NA PRIMORSKEM FAKULTETA ZA MATEMATIKO, NARAVOSLOVJE IN INFORMACIJSKE TEHNOLOGIJE ZAKLJUČNA NALOGA VPLIV SPANJA NA KONSOLIDACIJO SPOMINA ANITA TURŠIČ UNIVERZA NA PRIMORSKEM FAKULTETA
ZAKLJUČNA NALOGA UNIVERZA NA PRIMORSKEM FAKULTETA ZA MATEMATIKO, NARAVOSLOVJE IN INFORMACIJSKE TEHNOLOGIJE ZAKLJUČNA NALOGA VPLIV SPANJA NA KONSOLIDACIJO SPOMINA ANITA TURŠIČ UNIVERZA NA PRIMORSKEM FAKULTETA
PROTIMIKROBNO DELOVANJE IZVLEČKOV LISTJA IN GROZDNIH KOŽIC VINSKE TRTE (Vitis vinifera L.) NA PATOGENE BAKTERIJE ŽIVIL
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Bojana KESER PROTIMIKROBNO DELOVANJE IZVLEČKOV LISTJA IN GROZDNIH KOŽIC VINSKE TRTE (Vitis vinifera L.) NA PATOGENE BAKTERIJE ŽIVIL DIPLOMSKO
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Bojana KESER PROTIMIKROBNO DELOVANJE IZVLEČKOV LISTJA IN GROZDNIH KOŽIC VINSKE TRTE (Vitis vinifera L.) NA PATOGENE BAKTERIJE ŽIVIL DIPLOMSKO
Antalašić M. Učinkovitost imunoencimske metode (E.L.I.S.A.) potvorb ovčjega s kravjim mlekom. Dipl. delo. Ljubljana, Univ. v Ljubljani, Biotehniška fa
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Monika ANTALAŠIĆ UČINKOVITOST UPORABE HITRE IMUNOENCIMSKE METODE (E.L.I.S.A.) ZA ODKRIVANJE POTVORB OVČJEGA MLEKA S KRAVJIM MLEKOM DIPLOMSKO
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Monika ANTALAŠIĆ UČINKOVITOST UPORABE HITRE IMUNOENCIMSKE METODE (E.L.I.S.A.) ZA ODKRIVANJE POTVORB OVČJEGA MLEKA S KRAVJIM MLEKOM DIPLOMSKO
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO SARA PAPLER DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJSKI PROGRAM KOZMETOLOGIJA Ljubljana, junij 2015 1 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO SARA PAPLER VPLIV
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO SARA PAPLER DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJSKI PROGRAM KOZMETOLOGIJA Ljubljana, junij 2015 1 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO SARA PAPLER VPLIV
STRUPENOST IN ESTROGENOST ORGANSKIH UV- FILTROV NA VODNE ORGANIZME
 UNIVERZA V NOVI GORICI FAKULTETA ZA ZNANOSTI O OKOLJU STRUPENOST IN ESTROGENOST ORGANSKIH UV- FILTROV NA VODNE ORGANIZME DIPLOMSKO DELO Mitja MARC Mentor: doc. dr. Tatjana TIŠLER Nova Gorica, 2012 ZAHVALA
UNIVERZA V NOVI GORICI FAKULTETA ZA ZNANOSTI O OKOLJU STRUPENOST IN ESTROGENOST ORGANSKIH UV- FILTROV NA VODNE ORGANIZME DIPLOMSKO DELO Mitja MARC Mentor: doc. dr. Tatjana TIŠLER Nova Gorica, 2012 ZAHVALA
EVALUATION OF ANTIMICROBIAL EFFECT OF IRANIAN SUMAC ON Bacillus cereus IN A COMMERCIAL BARLEY SOUP
 Slov Vet Res 2017; 54 (2): 65-9 UDC 615.281.9:582.742:579.852.11:641.827 Original Research Article EVALUATION OF ANTIMICROBIAL EFFECT OF IRANIAN SUMAC ON Bacillus cereus IN A COMMERCIAL BARLEY SOUP Reza
Slov Vet Res 2017; 54 (2): 65-9 UDC 615.281.9:582.742:579.852.11:641.827 Original Research Article EVALUATION OF ANTIMICROBIAL EFFECT OF IRANIAN SUMAC ON Bacillus cereus IN A COMMERCIAL BARLEY SOUP Reza
STABILNOST ASKORBINSKE IN DEHIDROASKORBINSKE KISLINE V VODNIH RAZTOPINAH DIPLOMSKO DELO Univerzitetni študij
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tomaž POREDOŠ STABILNOST ASKORBINSKE IN DEHIDROASKORBINSKE KISLINE V VODNIH RAZTOPINAH DIPLOMSKO DELO Univerzitetni študij STABILITY OF ASCORBIC
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Tomaž POREDOŠ STABILNOST ASKORBINSKE IN DEHIDROASKORBINSKE KISLINE V VODNIH RAZTOPINAH DIPLOMSKO DELO Univerzitetni študij STABILITY OF ASCORBIC
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MELITA HRIBAR DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJ FARMACIJE
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MELITA HRIBAR DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJ FARMACIJE Ljubljana, 2014 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MELITA HRIBAR REŠETANJE ZAVIRALCEV
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MELITA HRIBAR DIPLOMSKA NALOGA UNIVERZITETNI ŠTUDIJ FARMACIJE Ljubljana, 2014 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MELITA HRIBAR REŠETANJE ZAVIRALCEV
RAZPOREDITEV GENOTIPOV VIRUSA HEPATITISA C V SLOVENIJI V LETIH
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Gregor ZUPAN RAZPOREDITEV GENOTIPOV VIRUSA HEPATITISA C V SLOVENIJI V LETIH 2003-2006 DIPLOMSKO DELO Univerzitetni
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Gregor ZUPAN RAZPOREDITEV GENOTIPOV VIRUSA HEPATITISA C V SLOVENIJI V LETIH 2003-2006 DIPLOMSKO DELO Univerzitetni
DEJAVNIKI TVEGANJA ZA PARODONTALNO BOLEZEN PRI PREBIVALCIH LJUBLJANE Risk factors for periodontal disease among residents of Ljubljana
 skaleric_e_skaleric_e.qxd 27.10.2014 11:22 Page 28 Zobozdrav Vestn 2014; 69: 28--35 28 DEJAVNIKI TVEGANJA ZA PARODONTALNO BOLEZEN PRI PREBIVALCIH LJUBLJANE Risk factors for periodontal disease among residents
skaleric_e_skaleric_e.qxd 27.10.2014 11:22 Page 28 Zobozdrav Vestn 2014; 69: 28--35 28 DEJAVNIKI TVEGANJA ZA PARODONTALNO BOLEZEN PRI PREBIVALCIH LJUBLJANE Risk factors for periodontal disease among residents
CITOTOKSIČNO IN GENOTOKSIČNO DELOVANJE NARAVNIH IN MINERALNIH VOD NA CELICE HepG2
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Jana PETKOVIĆ CITOTOKSIČNO IN GENOTOKSIČNO DELOVANJE NARAVNIH IN MINERALNIH VOD NA CELICE HepG2 DIPLOMSKO DELO Univerzitetni
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Jana PETKOVIĆ CITOTOKSIČNO IN GENOTOKSIČNO DELOVANJE NARAVNIH IN MINERALNIH VOD NA CELICE HepG2 DIPLOMSKO DELO Univerzitetni
CONCENTRATION OF PROTEINS, BETA-GLUCANS, TOTAL PHENOLS AND ANTIOXIDANT CAPACITY OF SLOVENIAN SAMPLES OF BARLEY
 CONCENTRATION OF PROTEINS, BETA-GLUCANS, TOTAL PHENOLS AND ANTIOXIDANT CAPACITY OF SLOVENIAN SAMPLES OF BARLEY VSEBNOST PROTEINOV, BETA-GLUKANOV, SKUPNIH FENOLOV IN ANTIOKSIDATIVNA VREDNOST SLOVENSKIH
CONCENTRATION OF PROTEINS, BETA-GLUCANS, TOTAL PHENOLS AND ANTIOXIDANT CAPACITY OF SLOVENIAN SAMPLES OF BARLEY VSEBNOST PROTEINOV, BETA-GLUKANOV, SKUPNIH FENOLOV IN ANTIOKSIDATIVNA VREDNOST SLOVENSKIH
Osnove farmakokinetike
 Osnove farmakokinetike prof. dr. Lovro Stanovnik Inštitut za farmakologijo in eksperimentalno toksikologijo, Medicinska fakulteta, Univerza v Ljubljani Farmakologija Vedo o delovanju zdravilih in drugih
Osnove farmakokinetike prof. dr. Lovro Stanovnik Inštitut za farmakologijo in eksperimentalno toksikologijo, Medicinska fakulteta, Univerza v Ljubljani Farmakologija Vedo o delovanju zdravilih in drugih
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO. Laura BERTALANIČ
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Laura BERTALANIČ VPLIV TOPILA NA DOLOČENO ANTIOKSIDATIVNO AKTIVNOST VIN IN MODELNIH ANTIOKSIDANTOV DIPLOMSKO DELO Univerzitetni študij THE
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Laura BERTALANIČ VPLIV TOPILA NA DOLOČENO ANTIOKSIDATIVNO AKTIVNOST VIN IN MODELNIH ANTIOKSIDANTOV DIPLOMSKO DELO Univerzitetni študij THE
Univerzitetni študij. University studies
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Blaž NEMANIČ ZAŠČITA PRED OKSIDATIVNIM STRESOM ŠPORTNIH KONJ DIPLOMSKO DELO Univerzitetni študij DEFENCE MECHANISMS AGAINST OXIDATIVE STRESS
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ZOOTEHNIKO Blaž NEMANIČ ZAŠČITA PRED OKSIDATIVNIM STRESOM ŠPORTNIH KONJ DIPLOMSKO DELO Univerzitetni študij DEFENCE MECHANISMS AGAINST OXIDATIVE STRESS
Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str Zreče, marec 2003
 Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 7-79 Zreče, 4. 6. marec 3 KEMIJSKO IN BIOTIČNO SLEDENJE ORGANSKIH FOSFORNIH PESTICIDOV V OKOLJU Polonca TREBŠE, Mojca
Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 7-79 Zreče, 4. 6. marec 3 KEMIJSKO IN BIOTIČNO SLEDENJE ORGANSKIH FOSFORNIH PESTICIDOV V OKOLJU Polonca TREBŠE, Mojca
VREDNOTENJE PREHRANE KARDIOVASKULARNIH BOLNIKOV
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Ana ŠERONA VREDNOTENJE PREHRANE KARDIOVASKULARNIH BOLNIKOV DIPLOMSKO DELO Univerzitetni študij Ljubljana, 2009 UNIVERZA V LJUBLJANI BIOTEHNIŠKA
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA ŽIVILSTVO Ana ŠERONA VREDNOTENJE PREHRANE KARDIOVASKULARNIH BOLNIKOV DIPLOMSKO DELO Univerzitetni študij Ljubljana, 2009 UNIVERZA V LJUBLJANI BIOTEHNIŠKA
VPLIV POVEČANEGA UV-B SEVANJA NA AKTIVNOST SMREKE (Picea abies) IN TVORBO ZAŠČITNIH SNOVI
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA BIOLOGIJO Tadeja TROŠT, univ. dipl. biol. VPLIV POVEČANEGA UV-B SEVANJA NA AKTIVNOST SMREKE (Picea abies) IN TVORBO ZAŠČITNIH SNOVI MAGISTRSKO DELO
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ODDELEK ZA BIOLOGIJO Tadeja TROŠT, univ. dipl. biol. VPLIV POVEČANEGA UV-B SEVANJA NA AKTIVNOST SMREKE (Picea abies) IN TVORBO ZAŠČITNIH SNOVI MAGISTRSKO DELO
ANALIZA MOLEKULSKIH MEHANIZMOV DELOVANJA FENILBUTIRATA, FENILACETATA IN NIKOTINA NA KVASOVKO Saccharomyces cerevisiae
 UNIVERZA V NOVI GORICI FAKULTETA ZA ZNANOSTI O OKOLJU Katjuša REJA MOZETIČ ANALIZA MOLEKULSKIH MEHANIZMOV DELOVANJA FENILBUTIRATA, FENILACETATA IN NIKOTINA NA KVASOVKO Saccharomyces cerevisiae DIPLOMSKO
UNIVERZA V NOVI GORICI FAKULTETA ZA ZNANOSTI O OKOLJU Katjuša REJA MOZETIČ ANALIZA MOLEKULSKIH MEHANIZMOV DELOVANJA FENILBUTIRATA, FENILACETATA IN NIKOTINA NA KVASOVKO Saccharomyces cerevisiae DIPLOMSKO
Varnostni list. ODDELEK 1:Identifikacijasnovi/zmesiindružbe/podjetja. Oznaka izdelka. A10026COMPONENTE dimethylsulfoxide (DMSO)
 Varnostni list (vskladuzuredbo KOMISIJE(EU)št.453/2010) Oznaka izdelka ODDELEK 1:Identifikacijasnovi/zmesiindružbe/podjetja Ime izdelka Registracijskaštevilka REACH dimethylsulfoxide (DMSO) Tasnov/tesnovivtejzmesinima/-joregistrskeštevilke,kerjeletnauvozna
Varnostni list (vskladuzuredbo KOMISIJE(EU)št.453/2010) Oznaka izdelka ODDELEK 1:Identifikacijasnovi/zmesiindružbe/podjetja Ime izdelka Registracijskaštevilka REACH dimethylsulfoxide (DMSO) Tasnov/tesnovivtejzmesinima/-joregistrskeštevilke,kerjeletnauvozna
UGOTAVLJANJE PRISOTNOSTI EKOTIPOV KRANJSKE ČEBELE (Apis mellifera carnica Pollman) V SLOVENIJI NA PODLAGI RAZLIK V OŽILJENOSTI PREDNJIH KRIL
 Acta agriculturae Slovenica, 92(december 2008)2, 139 149. http://aas.bf.uni-lj.si Agris category codes: L10 COBISS Code 1.01 UGOTAVLJANJE PRISOTNOSTI EKOTIPOV KRANJSKE ČEBELE (Apis mellifera carnica Pollman)
Acta agriculturae Slovenica, 92(december 2008)2, 139 149. http://aas.bf.uni-lj.si Agris category codes: L10 COBISS Code 1.01 UGOTAVLJANJE PRISOTNOSTI EKOTIPOV KRANJSKE ČEBELE (Apis mellifera carnica Pollman)
Izvleček. Abstract. Namen: Cilj te raziskave je bil ugotoviti,
 Vpliv enostavne intervencije na večje upoštevanje smernic pri zdravljenju bolnic z nezapleteno okužbo spodnjih sečil v dežurnih ambulantah na primarni ravni Increased adherence to treatment guidelines
Vpliv enostavne intervencije na večje upoštevanje smernic pri zdravljenju bolnic z nezapleteno okužbo spodnjih sečil v dežurnih ambulantah na primarni ravni Increased adherence to treatment guidelines
Damir FRANIC 1*, Ivan VERDENIK 2. Outpatient Clinic for Obstetrics and Gynecology, Celjska cesta 10, 3250 Rogaska Slatina, Slovenia 2
 Franic D, Verdenik I. Risk factors for osteoporosis in postmenopausal women from the point of view of primary care gynecologist. Zdr Varst. 2018;57(1):33-38. doi: 10.2478/sjph-2018-0005. RISK FACTORS FOR
Franic D, Verdenik I. Risk factors for osteoporosis in postmenopausal women from the point of view of primary care gynecologist. Zdr Varst. 2018;57(1):33-38. doi: 10.2478/sjph-2018-0005. RISK FACTORS FOR
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MARJANA PRAH KRUMPAK MAGISTRSKA NALOGA. Magistrski študij laboratorijske biomedicine
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MARJANA PRAH KRUMPAK MAGISTRSKA NALOGA Magistrski študij laboratorijske biomedicine Ljubljana, 2012 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MARJANA PRAH
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MARJANA PRAH KRUMPAK MAGISTRSKA NALOGA Magistrski študij laboratorijske biomedicine Ljubljana, 2012 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO MARJANA PRAH
PRIVZEM KOVIN IN SELENA V TATARSKI AJDI (Fagopyrum tataricum Gaertn.) IN NJENA VLOGA PRI FITOREMEDIACIJI TAL
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Petra ŠTREKELJ PRIVZEM KOVIN IN SELENA V TATARSKI AJDI (Fagopyrum tataricum Gaertn.) IN NJENA VLOGA PRI FITOREMEDIACIJI TAL DOKTORSKA DISERTACIJA Ljubljana, 2015
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA Petra ŠTREKELJ PRIVZEM KOVIN IN SELENA V TATARSKI AJDI (Fagopyrum tataricum Gaertn.) IN NJENA VLOGA PRI FITOREMEDIACIJI TAL DOKTORSKA DISERTACIJA Ljubljana, 2015
INSEKTICIDNO DELOVANJE PETIH ETERIČNIH OLJ NA ODRASLE OSEBKE FIŽOLARJA (Acanthoscelides obtectus [Say], Coleoptera, Chrysomelidae)
![INSEKTICIDNO DELOVANJE PETIH ETERIČNIH OLJ NA ODRASLE OSEBKE FIŽOLARJA (Acanthoscelides obtectus [Say], Coleoptera, Chrysomelidae) INSEKTICIDNO DELOVANJE PETIH ETERIČNIH OLJ NA ODRASLE OSEBKE FIŽOLARJA (Acanthoscelides obtectus [Say], Coleoptera, Chrysomelidae)](/thumbs/91/106860994.jpg) INSEKTICIDNO DELOVANJE PETIH ETERIČNIH OLJ NA ODRASLE OSEBKE FIŽOLARJA (Acanthoscelides obtectus [Say], Coleoptera, Chrysomelidae) Tanja BOHINC 1, Stanislav TRDAN 2 1,2 Biotehniška fakulteta, Oddelek za
INSEKTICIDNO DELOVANJE PETIH ETERIČNIH OLJ NA ODRASLE OSEBKE FIŽOLARJA (Acanthoscelides obtectus [Say], Coleoptera, Chrysomelidae) Tanja BOHINC 1, Stanislav TRDAN 2 1,2 Biotehniška fakulteta, Oddelek za
PREHRANA ŠPORTNIKA in REKREATIVCA. Asist. Dr. Urška Bukovnik Dr. biokem., mag. biotehn., IOC dipl. šport.prehr.
 PREHRANA ŠPORTNIKA in REKREATIVCA Asist. Dr. Urška Bukovnik Dr. biokem., mag. biotehn., IOC dipl. šport.prehr. 2 Vsebina predavanja 1.) HRANA KOT GORIVO 2.) MAKRO IN MIKROHRANILA - individualizacija in
PREHRANA ŠPORTNIKA in REKREATIVCA Asist. Dr. Urška Bukovnik Dr. biokem., mag. biotehn., IOC dipl. šport.prehr. 2 Vsebina predavanja 1.) HRANA KOT GORIVO 2.) MAKRO IN MIKROHRANILA - individualizacija in
