UNIVERZA V MARIBORU FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO DOKTORSKA DISERTACIJA
|
|
|
- Garey Jefferson
- 5 years ago
- Views:
Transcription
1 UNIVERZA V MARIBORU FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO DOKTORSKA DISERTACIJA DOLOČEVANJE SESTAVE MAŠČOBNIH KISLIN IN NJIHOVIH PROFILOV V MEMBRANAH RDEČIH KRVNIH CELIC BOLNIKOV Z RAZLIČNIMI BOLEZNIMI Z METODO PLINSKE KROMATOGRAFIJE junij, 2011 Zdenka CENCIČ KODBA
2 DOKTORSKA DISERTACIJA DOLOČEVANJE SESTAVE MAŠČOBNIH KISLIN IN NJIHOVIH PROFILOV V MEMBRANAH RDEČIH KRVNIH CELIC BOLNIKOV Z RAZLIČNIMI BOLEZNIMI Z METODO PLINSKE KROMATOGRAFIJE DOCTORAL DISSERTATION DETERMINATION OF RED CELL MEMBRANE FATTY ACID PROFILES IN PATIENTS WITH DIFFERENT DISEASES WITH GAS CHROMATOGRAPHY junij, 2011 Zdenka Cencič Kodba Mentor: red. prof. dr. Darinka Brodnjak Vončina Somentor: izred. prof. dr. Lucija Zupančič - Kralj
3 i
4 SKLEP SENATA UM FKKT O ZAGOVORU ii
5 iii To, kar vemo, je kapljica, to, č esar ne vemo, je morje. Newton ZAHVALA Zahvaljujem se mentorici prof. dr. Darinki Brodnjak Vončini za vodenje, strokovno pomoč, nasvete in vzpodbude pri izdelavi doktorske naloge. Za somentorstvo se zahvaljujem prof. dr. Luciji Zupančič- Kralj. Za strokovno usmerjanje in vsestranske nasvete se zahvaljujem doc. dr. Ernestu Vončini. Za sodelovanje se zahvaljujem prof. dr. Urošu Potočniku. Zahvaljujem se tehnični sodelavki ge. Alenki Lednik za pomoč v laboratoriju. Nenazadnje se zahvaljujem družini in vsem drugim, ki so mi pomagali, pa jih nisem omenila.
6 iv KLJUČNA DOKUMENTACIJSKA INFORMACIJA ŠD Dn DK UDK: : (043.3) KG rdeče krvne celice, eritrociti, celične membrane, fosfolipidi, maščobne kisline, profili maščobnih kislin, plazmalogeni, plinska kromatografija, tankoplastna kromatografija, metoda glavnih osi, klasifikacija AV CENCIČ KODBA, Zdenka SA BRODNJAK VONČINA, Darinka (mentorica) ZUPANČIČ KRALJ, Lucija (somentorica) KZ SI-2000 Maribor, Smetanova 17 ZA Univerza v Mariboru, Fakulteta za kemijo in kemijsko tehnologijo LI 2011 IN DOLOČEVANJE SESTAVE MAŠČOBNIH KISLIN IN NJIHOVIH PROFILOV V MEMBRANAH RDEČIH KRVNIH CELIC BOLNIKOV Z RAZLIČNIMI BOLEZNIMI Z METODO PLINSKE KROMATOGRAFIJE TD Doktorska disertacija OP 147 str., 23 pregl., 108 sl., 1 pril., 85 vir. IJ sl JI SI/en POVZETEK V doktorski disertaciji sem primerjala sestave maščobnih kislin in njihove karakteristične profile izoliranih fosfolipidov membran rdečih krvnih celic bolnikov z različnimi boleznimi z namenom, da bi preverila hipotezo, da so razlike med profili maščobnih kislin pomembne pri prepoznavanju različnih bolezenskih stanj oziroma motenj v metabolizmu. V študijo sem vključila vzorce krvi 272 bolnikov, od tega 135 bolnikov s kronično vnetno črevesno boleznijo (60 bolnikov s Crohnovo črevesno boleznijo in 75 bolnikov z drugimi vnetnimi črevesnimi boleznimi), 18 bolnikov s črevesnimi polipi, 52 bolnikov z astmo, 53 bolnic z miomi na maternici ter 14 vzorcev krvi žensk, ki miomov nimajo. 70 zdravih ljudi, ki niso oboleli za nobeno od naštetih bolezni, je predstavljalo kontrolno skupino. Izbira bolnikov je bila naključna in neodvisna od njihovih prehranjevalnih navad ali prehranskih dodatkov lipidov. Uporabila sem robustno in natančno analizno metodo ekstrakcije lipidov, separacije lipidnih razredov in izolacije fosfolipidov na silikagel trdni fazi (SPE-Si), ki sem jo izboljšala in optimizirala. Izolaciji rdečih krvnih celic je sledila metoda postopne ekstrakcije tekoče-tekoče, s katero sem povečala izkoristek izoliranih celokupnih lipidov, ki sem jih z ekstrakcijo na trdni fazi ločila na nepolarne lipide in polarne fosfolipide. Optimizacijo izolacije fosfolipidov na trdni fazi sem izvedla z vzporednim preskušanjem in uporabo tankoplastne kromatografije (TLC). Umiljenju fosfolipidne frakcije je sledila esterifikacija v metanolni raztopini borovega trifluorida. Sestavo metilnih estrov maščobnih kislin (FAME) fosfolipidov rdečih krvnih celic sem določala s plinsko kromatografijo (GC) s plamensko ionizacijskim detektorjem (FID). V membranah rdečih krvnih celic sem določila tudi dva dimetil acetala (heksadekanal in oktadekanal dimetil acetal; 16:0 DMA in 18:0 DMA), ki sta merilo oksidacijske prizadetosti celičnih membranskih fosfolipidnih plazmalogenov, ki so pomembni lipidni antioksidanti. S kemometrijskimi in statističnimi metodami sem karakterizirala vzorce glede na sestavo in vsebnost maščobnih kislin in dimetil acetalov. Študija je potrdila, da obstajajo pri opisanih bolnikih razlike v sestavi maščobnih kislin, kar bi lahko uporabili za diagnostične presejalne teste, kjer bi maščobne kisline prevzele vlogo bioloških označevalcev bolezni. KLJUČNE BESEDE: rdeče krvne celice, eritrociti, celične membrane, fosfolipidi, maščobne kisline, profili maščobnih kislin, plazmalogeni, plinska kromatografija, tankoplastna kromatografija, metoda glavnih osi, klasifikacija.
7 v KEY WORD DOCUMENTATION DN Dd DC UDC: : (043.3) CX red blood cell, human erythrocytes, cell membranes, phospholipids, fatty acids, fatty acid profiles, plasmalogens, gas chromatography, thin layer chromatography, principal component analysis, classification. AU CENCIČ KODBA, Zdenka AA BRODNJAK VONČINA, Darinka (supervisor) ZUPANČIČ KRALJ, Lucija (co-supervisor) PP SI-2000 Maribor, Smetanova 17 PB University of Mariboru, Faculty of Chemistry and Chemical Engineering PY 2011 TI DETERMINATION OF RED CELL MEMBRANE FATTY ACID PROFILES IN PATIENTS WITH DIFFERENT DISEASES WITH GAS CHROMATOGRAPHY DT Doctoral Dissertation NO 147 p., 23 tab., 108 fig., 1 ann., 85 ref. LA sl AL SI/en ABSTRACT The dissertation presented here aims to compare the fatty acid composition and their characteristic profiles derived from erythrocyte phospholipids of patients with different diseases and to test the hypothesis that the changes in their profiles might be relevant to various diseases and metabolic abnormalities. The study sample consisted of 272 patients, among them 135 with inflammatory bowel disease (60 patients with Crohn disease and 75 patients with other inflammatory bowel diseases), 18 with colon adenomas, 52 with asthma, 53 with uterine leiomyoma, 14 with verified absence of uterine leiomyoma. 70 blood samples without any of mentioned diseases were used as a control group. A robust and reliable analytical method, additionally improved and optimised, was used for the lipid extraction, separation of lipid classes and isolation of phospholipids by silica solid phase (SPE-Si). After the isolation of erythrocytes from blood samples, the method of sequential liquid-liquid extraction was used to yield more isolated total lipids, which were then separated by solid phase extraction into non polar lipids and polar phospholipids. The phospholipid SPE isolation was optimised by thin layer chromatography (TLC). After the saponification of phospholipid fraction, the esterification process followed with boron trifluoride methanol reagent. The fatty acid methyl ester (FAME) composition of the total red blood cell phospholipid fraction was analyzed by gas chromatography (GC) with flame ionization detector (FID). Additionally, two fatty aldehyde dimethyl acetals (hexadecanal and octadecanal dimethyl acetals; 16:0 DMA and 18:0 DMA) derived from erythrocyte membrane plasmalogen phospholipids were also determined. Plasmalogens act as targets for oxidants and are major lipophilic antioxidants. The resulting fatty acids and plasmalogen linked dimethyl acetals were evaluated by chemometrics and statistical methods. The study suggests differences in membrane fatty acid profiles in patients with different diseases which might have a potential for diagnostics and population screening for diseases, where fatty acids may play role as biomarkers for diseases. KEY WORDS: red blood cell, human erythrocytes, cell membranes, phospholipids, fatty acids, fatty acid profiles, plasmalogens, gas chromatography, thin layer chromatography, principal component analysis, classification.
8 vi KAZALO VSEBINE SKLEP SENATA UM FKKT O ZAGOVORU... ii ZAHVALA... iii KLJUČNA DOKUMENTACIJSKA INFORMACIJA... iv POVZETEK... iv KEY WORD DOCUMENTATION... v ABSTRACT... v KAZALO VSEBINE... vi KAZALO SLIK... viii KAZALO PREGLEDNIC... xiii UPORABLJENE KRATICE... xiv UPORABLJENI SIMBOLI... xv NAMEN DOKTORSKE DISERTACIJE... xvi 1 TEORETIČNI DEL Lipidomika in celična fiziologija Uvod v lipide Lipidi, nomenklatura in strukturna pestrost lipidov Klasifikacija lipidov Maščobne acilne spojine Razredi in podrazredi maščobnih acilnih spojin (FA) Arahidonska kislina in vnetni biološki procesi Voski Glicerolipidi Glicerolipidni razredi in podrazredi Monoacilgliceroli (MAG) Diacilgliceroli (DAG) Triacilgliceroli (TAG) Glicerofosfolipidi Razredi glicerofosfolipidov Plazmalogeni - eterski lipidi Sfingolipidi Razredi sfingolipidov Sterolni lipidi Razredi in podrazredi sterolnih lipidov Prenolni lipidi Razredi in podrazredi prenolnih lipidov Celična membrana in strukturna organiziranost rdeče krvne celice DOLOČANJE LIPIDOV Ekstrakcija lipidov iz bioloških materialov Ekstrakcijska topila Primerjava ekstrakcijskih postopkov za izolacijo lipidov iz bioloških materialov Adsorpcijska kromatografija lipidnih razredov Izolacija lipidnih razredov s podobno polarnostjo Priprava metilnih estrov maščobnih kislin in dimetil acetalov z metanolno raztopino borovega trifluorida... 39
9 2.4.1 Kislinsko katalizirana esterifikacija in transesterifikacija Izolacija trans maščobnih kislin z ekstrakcijo na SPE Ag-Ion nosilcu EKSPERIMENTALNI DEL Materiali in metode Pribor in aparati Kemikalije in reagenti Priprava steklovine Ekstrakcijska topila Standardni materiali metilnih estrov maščobnih kislin Standardni materiali predstavnikov lipidnih razredov Priprava osnovnih standardnih raztopin lipidov Priprava delovne standardne raztopine lipidov Priprava vzorcev Etična ustreznost Izolacija eritrocitov Postopek ekstrakcije lipidov rdečih krvnih celic Shranjevanje lipidnih ekstraktov Izolacija fosfolipidov z ekstrakcijo na trdni fazi (SPE) Priprava metilnih estrov maščobnih kislin Plinska kromatografija Instrumentalni pogoji Določevanje maščobnih kislin fosfolipidov Metoda izračuna masnega deleža metilnih estrov maščobnih kislin Identifikacija maščobnih kislin Identifikacija dimetil acetalov Optimizacija ločevanja lipidnih razredov s TLC in SPE-Si Tankoplastna kromatografija (TLC) Preskušanje razvijalnih raztopin za TLC REZULTATI IN DISKUSIJA Opis vzorcev Statistična analiza podatkov Metoda glavnih osi (PCA) Ponovljivost metode Testi signifikantnosti Parametrični testi Izboljšava ekstrakcije lipidov iz rdečih krvnih celic Rezultati analiz vzorcev fosfolipidov rdečih krvnih celic ZAKLJUČEK PRILOGA LITERATURA IN VIRI ŽIVLJENJEPIS BIBLIOGRAFIJA vii
10 viii KAZALO SLIK Slika 1 1: Lipidna raznolikost in njihova številska zastopanost v človeški plazmi Slika 1 2: Struktura membranskih lipidov Slika 1 3: Značilni predstavniki posameznih lipidnih razredov Slika 1 4, a: Reprezentativne strukture maščobnih acilnih spojin Slika 1 4, b: Reprezentativne strukture maščobnih acilnih spojin Slika 1 4, c: Reprezentativne strukture maščobnih acilnih spojin Slika 1 5: Primer motenih dvojnih vezi z metilensko skupino Slika 1 6: Strukturni formuli linolne kisline (9-cis,12-cis-oktadekadienojske; 18:2n6) (LA) a) in α-linolenske lisline (9-cis,12-cis,15-cis-oktadekatrienojska; 18:3n3) (ALA) b) Slika 1 7: Prikaz biosinteze linolne (18:2n6) kisline (LA) in α-linolenske (18:3n3) kisline (ALA) Slika 1 8: Biosinteza omega-6 polinenasičenih maščobnih kislin Slika 1 9: Biosinteza omega-3 polinenasičenih maščobnih kislin Slika 1 10: Strukturna formula LA (linolna kislina; 18:2n6) Slika 1 11: Strukturna formula AA (arahidonska kislina; 20:4n6) Slika 1 12: Strukturna formula ALA (α-linolenska kislina; 18:3n3) Slika 1 13: Strukturna formula DHA (dokozaheksaenojska kislina; 22:6n3) Slika 1 14: Metabolizem esencialnih maščobnih kislin in nastanek eikozanoidov Slika 1 15: Strukturna formula estra voska Slika 1 16, a: Reprezentativne strukture glicerolipidov Slika 1 16, b: Reprezentativne strukture glicerolipidov Slika 1 17: Stereokemične oblike monoacilglicerolov Slika 1 18: Stereokemične oblike diacilglicerolov Slika 1 19: Fisherjeva projekcija triacil-sn-glicerola Slika 1 20: Strukturna formula soli fosfatidinske kisline Slika 1 21, a: Reprezentativne strukture glicerofosfolipidov Slika 1 21, b: Reprezentativne strukture glicerofosfolipidov Slika 1 22: Fosfatidilholin Slika 1 23: Fosfatidiletanolamin Slika 1 24: Fosfatidilserin Slika 1 25: Fosfatidilinozitol Slika 1 26: Plazmaniletanolamin (eter) Slika 1 27: Plazmeniletanolamin (vinil eter) Slika 1 28: Hidroliza plazmalogena in nastanek aldehida Slika 1 29: Dimetil acetal Slika 1 30: Sfingozin Slika 1 31: Sfingomielin Slika 1 32: Reprezentativne strukture sfingolipidov Slika 1 33, a: Reprezentativne strukture sterolnih lipidov Slika 1 33, b: Reprezentativne strukture sterolnih lipidov Slika 1 34, a: Reprezentativne strukture prenolnih lipidov Slika 1 34, b: Reprezentativne strukture prenolnih lipidov Slika 1 35: Shematski prikaz zgradbe celice in celične membrane Slika 1 36: Posnetek rdeče krvne celice (a), trombocita (b) in leukocita (c) z elektronskim mikroskopom
11 Slika 1 37: Prikaz asimetrične porazdelitve lipidov na zunanji in notranji strani membrane rdeče krvne celice Slika 2 1: Kislinsko katalizirana esterifikacija maščobnih kislin Slika 2 2: Kislinsko katalizirana transesterifikacija lipidov Slika 2 3: Shematski prikaz interakcij med Ag + in cis dvojnimi vezmi Slika 2 4: GC-FID kromatogram standardne raztopine Supelco 37 FAME Mix U a), kromatogram izoliranih nasičenih in trans monoen maščobnih kislin b), kromatogram izoliranih cis monoen maščobnih kislin in trans dien maščobnih kislin c), kromatogram izoliranih cis dien, cis/trans dien maščobnih kislin, trans trien ter cis/trans trien maščobnih kislin d), kromatogram izoliranih cis trien maščobnih kislin e) in kromatogram izoliranih cis tetraen, penta in heksaen maščobnih kislin f) Slika 2 5: GC-FID kromatogram rastlinskega olja a), kromatogram izoliranih nasičenih in trans monoenskih maščobnih kislin (18:1 trans izomere 1. frakcija) b), kromatogram izoliranih cis monoenskih maščobnih kislin (18:1 cis izomere 2. frakcija) c) Slika 3 1: Skvalen Slika 3 2: Stearil palmitat Slika 3 3: Holesteril stearat Slika 3 4: 3-Heksadekanon Slika 3 5: Gliceril tripalmitat Slika 3 6: Gliceril monopalmitat Slika 3 7: Palmitinska kislina Slika 3 8: Cetil alkohol Slika 3 9: Holesterol Slika 3 10: L-α-lecitin Slika 3 11: L-α kefalin Slika 3 12: 3-sn-fosfatidil-L-serin Slika 3 13: Sfingomielin Slika 3 14: Shematski prikaz vzorca krvi po centrifugiranju Slika 3 15: Prenos vzorca rdečih krvnih celic v epruveto a), dodajanje solnice in priprava»lizata«b), postopno dodajanje ekstrakcijskih topil c) Slika 3 16: Prenos epruvet v centrifugo a), vzorci po centrifugiranju b), prenos lipidnega ekstrakta v kloroformu c) Slika 3 17: V epruveti A in C je vzorec eritrocitov pred in po centrifugiranju, pripravljen po postopnem dodajanju topil metanola (2,5 ml) in kloroforma (5 ml) Slika 3 18: Lipidni ekstrakt v kloroformu a), postopek kondicioniranja SPE b), nanos ekstrakta na SPE c) Slika 3 19: Alkalna hidroliza fosfolipidov v grelnem bloku a), dodajanje heksana b), dodajanje nasičene raztopine natrijevega klorida c) Slika 3 20: GC-FID kromatogram standardne raztopine mešanice 37 metilnih estrov maščobnih kislin. (Supelco 37 FAME Mix U), mešanice cis/trans izomer 18:1 kisline (Restek cis/trans FAME Mix 35079), mešanice cis/trans izomer 18:2 kislin (Supelco 18:2 (linolna) cis/trans FAME Mix 47791) in mešanice cis/trans izomer 18:3 kislin (Supelco 18:3 (linolenska) cis/trans FAME Mix 47792) Slika 3 21: GC-FID kromatogram standardne raztopine mešanice 37 metilnih estrov maščobnih kislin (Supelco 37 FAME Mix U). Identifikacija kromatografskih ix
12 vrhov: (1) 4:0, (2) 6:0, (3) 8:0, (4) 10:0, (5) 11:0, (6) 12:0, (7) 13:0, (8) 14:0, (9) 14:1n5, (10) 15:0, (11) 15:1n5, (12) 16:0, (13) 16:1n7, (14) 17:0, (15) 17:1n7, (16) 18:0, (17) 18:1n9t, (18) 18:1n9c, (19) 18:2n6t, (20) 18:2n6c, (21) 20:0, (22) 18:3n6 GLA, (23) 20:1n9, (24) 18:3n3 ALA, (25) 21:0, (26) 20:2n6, (27) 22:0, (28) 20:3n6 DGLA, (29) 22:1n9, (30) 20:3n3, (31) 20:4n6 AA, (32) 23:0, (33) 22:2n6, (34) 24:0, (35) 20:5n3 EPA, (36) 24:1n9, (37) 22:6n3 DHA Slika 3 22: GC-FID kromatogram standardne raztopine mešanice cis/trans izomer 18:1 kislin (Restek cis/trans FAME Mix 35079). Identifikacija kromatografskih vrhov: (1) 18:0, (2) 18:1n12t, (3) 18:1n9t, (4) 18:1n7t, (5) 18:1n12c, (6) 18:1n9c, (7) 18:1n7c, (8) 18:2n Slika 3 23: GC-FID kromatogram standardne mešanice cis/trans izomer 18:2 kislin (Supelco 18:2 (linolna) cis/trans FAME Mix 47791). Identifikacija kromatografskih vrhov: (1) 18:2n6t, (2) 18:2-9c12t, (3) 18:2-9t12c, (4) 18:2n6c. 58 Slika 3 24: GC-FID kromatogram standardne mešanice cis/trans izomer 18:3 kislin (Supelco 18:3 (linolenska) cis/trans FAME Mix 47792). Identifikacija kromatografskih vrhov: (1) 18:3n3t, (2) 18:3-9t12t15c, (3) 18:3-9t12c15t, (4) 18:3-9c12t15t, (5) 18:3-9c12c15t, (6) 18:3-9c12t15c, (7) 18:3-9t12c15c, (8) 18:3n3c ALA Slika 3 25: GC-MS kromatogrami izbranih fragmentnih ionov (za heksadekanal dimetil acetal (16:0 DMA) in oktadekanal dimetil acetal (18:0 DMA) (m/z = 75, m/z = 255 in m/z = 283)) ekstrakta fosfolipidov rdečih krvnih celic Slika 3 26: Masni spekter heksadekanal dimetil acetala (16:0 DMA) z značilnim fragmentnim ionom m/z = 75 (CH(CH 3 O) 2 + ) in m/z = 255 (M + = 286) Slika 3 27: Masni spekter oktadekanal dimetil acetala (18:0 DMA) z značilnim fragmentnim ionom m/z = 75 (CH(CH 3 O) 2 + ) in m/z = 283 (M + = 314) Slika 3 28: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini Slika 3 29: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini Slika 3 30: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini Slika 3 31: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini Slika 3 32: TLC-2D kromatogram ločevanja standardnih raztopin lipidov. Plošča je najprej razvita v smeri a) z raztopino heksan-dietileter (65:35, v/v), nato v smeri b) z raztopino heksan-dietileter (65:35, v/v) in nato v smeri c) z raztopino kloroformmetanol-voda (65:25:4, v/v/v) Slika 3 33: TLC kromatogram standardnih raztopin lipidov v primerjavi s spojinami, ki jih dobim po ločevanju s SPE-Si Slika 3 34: GC-FID kromatogram eluata I (prisoten metilni ester palmitinske kisline) a) in eluata II (metil ester palmitinske kisline ni prisoten) b) Slika 3 35: TLC-2D kromatogram (vzorec: surov lipidni ekstrakt eritrocitov) Slika 3 36: TLC-2D kromatogram (vzorec: eluat I) Slika 3 37: TLC-2D kromatogram (vzorec: eluat II) Slika 4 1: GC-FID kromatogram FAME in DMA fosfolipidov rdečih krvnih celic. Identifikacija kromatografskih vrhov: (1) 14:0, (2) 15:0, (3) 16:0, (4) 16:0 DMA, (5) 16:1n7, (6) 17:0, (7) 18:0, (8) 18:0 DMA, (9) sum18:1 trans, (10) 18:1n9, (11) 18:1n7, (12) 18:2n6, (13) 20:0, (14) 18:3(9t, 12c, 15t), (15) 18:3n6 GLA, (16) 20:1n9, (17) 18:3n3 ALA, (18) 18:4n3 STD, (19) 20:2n6, (20) 22:0, (21) 20:3n6 DGLA, (22) 22:1n9, (23) 20:4n6 AA, (24) 20:5n3 EPA, (25) 24:0, (26) 24:1n9, (27) 22:4n6, (28) 22:5n6, (29) 22:5n3 DPA, (30) 22:6n3 DHA x
13 Slika 4 2: Rezultat 342 vzorcev in 39 spremenljivk v PC1 PC2 koordinatnem sistemu Slika 4 3: Faktorji vsebnosti (»loadings«) 342 vzorcev in 39 spremenljivk v PC1 PC2 koordinatnem sistemu Slika 4 4: Razmerje vsebnosti vsote nasičenih maščobnih kislin (S) in arahidonske (20:4n6) kisline (AA) (r = - 0,964) Slika 4 5: Razmerje vsebnosti vsote nasičenih maščobnih kislin (S) in adrenske (22:4n6) kisline (r = - 0,902) Slika 4 6: Razmerje vsebnosti palmitinske (16:0) kisline in vsote omega-6 polinenasičenih maščobnih kislin Slika 4 7: Vsebnost linolne (18:2n6) kisline pri 342 donorjih (za sedem skupin bolnikov z oznakami od 1 do 6 in kontrolno skupino z oznako 0) Slika 4 8: Vsebnost polinenasičenih kislin (P) pri 342 donorjih (kontrolni vzorci in bolniki) Slika 4 9: Vsebnost omega-3 kislin (n3) pri 342 donorjih (kontrolni vzorci in bolniki) Slika 4 10: Vsebnost omega-6 kislin (n6) pri 342 donorjih (kontrolni vzorci in bolniki) Slika 4 11: Vsebnost razmerij omega-3 in omega-6 kislin (n3 / n6) pri 342 donorjih (kontrolni vzorci in bolniki) Slika 4 12: Vsebnosti maščobnih kislin 342 donorjev glede na najbolj diskriminatorne spremenljivke (palmitinska (16:0) kislina, linolna (18:2n6) kislina in vsota polinenasičenih maščobnih kislin (P)) Slika 4 13: Profili maščobnih kislin bolnikov z različnimi boleznimi v primerjavi s kontrolno skupino KON(0) ( ) (izraženi v masnem deležu (%) in logaritmu masnega deleža) Slika 4 14: Profili maščobnih kislin bolnic z miomi maternice, bolnic brez miomov maternice in kontrolno skupino KON(0) (izraženi v masnem deležu (%) in logaritmu masnega deleža) Slika 4 15: Vsebnost stearinske (18:0) kisline pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 16: Vsebnost linolne (18:2n6) kisline pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 17: Vsebnost arahidonske (20:4n6) kisline pri bolnicah z miomi (3, 31- podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 18: Vsebnost adrenske (22:4n6) kisline pri bolnicah z miomi (3, 31- podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 19: Vsebnost omega-3 kislin pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 20: Vsebnost razmerja omega-3 in omega-6 kislin pri bolnicah miomi (3, 31- podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 21: Vsebnost 16:0 DMA pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) Slika 4 22: Vsebnost 18:0 DMA pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0) xi
14 Slika 4 23: Razmerja 16:0 dimetil acetala in palmitinske (16:0) kisline ( ) ter 18:0 dimetil acetala ter stearinske (18:0) kisline ( ) v vzorcih bolnikov z različnimi boleznimi v primerjavi s kontrolno skupino xii
15 xiii KAZALO PREGLEDNIC Preglednica 1 1: Kategorije lipidov s primeri Preglednica 1 2: Seznam nasičenih maščobnih kislin (SFA) Preglednica 1 3: Seznam mononenasičenih maščobnih kislin (MUFA) Preglednica 1 4: Seznam polinenasičenih (PUFA) maščobnih kislin Preglednica 1 5: Tri esencialne kisline C20 in eikozanoidi, ki iz njih nastajajo Preglednica 2 1: Lastnosti SPE nosilcev Preglednica 2 2: Ločevanje maščobnih kislin glede na število in cis/trans izomerizacijo dvojnih vezi na SPE Ag-Ion kolonah Preglednica 3 1: Ločitev fosfolipidov (PL) na SPE-Si koloni Preglednica 3 2: Ločevanje trans maščobnih kislin (TFA) na SPE Ag-Ion Preglednica 4 1: Lastnosti in oznake vzorcev krvi Preglednica 4 2: Seznam maščobnih kislin in dimetil acetalov določenih v fosfolipidih membran rdečih krvnih celic Preglednica 4 3:. Sestava maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) 39 spremenljivk pri 23 bolnikih KVČB(5) z oznakami od zaporedne številke 180 do 202. Števka 1 pomeni analitika 1 (opravil analizo 23 vzorcev z zaporedno številko od 180 do 202), števka 2 pa analitika 2 (opravil analizo 23 vzorcev z zaporedno številko od 180 do 202) Preglednica 4 4: ANOVA F-test za linolno (18:2n6) kislino Preglednica 4 5: Parni t-test dveh setov meritev dveh analitikov za linolno (18:2n6) kislino Preglednica 4 6: ANOVA F-test za linolno (18:2n6) kislino za vseh sedem skupin Preglednica 4 7: Rezultati t-testa primerjave povprečnih vrednosti različnih skupin vzorcev Preglednica 4 8: Primerjava povprečnih vrednosti meritev posamezne spremenljivke (S) med skupinama KVČB-I(1) in KVČB-II(5) Preglednica 4 9: Primerjava ekstrakcije lipidov po izboljšani metodi in konvencionalni metodi po Folchu Preglednica 4 11: Vrednosti medsebojnih korelacijskih koeficientov 39 spremenljivk maščobnih kislin in njihovih razmerij Preglednica 4 12: Povprečne vsebnosti sestav maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) za donorje KVČB-I(1), AST(2), GIN(3), GIN(KON)(4), KVČB-II(5), POL(6) in KON(0) kontrolne vzorce Preglednica 4 13: Povprečne vsebnosti sestav maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) za donorje GIN(3), GIN(3)-podskupina, GIN(KON)(4), GIN(KON)(4)-podskupina in KON(0) kontrolne vzorce Preglednica 4 14: Povprečne vrednosti razmerij dimetil acetalov in njihovih pripadajočih kislin (16:0 DMA in palmitinska (16:0) kislina ter 18:0 DMA ter stearinska (18:0) kislina) v fosfolipidih rdečih krvnih celic (masni delež, %) za donorje KVČB-I(1), AST(2), GIN(3), GIN(3) podskupina, GIN(KON)(4), GIN(KON)(4) podskupina, KVČB-II(5), POL(6) in KON(0) kontrolne vzorce Preglednica 4 10: Sestave maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) 342 vzorcev z oznakami 1, 2, 3, 4, 5, 0 in 6 glede na izbrane bolezni
16 xiv UPORABLJENE KRATICE FA FFA FAME LA AA EPA DHA GL TAG DAG MAG WE HC SE KET FAO GP PL PC PE PI PG PS SP SM ST HST PR SL PK DMA TLC SPE GC GC-MS SIM HPLC UPLC CAS maščobna kislina (angl. Fatty acid) proste maščobne kisline (angl. Free fatty acids) metilni estri maščobnih kislin (angl. Fatty acid methyl esters) linolna kislina (angl. Linoleic acid; 18:2n6) arahidonska kislina (angl. Arachidonic acid; 20:4n6) eikozapentaenojska kislina (angl. Eicosapentaenoic acid; 20:5n3) dokozaheksaenojska kislina (angl. Docosahexaenoic acid; 22:6n3) glicerolipidi (angl. Glycerolipids) triacilgliceroli (angl. Triacylglycerols) diacilgliceroli (angl. Diacylglycerols) monoacilgliceroli (angl. Monoacylglycerols) estri voskov (angl. Wax esters) alifatski ogljikovodiki (angl. Hydrocarbons) sterolni estri (angl. Sterol esters, Acylated sterols) ketoni (angl. Ketones) maščobni alkoholi (angl. Fatty alcohol) glicerofosfolipidi (angl. Glycerophospholipids) fosfolipidi (angl. Phospholipids) holin glicerofosfolipid (angl. Phosphatidylcholine) etanolamin glicerofosfolipid (angl. Etanolamin glycerophospholipid, Phosphatidylethanolamine) inozitol glicerofosfolipid (angl. Inositol glycerophospholipid, Phosphatidylinositol) glicerol glicerofosfolipid (angl. Glycerol glycerophospholipid, Phosphatidylglycerol) serin glicerofosfolipid (angl. Serine glycerophospholipid, Phosphatidylserine) sfingolipidi (angl. Sphingolipids) fosfosfingolipid sfingomielin (angl. phosphosphingolipid sphyngomyelin) sterolni lipidi (angl. Sterol lipids) holesterol (angl. Cholesterol) prenolni lipidi (angl. Prenol lipids) saharolipidi (angl. Saccharolipids) poliketidi (angl. Polyketides) dimetil acetali (angl. Dimethylacetals) tankoplastna kromatografija (angl. Thin layer chromatography) ekstrakcija na trdni fazi (angl. Solid phase extraction) plinska kromatografija (angl. Gas chromatography) plinska kromatografija z masno sprektrometrijo (angl. Gas chromatography with mass spectrometry) merjenje ionskega toka izbranih ionov (angl. Selected ion monitoring) tekočinska kromatografija visoke ločljivosti (angl. High performance liquid chromatography) tekočinska kromatografija ultra visoke ločljivosti (angl. Ultra performance liquid chromatography) (angl. Chemical Abstract Service)
17 xv Rf retencijski faktor (angl. Retention factor) P/N kataloška številka (angl. Part number) SFA nasičene maščobne kisline (angl. Saturated fatty acids) MUFA mononenasičene maščobne kisline (angl. Monounsaturated fatty acids) PUFA polinenasičene maščobne kisline (angl. Polyunsaturated fatty acids) TFA trans maščobne kisline (angl. Trans fatty acids) n-3 PUFA n-3 polinenasičene maščobne kisline (angl. n-3 polyunsaturated fatty acids) n-6 PUFA n-6 polinenasičene maščobne kisline (angl. n-6 polyunsaturated fatty acids) S vsota nasičenih maščobnih kislin (angl. Sum of saturated fatty acids-sfa) M vsota mononenasičenih maščobnih kislin (angl. Sum of monounsaturated fatty acids-mufa) P vsota polinenasičenih maščobnih kislin (angl. Sum of polyunsaturated fatty acids-pufa) T vsota trans maščobnih kislin (angl. Sum of trans fatty acids-tfa) n3 vsota n-3 polinenasičenih maščobnih kislin (angl. Sum of n-3 polyunsaturated fatty acids) n6 vsota n-6 polinenasičenih maščobnih kislin (angl. Sum of n-6 polyunsaturated fatty acids) PBS fosfatni pufer (angl. Phosphate buffered saline) PCA metoda glavnih osi (angl. Principal component analysis) ANOVA analiza varianc (angl. Analysis of variace) UPORABLJENI SIMBOLI w masni delež % s standardni odmik RSD relativni standardni odmik I.D. notranji premer mm
18 xvi NAMEN DOKTORSKE DISERTACIJE Namen doktorske disertacije z naslovom»določevanje sestave maščobnih kislin in njihovih profilov v membranah rdečih krvnih celic bolnikov z različnimi boleznimi z metodo plinske kromatografije«je bil poiskati povezave, podobnosti in odstopanja med sestavo maščobnih kislin membranskih fosfolipidov rdečih krvnih celic pri ljudeh z različnimi boleznimi. V doktorski disertaciji sem se osredotočila na maščobne kisline membran rdečih krvnih celic, čeprav bi lahko spremljala sestavo maščobnih kislin v plazmi. Te se zaradi trenutnega vnosa maščob iz prehrane spreminjajo hitreje, zato je plazma za študijo manj primerna. Najpomembnejša funkcija lipidov v bioloških sistemih je tvorba membranske fosfolipidne dvojne plasti. To je struktura, ki predstavlja mejo med celicami in ločuje zunanji del celice od notranjosti. Ta membranska dvojna plast omogoča celicam strukturo in ustvarja pogoje za njihovo delovanje. Strukturne spremembe fosfolipidov lahko vplivajo na spremembo membrane in posledično na funkcijo celice. Študija lipidov v naravnem okolju se imenuje»lipidomika«, ki je novejše študijsko področje in obravnava vlogo specifičnih lipidov pri fizioloških in bolezenskih stanjih. Vse informacije, ki se nanašajo na kontrolne procese lipidov pri celičnih procesih, lahko odpirajo nova terapevtska področja. Znanstveni prispevki s področja študij membran kažejo na pomembnost izbrane problematike in iskanja bioloških označevalcev kroničnih bolezni. Večina študij obravnava vnose različnih skupin maščobnih kislin v prehranjevalno verigo in spremljanje njihove vgradnje v celične membrane. Izbira bolnikov je bila naključna in neodvisna od njihovih prehranjevalnih navad ali prehranskih dodatkov lipidov. V doktorski disertaciji sem želela preveriti hipotezo, da so razlike v sestavi maščobnih kislin celičnih membranskih lipidov v povezavi z izbranimi boleznimi. S spremljanjem sestave maščobnih kislin sem želela slediti različnim bolezenskim stanjem ter motnjam v metabolizmu. S tem bi predstavila nove možnosti za nadaljnje študije presejalnega testa pri diagnosticiranju bolezni. Trenutno se uporabljajo različne metode ekstrakcij, izolacij in določevanja maščobnih kislin v različnih bioloških matricah (tkivo, plazma, rdeče krvne celice). Metodo ekstrakcije celokupnih lipidov sem izboljšala s postopkom kontinuiranega in postopnega dodajanja ekstrakcijskih topil. Analizna metoda je robustna in zanesljiva ter je uporabna za rutinske analize maščobnih kislin v izoliranih fosfolipidih membran rdečih krvnih celic.
19 T e o r e t i č n i d e l 1 TEORETIČNI DEL 1.1 Lipidomika in celična fiziologija V sklopu genomike in proteomike je analitika lipidov lipidomika nujna za razumevanje celične fiziologije. Biologija lipidov je po genomiki postala ciljno raziskovalno področje. Lipidomiko lahko definiramo kot študijo poti in mrež celičnih lipidov v bioloških sistemih. Proučuje lipidne razrede, njihovo spremembo v metabolizmu in signalne lipidne procese v celici, tkivu ali organizmu. Lipidomika je mlajše raziskovalno področje in se razvija z napredkom tehnologije (predvsem masne spektrometrije) v povezavi z razumevanjem vloge lipidov pri številnih metabolnih boleznih, kot so debelost, ateroskleroza, kap, visok tlak, diabetes, rak, artritis ter Alzheimerjevi in drugih z lipidi povezanih boleznih. Študij lipidomike vključuje identifikacijo in kvantifikacijo tisočih lipidnih molekul in njihovih medsebojnih interakcij, študij struktur, funkcije in dinamiko celičnih lipidov ter spremembe, ki nastajajo v primeru motenj biološkega sistema. Področje lipidomike sta prva definirala Han in Gross (Han, 2003). Čeprav je to področje pod okriljem bolj splošne metabolomike, ki pokriva še sladkorje, nukleotide in aminokisline, se loči od ostalih prav po svoji enkratnosti in funkcionalni specifičnosti. S študijem lipidomike dobimo vpogled v spremembe celične funkcionalnosti ter definicijo biokemičnih mehanizmov pri boleznih, ki so povezane z lipidi zaradi sprememb celično lipidnega metabolizma. Leta 2003 je bil ustanovljen konzorcij»lipid MAPS - Lipid Metabolites And Pathways Strategy«z namenom identifikacije in kvantifikacije lipidov v celicah sesalcev. Cilji konzorcija so popisati že znane lipide in identificirati nove, ter vzpostavitev bioinformatike in dinamične lipidne mreže. Trenutno obstaja nekaj študij na področju lipidomike bioloških materialov (Sandra, 2010), (Camera, 2010), (Quenhenberger, 2010), kjer uspešno identificirajo nekatere lipidome v človeški plazmi standardnega referenčnega materiala. Ugotovili so, da vsebuje plazma več tisoč različnih lipidnih molekul. Celokupno je bilo kvantificiranih 588 lipidov izmed šestih razredov: maščobni acili, glicerolipidi, glicerofosfolipidi, sfingolipidi, sterolni lipidi in prenolni lipidi. Število posameznih lipidov, ki so klasificirani v razrede, je razvidno iz Slike 1-1. Od maščobnih kislin je najbolj zastopana oleinska (18:1n9) kislina, ki ji sledita palmitinska (16:0) kislina in stearinska (18:0) kislina. Te predstavljajo približno 78 % vseh maščobnih kislin. Linolna (18:2n6) kislina in arahidonska (20:4n6) kislina (AA) sta najpomembnejši polinenasičeni maščobni kislini (PUFA). Prehrambeno nujne α- linolenska (18:3n3) kislina (ALA), eikozapentaenojska (20:5n3) kislina (EPA) in dokozaheksaenojska (22:6n3) kislina (DHA) predstavljajo do 1 % vseh maščobnih kislin. Lipidomika omogoča dostop do razumevanja biologije lipidov. 1
20 T e o r e t i č n i d e l Slika 1 1: Lipidna raznolikost in njihova številska zastopanost v človeški plazmi. Obstoječi profil lipidomov standardnega referenčnega materiala plazme lahko primerjamo s profilom bolnikov ali s tistimi, ki so na dieti. Trenutno so le holesterol in trigliceridi ter v novejšem času še vitamin D ovrednoteni za namene medicinske diagnostike. V primerih številnih metabolnih bolezni, kjer je vzrok genetika ali prehrana, je lipidni metabolizem zelo pomemben (npr. diabetes tipa 2, kardiovaskularne bolezni, avtoimune motnje, revmatoidni artritis, nevrodegenerativne bolezni, jetrne in ledvične motnje). Razen tega, da so gradniki membran celic in organel, so lipidi tudi zaloga energije, uravnavajo pa tudi metabolno regulacijo in funkcijo sporočanja signaliziranja. Analiza bolnikovih lipidomov bo v prihodnosti klinične medicine omogočala dragocen pristop k določanju in spremljanju bolezenskih stanj in učinkovitosti zdravljenja. 1.2 Uvod v lipide Lipidi (maščobe) so eni od štirih pomembnih sestavin bioloških organizmov, med katere uvrščamo še nukleinske kisline, amino kisline (proteini) in ogljikove hidrate (sladkorji). Celični lipidom vključuje več kot tisoč različnih lipidov (termin lipidom zajema celokupne lipide v celici), čeprav ponavadi slišimo le za podrazrede kot sta holesterol in trigliceridi. Še danes povsem ne vemo, kako se lipidi spreminjajo glede na raznolikost prehrane, diete in stila življenja. Večina lipidov je med seboj podobnih in jih sestavlja polarni del molekule in nepolarni večinoma dolgoverižni del. Celice prepoznavajo lipide z izjemno specifičnostjo. Funkcionalnost lipidov je določena z njihovo koncentracijo, ki niha med organeli kot tudi med celično lipidno dvoplastjo. S celično lipidomiko bi določali vrsto lipidov in njihovo koncentracijo v celici in medsebojne interakcije ter kakšna je časovna regulacija lipidne koncentracije in na katere druge molekule imajo lipidi vpliv. Proučevanje lipidov 2
21 T e o r e t i č n i d e l vključuje tudi encime lipidnega metabolizma in njihov transport, specifičnost, lokacijo in uravnavanje. Zahteva tudi razumevanje fizikalnih lastnosti lipidov in membran, še posebej»lipid-lipid«ter»lipid-protein«interakcije. Celična lipidomika je okvir za razumevanje ključne vloge lipidov, še posebej membranskega transporta. Najbolj preučevani bolezni, kot sta rak in Alzheimerjeva bolezen, imata vzrok v lipidnih spojinah (Mikirova, 2004), (Meng, 2004), (Pandey, 2003), (Bartsch, 1999), (Kuriki, 2011), (MacLean, 2006), (Punnonen, 1989), (Nourooz-Zadeh, 1999), (Söderberg, 1991). Klinična diagnostika si veliko obeta prav od analiz lipidnih profilov. Večina celičnih lipidov se organizira v membranah. Standardni membranski lipid je cilindrični fosfolipid (fosfatidilholin, PC), ki predstavlja 50 % celičnih lipidov. Nenasičen PC povzroča celično membransko dvoplastno fluidnost. Fosfatidilserin (PS) se pojavi na površini celice v primeru celične smrti in strjevanja krvi. Fosfatidilinozitol (PI) je osnova za fosfoinozitide, fosforilirane derivate, katerih signalna funkcija je odvisna od števila in položaja fosfatov na inozitolnem obroču. Sfingomielin (SM), podobno kot PC, vsebuje fosfoholinsko glavo, vendar ima hidrofobno ceramidno osnovo. Sfingolipidi tvorijo zbito, trdno membrano. Kadar so v bližini holesterola, ki je sterol sesalcev, postane membrana bolj fluidna. Na Sliki 1-2 vidimo strukturo membranskih lipidov. Slika 1 2: Struktura membranskih lipidov. Cilindrični glicerofosfolipid fosfatidilholin (PC) s fosfoholinsko»glavo«in dvema acilnima verigama (diacilglicerol), kjer je običajno ena nasičena in ena nenasičena (zvita) veriga. Fosfatidiletanolamin (PE) z manjšo polarno»glavo«, konične oblike, povzroča motnjo v dvoplasti. Fosfosfingolipid sfingomielin (SM) s svojo ravno obliko ustvarja urejenost in se rad nahaja v bližini ploščate obročaste strukture holesterola (HST). 3
22 T e o r e t i č n i d e l 1.3 Lipidi, nomenklatura in strukturna pestrost lipidov Splošna definicija lipidov je, da so to hidrofobne, majhne molekule, ki v celoti ali delno izvirajo iz dveh tipov bioloških podenot ali gradnikov; keto-acil in izoprenske osnove (Fahy, 2005, 2009). Zaradi svoje hidrofobne lastnosti v vodnem okolju tvorijo mehurčke, liposome in membrane. Strukturna raznolikost izvira iz biosintez mnogih kombinacij teh gradnikov. Na primer, glicerofosfolipidi so sestavljeni iz glicerolne osnove, vezane na enega od približno desetih možnih skupin in hkrati na dve maščobno acil/alkil verigi, ki imajo trideset ali več različnih struktur. Vseh kombinacij ni bilo mogoče eksperimentalno določiti. V celicah sesalcev je bilo določenih nekaj sto različnih glicerofosfolipidov. Še vedno ni povsem jasno, zakaj obstaja toliko različnih lipidov, saj jih je več kot tisoč. Nujno potrebnih je v naravi precej manj. Raziskuje se vzrok heterogene porazdelitve bioloških lipidov, kot tudi to, da so nekateri lipidi (družina omega-3)»dobri«in nekateri»slabi«(nasičene in omega-6 maščobne kisline ter holesterol). Pri ekstrakciji bioloških materialov z nepolarnimi topili dobimo množico spojin, kot so terpeni, steroidi, maščobe in olja in skupino drugih nepolarnih spojin, ki jih skupinsko imenujemo lipidi. Pri lipidih gre za veliko skupino naravno prisotnih molekul, kot so maščobe, voski, steroli, vitamini (vitamini A, D, E in K), monogliceridi, digliceridi, fosfolipidi in drugi. Najbolj splošna definicija lipidov je, da so to molekule, ki so netopne v vodi in topne v organskem topilu, kot so ogljikovodiki, kloroform, benzen, eter in alkohol. Takšna definicija je zavajajoča, saj je veliko lipidov topnih tako v vodi kot v organskih topilih. Najbolj razširjen sistem klasifikacije lipidov temelji na definiciji po Christie (Christie, 1982), ki razdeli lipide na enostavne lipide (spojine, kjer pri hidrolizi ne dobimo več kot dve vrsti primarnih produktov na mol), ki jih imenuje tudi nevtralni ali nepolarni lipidi, ter na polarne ali kompleksne lipide (spojine, kjer pri hidrolizi dobimo tri ali več primarnih produktov na mol). Kompleksni lipidi so npr. glicerofosfolipidi in glikosfingolipidi. Enostavni lipidi so steroli (holesterol in holesteril estri), proste maščobne kisline in acilgliceroli (triacilgliceroli). Na osnovi gradnikov lahko lipide delimo na osem kategorij (maščobni acili, glicerolipidi, glicerofosfolipidi, sfingolipidi, sterolni lipidi, prenolni lipidi, saharolipidi in poliketidi). Teh osem kategorij se nadalje deli na razrede in podrazrede. Seveda pa je vsaka shema delitve tudi subjektivna in temelji na strukturni in biosintezni kompleksnosti lipidov. Lipidna klasifikacijska shema kemijsko temelji na hidrofilnih oziroma hidrofobnih delih, ki sestavljajo lipide (Fahy, 2005). Klasifikacija je nujna za sistematično organiziranost lipidov. 4
23 T e o r e t i č n i d e l 1.4 Klasifikacija lipidov Predlagane kategorije v Preglednici 1-1 so poimenovane z okrajšavami tako, da so imena sprejeta v mednarodni literaturi (Fahy, 2005, 2009). Preglednica 1 1: Kategorije lipidov s primeri. Kategorija Okrajšava Primer Maščobni acili FA dodekanojska kislina Glicerolipidi GL 1-heksadekanoil 2-(9Z-oktadecenoil)-sn-glicerol Glicerofosfolipidi GP 1-heksadekanoil 2-(9Z-oktadecenoil)-sn-glicero-3-fosfoholin Sfingolipidi SP N-(tetradekanoil)-sfing-4-enin Sterolni lipidi ST Holest-5-en-3beta-ol Prenolni lipidi PR 2E, 6E-farnezol Saharolipidi SL UDP-3-O-(3R-hidroksi-tetradekanoil)-alfaD-Nacetilglukozamin Poliketidi PK aflatoksin B 1 (skupina metabolitov rastlinskega in mikrobnega izvora Maščobni acil (heksadekanojska kislina) Glicerolipid Glicerofosfolipid Sfingolipid Sterolni lipid Prenolni lipid Saharolipid Poliketid (aflatoksin B1) Slika 1 3: Značilni predstavniki posameznih lipidnih razredov. 5
24 T e o r e t i č n i d e l Maščobne acilne spojine Maščobne acilne spojine ali»maščobni acili«je splošen termin za opis maščobnih kislin, njihovih konjugatov in derivatov. Maščobna acilna struktura predstavlja napomembnejši gradnik kompleksnih lipidov in zato predstavlja osnovni gradnik bioloških lipidov. Veliko zaužitih lipidov se hidrolizira do prostih (nezaestrenih) maščobnih kislin (FFA), preden se absorbirajo in nadalje metabolizirajo. Maščobna kislina je najosnovnejši gradnik bioloških lipidov. Ogljikovo verigo večinoma sestavlja od 4 do 24 C atomov. Ponavljajoča metilenska skupina predstavlja hidrofobne lastnosti te kategorije lipidov. Možnih je ena ali več dvojnih ter trojnih vezi. Mogoča je tudi vezava heteroatomov kot so kisik, halogeni, dušik ali žveplo, pri čemer dobimo številne podrazrede. Ciklične maščobne kisline vsebujejo tri do šest ogljikovih atomov ali heterociklične obroče, ki vsebujejo kisik ali dušik. Tio maščobne kisline vsebujejo žveplove atome. Eikozanoide dobimo iz arahidonske (20:4n6) kisline (AA) in vključujejo prostaglandine, leukotriene in druge derivate. Dokozanoidi vsebujejo 22 ogljikovih atomov in nastanejo iz prekurzorja dokozaheksaenojske (22:6n3) kisline (DHA) Razredi in podrazredi maščobnih acilnih spojin (FA) Maščobne kisline in konjugati Ravnoverižne maščobne kisline Metil razvejane maščobne kisline Nenasičene maščobne kisline Metilensko prekinjene polinenasičene maščobne kisline Hidroperoksi maščobne kisline Hidroksi maščobne kisline Okso maščobne kisline Epoksi maščobne kisline Metoksi maščobne kisline Halogenirane maščobne kisline Amino maščobne kisline Ciano maščobne kisline Nitro maščobne kisline Tio maščobne kisline Karboksilne maščobne kisline Heterociklične maščobne kisline Dikarboksilne maščobne kisline Eikozanoidi Prostaglandini Leukotrieni Tromboksani Lipoksini Hidroksieikozatrienojske kisline Dokozanoidi Maščobni alkoholi Maščobni aldehidi Maščobni estri Voski monoestri Voski diestri Ciano estri Laktoni Maščobni acil-coas Maščobni acil-acil nosilec proteinov Maščobni acil karnitini Maščobni acil adenilati Maščobni amidi Primarni amidi N-Acil amidi Maščobni acil homoserinski laktoni N-Acil etanolamidi Maščobni nitrili Maščobni etri Ogljikovodiki Oksigenirani ogljikovodiki 6
25 T e o r e t i č n i d e l Hidroksieikozatetraenojske kisline Hidroksieikozapentaenojske kisline Epoksieikozatrienojske kisline Hepoksilini Levuglandini Izoprostani Klavuloni Drugi Ravnoverižna maščobna kislina Metil razvejana maščobna kislina Nenasičena maščobna kislina Hidroksi maščobna kislina Okso maščobna kislina Epoksi maščobna kislina Metoksi maščobna kislina Tio maščobna kislina Hidroperoksi maščobna kislina Karboksilna maščobna kislina Slika 1 4, a: Reprezentativne strukture maščobnih acilnih spojin. 7
26 T e o r e t i č n i d e l Heterociklična maščobna kislina Amino maščobna kislina Nitro maščobna kislina Halogenirana maščobna kislina Dikarboksilna kislina Prostaglandini Leukotrieni Maščobni alkoholi Maščobni aldehidi Maščobni amidi Maščobni nitrili Ogljikovodik Oksigeniran ogljikovodik. Vosek monoester Slika 1 4, b: Reprezentativne strukture maščobnih acilnih spojin. 8
27 T e o r e t i č n i d e l Vosek diester Lakton Slika 1 4, c: Reprezentativne strukture maščobnih acilnih spojin. Nekatere ravnoverižne nasičene maščobne kisline so zbrane v Preglednici 1 2. Njihova geometrijska konfiguracija in kot med C-C atomi (109 ºC) določata obliko kisline. Preglednica 1 2: Seznam nasičenih maščobnih kislin (SFA). Ime Trivialno Oznaka Ime Trivialno Oznaka ime ime etanojska ocetna 2:0 oktadekanojska stearinska 18:0 propanojska metilocetna 3:0 nonadekanojska 19:0 putanojska maslena 4:0 eikozanojska arašidinska 20:0 pentanojska valerianska 5:0 heneikozanojska 21:0 heksanojska kaprojska 6:0 dokozanojska behenska 22:0 heptanojska 7:0 trikozanojska 23:0 oktanojska kaprilska 8:0 tetrakozanojska lignocerinska 24:0 nonanojska 9:0 pentakozanojska 25:0 dekanojska kaprinska 10:0 heksakozanojska 26:0 undekanojska 11:0 heptakozanojska 27:0 dodekanojska lavrinska 12:0 oktakozanojska 28:0 tridekanojska 13:0 nonakozanojska 29:0 tetradekanojska miristinska 14:0 triakontanojska 30:0 pentadekanojska 15:0 hentriakontanojska 31:0 heksadekanojska palmitinska 16:0 dotriakontanojska 32:0 heptadekanojska margarinska 17:0 Nenasičene maščobne kisline (mononenasičene ravnoverižne maščobne kisline) imajo ponavadi dvojno vez v cis ali Z-konfiguraciji, čeprav so nekatere v naravnih lipidih prisotne tudi v trans- ali E-konfiguraciji (geometrijska izomerizacija, ki močno vpliva na konfiguracijo molekule). Cis dvojne vezi povzročajo upogibanje verige maščobnih kislin. Dobimo 30 º zasuk alkilne verige, kar zrahlja zloženost membran. Ta pojav ima pomembno vlogo pri strukturi in funkciji celične membrane. Najbolj pogoste monoenojske maščobne kisline so s 16 in 18 C atomi. 9
28 T e o r e t i č n i d e l Preglednica 1 3: Seznam mononenasičenih maščobnih kislin (MUFA). Ime Trivialno ime Oznaka Oznaka cis-9-tetradecenojska miristoleinska 14:1 (9c) 14:1n5 cis-7-heksadecenojska 16:1 (7c) 16:1n9 cis-9-heksadecenojska palmitoleinska 16:1 (9c) 16:1n7 cis-9-oktadecenojska oleinska 18:1 (9c) 18:1n9 cis-11-oktadecenojska cis-vakcenska 18:1 (11c) 18:1n7 cis-11-eikozenojska gondojska 20:1 (11c) 20:1n9 cis-13-dokozenojska eruka 22:1 (13c) 22:1n9 cis-15-tetrakozenojska nervonska 24:1 (15c) 24:1n9 trans-6-oktadecenojska 18:1 (6t) trans-9-oktadecenojska elaidinska 18:1 (9t) trans-11-oktadecenojska trans-vakcenska 18:1 (11t) Metilensko prekinjene polinenasičene maščobne kisline povzročajo v membranskem celičnem sistemu zrahljanje membranske zloženosti (dvojni vezi v cis-konfiguraciji ločeni z metilensko skupino (CH 2 ). Slika 1 5: Primer motenih dvojnih vezi z metilensko skupino. V naravi najdemo dve večji skupini polinenasičenih maščobnih kislin, ki izvirata iz linolne (18:2n6) kisline (LA) in iz α-linolenske (18:3n3) kisline (ALA). Prva je omega-6 (n6) polinenasičena maščobna kislina, druga je omega-3 (n3) polinenasičena maščobna kislina. Slika 1 6: Strukturni formuli linolne kisline (9-cis,12-cis-oktadekadienojske; 18:2n6) (LA) a) in α-linolenske lisline (9-cis,12-cis,15-cis-oktadekatrienojska; 18:3n3) (ALA) b). Biosintezo linolne in linolenske kisline vidimo na sliki 1 7. Slika 1 7: Prikaz biosinteze linolne (18:2n6) kisline (LA) in α-linolenske (18:3n3) kisline (ALA). Pretvorbe podaljšanja in nenasičenost verig linolne (18:2n6) kisline opravljajo enaki encimi kot v primeru biosinteze omega-3 kislin. Pri tem se linolna (18:2n6) kislina pretvori v arahidonsko (20:4n6) kislino (AA) (vmesni stopnji sta γ-linolenska (18:3n6) kislina (GLA) in dihomo γ-linolenska (20:3n6) kislina (DGLA)). V možganovini 10
29 T e o r e t i č n i d e l prevladuje dokozaheksaenojska (22:6n3) kislina (DHA), v vseh ostalih celicah pa arahidonska (20:4n6) kislina (AA). Biosintezo omega-6 polinenasičenih maščobnih kislin (n6-pufa) vidimo na sliki 1 8. Slika 1 8: Biosinteza omega-6 polinenasičenih maščobnih kislin. Biosintezo omega-3 polinenasičenih maščobnih kislin (n3-pufa) vidimo na sliki 1 9. Slika 1 9: Biosinteza omega-3 polinenasičenih maščobnih kislin. 11
30 T e o r e t i č n i d e l ALA (α-linolenska (18:3n3) kislina) je prekurzor eikozapentaenojske (20:5n3) kisline (EPA) in dokozaheksaenojske (22:6n3) kisline (DHA) (Slika 1 9). Podaljšanje verige poteka encimatsko. Encimi se imenujejo elongaze, procesu podaljšanja rečemo tudi elongacija. Nenasičenost povečujejo encimi desaturaze. Proces imenujemo desaturacija. Ti encimi so jetrni encimi. Preglednica 1 4: Seznam polinenasičenih (PUFA) maščobnih kislin. Ime Trivialno ime Oznaka Oznaka linolna (LA) 18:2 (9c,12c) 18:2n6 γ-linolenska (GLA) 18:3 (6c,9c,12c) 18:3n6 eikozadienojska 20:2 (11c,14c) 20:2n6 dihomo γ-linolenska (DGLA) 20:3 (8c,11c,14c) 20:3n6 arahidonska (AA) 20:4 (5c,8c,11c,14c) 20:4n6 adrenska 22:4 (7c,10c,13c,16c) 22:4n6 dokozapentaenojska 22:5 (4c,7c,10c,13c,16c) 22:5n6 α-linolenska (ALA) 18:3 (9c,12c,15c) 18:3n3 stearidonska 18:4 (6c,9c,12c,15c) 18:4n3 eikozapentaenojska (EPA) 20:5 (5c,8c,11c,14c,17c) 20:5n3 dokozapentaenojska (DPA) 22:5 (7c,10c,13c,16c,19c) 22:5n3 dokozaheksaenojska (DHA) 22:6 (4c,7c,10c,13c,16c,19c) 22:6n3 Strukturne formule pomembnejših polinenasičenih maščobnih kislin so na Slikah 1 10 do Slika 1 10: Strukturna formula LA (linolna kislina; 18:2n6). Slika 1 11: Strukturna formula AA (arahidonska kislina; 20:4n6). 12
31 T e o r e t i č n i d e l Slika 1 12: Strukturna formula ALA (α-linolenska kislina; 18:3n3). Slika 1 13: Strukturna formula DHA (dokozaheksaenojska kislina; 22:6n3). Med polinenasičenimi (PUFA) maščobnimi kislinami je glede na prehranske študije najbolj»pozitivna«dokozaheksaenojska (22:6n3) kislina (DHA) (rakave bolezni (Carroll, 1991), (Zerouga, 1996), srčna obolenja (McLennan, 1996), revmatoidni artritis (Kremer, 1990), astma (Yokoyama, 2000), lupus (Das, 1994), alkoholizem (Pawlosky, 1995), respiratorne bolezni (Knapp, 1995), dermatitis (Tomobe, 2000), psoriaza (Grimminger, 1993), shizofrenija (Laugharne, 1996), depresija (Hibbeln, 1995). 13
32 T e o r e t i č n i d e l Arahidonska kislina in vnetni biološki procesi Biološko zelo pomembne maščobne kisline so skupina eikozanoidov, ki vključujejo prostaglandine, leukotriene in tromboksane in izvirajo iz arahidonske (20:4n6) kisline (AA) ter eikozapentaenojske (20:5n3) kisline (EPA). Največjo vlogo pri vnetnih procesih in v centralno živčnem sistemu ima arahidonska (20:4n6) kislina (AA-kaskada). Vzporedno potekata dve tekmovalni kaskadi maščobnih kislin. Prva je EPA-kaskada (eikozapentaenojska (20:5n3) kislina), druga, manj pomembna, pa je DGLA-kaskada (dihomo γ-linolenska (20:3n6) kislina) (Slika 1-14). Obe kaskadi zmanjšujeta vnetne vplive arahidonske (20:4n6) kisline (AA). Slika 1-14 prikazuje n-3 in n-6 sintezni verigi, skupaj z glavnimi eikozanoidi, ki nastanejo iz EPA, DGLA in AA. Slika 1 14: Metabolizem esencialnih maščobnih kislin in nastanek eikozanoidov. 14
33 T e o r e t i č n i d e l Zmanjšan prehranski vnos»manj vnetnih«maščobnih kislin (še posebej omega-3) povezujemo z naraščanjem vnetnih bolezni (bolezni civilizacije). Eikozanoidi, ki nastanejo iz arahidonske (20:4n6) kisline (AA), v splošnem povzročajo vnetne procese. Tisti, ki nastanejo iz γ-linolenske (18:3n6) kisline (GLA) preko dihomoγ-linolenske (20:3n6) kisline (DGLA), delujejo manj vnetno ali celo protivnetno. S prehrano vnesena linolna (18:2n6) kislina (LA) se v procesu metabolizma podaljša do arahidonske (20:4n6) kisline (AA), ki je tudi bolj nenasičena kislina in se vgradi v fosfolipide membran. Kot odziv na vnetne povzročitelje fosfolipaza razcepi fosfolipid, kjer se sprosti arahidonska (20:4n6) kislina (AA) kot prosta maščobna kislina. Pri procesih oksigenacije nastanejo eikozanoidi (metaboliti arahidonske kisline), ki pospešujejo vnetne procese. Preglednica 1 5: Tri esencialne kisline C20 in eikozanoidi, ki iz njih nastajajo. Prehrambene esencialne maščobne Okrajšava Formula Eikozanoidi: vpliv kisline arahidonska kislina AA 20:4n6 poveča vnetne procese γ-linolenska kislina via GLA via DGLA 18:3n6 zmanjša vnetne procese dihomo γ-linolenska kislina 20:3n6 eikozapentaenojska EPA 20:5n3 zmanjša vnetne procese Za fiziologijo prostaglandinov je bila leta 1982 podeljena Nobelova nagrada za medicino. Aspirin in njemu podobna zdravila zavirajo sintezo prostaglandinov. Naslednja pomembnejša kategorija lipidov so maščobni estri - voski Voski Nastopajo v svoji najbolj običajni obliki kot estri (WE), kjer je maščobna kislina zaestrena na dolgoverižni alkohol približno enake dolžine (Slika 1-15). Slika 1 15: Strukturna formula estra voska Glicerolipidi Glicerolipide sestavljajo mono-, di- in tri- substituirani gliceroli, ki so bolj znani kot estri glicerola in maščobnih kislin (triacilgliceroli ali trigliceridi). Pri tem so tri hidroksilne skupine ponavadi zaestrene z različnimi maščobnimi kislinami. Imajo vlogo energijskih zalog. Hidrolizo esterskih vezi triacilglicerola in sprostitev glicerola ter maščobnih kislin iz zalog imenujemo maščobna mobilizacija. Dodatni podrazred glicerolipidov so glikozilgliceroli (glicerolglikozidi), kjer je eden ali več sladkorjev z glikozidno vezjo vezanih na glicerol (glicerolglukani). 15
34 T e o r e t i č n i d e l Glicerolipidni razredi in podrazredi Monoradilgliceroli* monoacilgliceroli monoalkilgliceroli mono-(1z-alkenil)-gliceroli monoacilglicerolglikozidi monoalkilglicerolglikozidi Diradilgliceroli diacilgliceroli alkilacilgliceroli dialkilgliceroli 1Z-Alkenilacilgliceroli diacilglicerolglikozidi alkilacilglicerolglikozidi dialkilglicerolglikozidi di-glicerol-tetraetri di-glicerol tetraeter glikani Triradilgliceroli triacilgliceroli alkildiacilgliceroli dialkilmonoacilgliceroli 1Z-alkenildiacilgliceroli estolidi Drugi *»radil«vključuje acilglicerole kot tudi alkil in 1-elkenil variante. monoradilglicerol: monoacilglicerol diradilglicerol: diacilglicerol diradilglicerol: alkilacilglicerol diradilglicerol: 1Z-alkenilacilglicerol Slika 1 16, a: Reprezentativne strukture glicerolipidov. 16
35 T e o r e t i č n i d e l triradilglicerol: triacilglicerol diradilglicerol: diacilglicerolglikozid diradilglicerol: di-glicerol tetraeter diradilglicerol: di-glicerol tetraeter glikan Slika 1 16, b: Reprezentativne strukture glicerolipidov Monoacilgliceroli (MAG) Monoacilgliceroli (2-monoacil-sn-gliceroli) nastanejo kot končni produkt encimske hidrolize triacilglicerolov. 1-/3- izomeri nastanejo sintetično. Označujemo jih kot α- monoacilgliceroli in jih med seboj ne ločimo. 2- izomeri so β-monoacilgliceroli. Stereokemijo opišemo s stereospecifičnim številčenjem (»sn«sistem) (Sika 1-17). Slika 1 17: Stereokemične oblike monoacilglicerolov Diacilgliceroli (DAG) Diacilglicerole pogosto poimenujejo»delni gliceridi«. 1,2-diacil-sn-gliceroli so prekurzorji biosinteze triacilglicerolov in drugih lipidov. Obstajajo lahko v treh stereokemičnih oblikah (Slika 1-18). Mešanico sn-1,2- in sn-2,3- diacilglicerolov lahko zapišemo tudi kot α,β-diacilgliceroli, medtem ko sn-1,3-diacilglicerole označimo tudi kot α,α'-diacilgliceroli. 17
36 T e o r e t i č n i d e l Slika 1 18: Stereokemične oblike diacilglicerolov Triacilgliceroli (TAG) V naravi se encimsko sintetizirajo. Center asimetrije je okoli C-2 atoma glicerolne osnove, kjer so vse tri hidroksilne skupine zaestrene z dolgoverižnimi maščobnimi kislinami. Zaradi svojih površinsko aktivnih lastnosti ne pričakujemo, da bi se akumulirali, saj bi imeli uničujoč vpliv na membrane. Slika 1 19: Fisherjeva projekcija triacil-sn-glicerola Glicerofosfolipidi Glicerofosfolipide imenujemo tudi fosfolipidi in so ključni sestavni del lipidne dvoplasti celičnih membran. Vključeni so v celični metabolizem in funkcijo signalizacije. Živčna tkiva vsebujejo velik delež glicerofosfolipidov. Posledice sprememb njihove sestave se kažejo kot številne motnje v delovanju živčevja (Strassnig, 2005), (Bell, 2000), (Greene, 2006), (Assies, 2001), (Amminger, 2010), (Peet, 1998), (Yao, 2000), (Peet, 2004). Najpomembnejši glicerofosfolipidi, ki jih najdemo v bioloških membranah, so fosfatidilholin (PC), fosfatidiletanolamin (PE) in fosfatidilserin (PS). Nomenklatura fosfolipidov temelji na poimenovanju polarnega dela molekule (holin, etanolamin, inozitol, glicerol, serin ). Fosfatidinska kislina (1,2-diacil-sn-glicerol-3-fosfat) je biosintezni prekurzor za vse glicerolipide. Ponavadi jo izoliramo v obliki soli (Slika 1-20). Slika 1 20: Strukturna formula soli fosfatidinske kisline. 18
37 T e o r e t i č n i d e l Običajen zapis molekul fosfolipida je v obliki x:y, kjer je x število ogljikovih atomov, y pa število dvojnih vezi. Obstaja več kot tisoč možnih struktur fosfolipidov. Za določevanje molekularnih gradnikov celic je potrebno uporabiti tehniko, s katero je mogoče razlikovati med polarnim delom molekule, dvojnimi vezmi, dolžino maščobnih kislin in tipom vezi na sn-1 in sn-2 položaju maščobne kisline Razredi glicerofosfolipidov Glicerofosfoholini (PC) Glicerofosfoetanolamini (PE) Glicerofosfoserini (PS) Glicerofosfogliceroli (PG) Glicerofosfoglicerofosfati Glicerofosfoinozitoli (PI) Glicerofosfoinozitol monofosfati Glicerofosfoinozitol bifosfati Glicerofosfoinozitol trifosfati Glicerofosfati Gliceropirofosfati Glicerofosfoglicerofosfogliceroli CDP-gliceroli Glicerofosfoglukozo lipidi Glicerofosfoinozitol glukani Glicerofosfonoholini Glicerofosfonoetanolamini Di-glicerol tetraeter fosfolipidi Oksidirani glicerofosfolipidi Drugi Glicerofosfoholini Glicerofosfoetanolamini Glicerofosfoserini Glicerofosfogliceroli Glicerofosfoglicerofosfati Glicerofosfoinozitoli Slika 1 21, a: Reprezentativne strukture glicerofosfolipidov. 19
38 T e o r e t i č n i d e l Glicerofosfoinozitol monofosfati Glicerofosfati Gliceropirofosfati Glicerofosfoglicerofosfogliceroli CDP-gliceroli Glicerofosfoinozitolglukani Glicerofosfonoholini Glicerofosfonoetanolamini Di-glicerol tetraeter fosfolipidi Slika 1 21, b: Reprezentativne strukture glicerofosfolipidov. 20
39 T e o r e t i č n i d e l Fosfatidilholin (PC) (trivialno ime lecitin) ali 1,2-diacil-sn-glicerol-3-fosforilholin je v membranah eden najbolj prisotnih fosfolipidov. Predstavlja skoraj 50 % vseh fosfolipidov in je ključni gradnik zunanje dvoplasti membrane. Je nevtralen fosfolipid tako v kislem kot alkalnem mediju. Pri živalih je v diacil obliki in le v majhnem deležu v alkilacil ali alkenilacil obliki. Živalski fosfatidilholin vsebuje manj arahidonske (20:4n6) kisline (AA) in dokozaheksaenojske (22:6n3) kisline (DHA) ter več C-18 nenasičenih maščobnih kislin. Nasičene maščobne kisline so bolj značilne na sn-1 položaju, medtem ko so nenasičene na sn-2. C-20 in C-22 polienojske kisline so izključno na sn-2 položaju. Slika 1 22: Fosfatidilholin. Fosfatidiletanolamin (PE) (trivialno ime kefalin) je običajno drugi najbolj prisoten fosfolipid. Amino skupina se lahko encimsko metilira do končnega produkta fosfatidilholina. Slika 1 23: Fosfatidiletanolamin. Fosfatidilserin (PS) je šibko kisel (anionski) fosfolipid (fosfatna skupina, amino in karboksilna skupina). V naravi obstaja v obliki soli. Najdemo ga tudi v mikroorganizmih. Nahaja se izključno na notranji dvoplasti celične membrane. Sodeluje pri bioloških procesih, kot je koagulacija krvi. Slika 1 24: Fosfatidilserin. 21
40 T e o r e t i č n i d e l Fosfatidilinozitol (PI) Je kisel (anionski) fosfolipid. Inozitol je heksahidroksicikloheksan. V živalskih tkivih sta najbolj prisotni stearinska (18:0) kislina (na sn-1 položaju) in arahidonska (20:4n6) kislina (AA) (na sn-2 položaju). Slika 1 25: Fosfatidilinozitol Plazmalogeni - eterski lipidi Naslednja delitev fosfolipidov je glede na tip vezi med glicerolom in maščobno kislino na sn-1 položaju. Povezava je lahko esterska, vinil eterska ali alkil eterska, kjer dobimo fosfatidil, plazmenil ali plazmanil podrazrede. V naravnih lipidih obstajata dva tipa eterske vezi (kot eter ali vinil eter). Slika 1 26: Plazmaniletanolamin (eter). Slika 1 27: Plazmeniletanolamin (vinil eter). Lipide, ki vsebujejo vinil etersko vez na sn-1 položaju glicerolne osnove, imenujemo plazmalogeni. To je fosfolipidni podrazred in jih v višjih koncentracijah najdemo v eritrocitih kot sestavni del celičnih membran. Najbolj pogosti so fosfatidiletanolamin (PE) plazmalogeni in fosfatidilholin (PC) plazmalogeni. Vsebnost prvih je približno 10- krat večja od slednjih. Celično membranski plazmalogeni sestavljajo od 15 % do 20 % vseh membranskih fosfolipidov (Nagan, 2001). Alifatski del na sn-1 položaju je večinoma nasičena ali delno nenasičena (vedno cis izomera) maščobna kislina. Plazmalogenski fosfolipidi imajo na sn-2 položaju najpogosteje zaestrene polinenasičene maščobne kisline z najmanj štirimi dvojnimi vezmi (dokozaheksaenojska (22:6n3) kislina (DHA) ali arahidonska (20:4n6) kislina (AA)) in predstavljajo večjo zalogo polinenasičenih maščobnih kislin v celičnih membranah (Lesig, 2009). V zadnjem desetletju študije nakazujejo, da so membranski plazmalogeni eden pomembnejših lipidno topnih antioksidantov. Doslej je veljal α-tokoferol (E vitamin) za 22
41 T e o r e t i č n i d e l najpomembnejši lipidno topni antioksidativni varovalni sistem. Ostali znani hidrofobni antioksidanti, kot sta β-karoten in ubikinon (koencim Q10), so prisotni v znatno nižjih koncentracijah in pogosto reagirata z omejenim izborom oksidantov (radikali, UV svetloba, ioni kovinskih prehodnih elementov). Vsakič, ko membransko polinenasičeno maščobno kislino ogroža oksidant, nastopi notranje molekularno tekmovanje med reakcijo oksidacije enol eter dvojne vezi ali dvojne vezi v polinenasičeni maščobni kislini na sn-2 položaju. Tako prihaja do oksidativne razgradnje plazmalogenov, pri čemer ostajajo polinenasičene maščobne kisline neprizadete. Bolezenska stanja, ki jih spremlja povečana lipidna oksidacija, lahko znatno zmanjšajo vsebnost plazmalogenov. Čeprav se plazmalogeni lahko regenerirajo, še ni znano, kako obnova poteka (Engelmann, 2004). Iz plazmalogenskih fosfolipidov membran rdečih krvnih celic nastane pri esterifikaciji z metanolno raztopino borovega trifluorida mešanica dimetil acetalov (predvsem 16:0 DMA in 18:0 DMA zaradi 16 in 18 alkilnih verig na sn-1 položaju glicerolne osnove). Pri hidrolizi se vinilna dvojna vez odpre in nastanejo prosti dolgoverižni aldehidi, ki se pri metiliranju pretvorijo v dimetil acetale, katere lahko analiziramo s plinsko kromatografijo. Slika 1 28: Hidroliza plazmalogena in nastanek aldehida. Slika 1 29: Dimetil acetal. 23
42 T e o r e t i č n i d e l Sfingolipidi Sfingolipidi ne vsebujejo glicerolne osnove in so derivati sfingozina (Slika 1-29). Slika 1 30: Sfingozin. Sestavljeni so iz dolgoverižne osnove, povezane z amidno vezjo na maščobno kislino in s terminalno hidroksilno skupino. Alifatska veriga je lahko nasičena ali nenasičena (cis ali trans konfiguracije). Maščobne kisline so ponavadi nenasičene ali mononenasičene z dolžino verige od 16 do 26 C-atomi. Najpomembnejši fosfosfingolipidi pri sesalcih so sfingomielini (ceramid fosfoholini) (Slika 1-30). Glikosfingolipidi so velika skupina molekul, kjer je eden ali več sladkorjev preko glikozidne vezi vezanih na sfingoidno osnovo. Slika 1 31: Sfingomielin Razredi sfingolipidov a1, a2, a3, a4) sfingoidne osnove (sfinganini, sfingozini) b1, b2) ceramidi c) fosfosfingolipidi (sfingomielini) d) fosfonosfingolipidi e) nevtralni glikosfingolipidi f1, f2, f3) kisli glikosfingolipidi (gangliozidi, sulfosfingolipidi, glukuronosfingolipidi) Alkalni glikosfingolipidi Drugi 24
43 T e o r e t i č n i d e l a1) sfinganin a2) sfingozin a3) N-metilirana sfingoidna osnova a4) fosfat sfingoidne osnove b1) ceramid b2) acilceramid c) sfingomielin d) fosfonosfingolipid e) nevtralni glikosfingolipidi f1) gangliozid f2) sulfosfingolipid f3) glukuronsfingolipid Slika 1 32: Reprezentativne strukture sfingolipidov. 25
44 T e o r e t i č n i d e l Sterolni lipidi Sterolne lipide delimo glede na njihove biološke funkcije. Pri sesalcih je najbolj preučevana spojina holesterol (HST), ki je pomemben sestavni del membranskih lipidov skupaj z glicerofosfolipidi in sfingomielini (Bach, 2003). Holesterol je najbolj znan predstavnik steroidov. Ima tetraciklični obročni sistem z dvojno vezjo in eno prosto hidroksilno skupino ter pomembno vlogo pri zagotavljanju fluidnosti membrane. V zaestreni obliki dobimo holesteril estre. Holesterol je prekurzor žolčnih kislin in steroidnih hormonov. V rastlinah njegovo vlogo prevzamejo fitosteroli (sitosterol, stigmasterol, avenasterol, kampesterol in brasikasterol ter njihovi estri maščobnih kislin). Steroidi nastopajo v vlogi hormonov. Delimo jih glede na število C-atomov skeleta. C 18 steroidi so estrogeni, medtem ko so C 19 androgeni (testosteron in androsteron). C 21 podrazred ima dodano verigo iz dveh C-atomov na C 17 položaju. Dobimo progesterone, (glukokortikoidi in mineralokortikoidi) Razredi in podrazredi sterolnih lipidov Steroli Holesterol in derivati Holesteril estri Fitosteroli in derivati Steroidi C 18 steroidi (estrogeni) in derivati C 19 steroidi (androgeni) in derivati C 21 steroidi (gluko/mineralokortikoidi, progestogini) in derivati Sekosteroidi Vitamin D 2 in derivati Vitamin D 3 in derivati Žolčne kisline in derivati C 24 žolčne kisline, alkoholi in derivati C 26 žolčne kisline, alkoholi in derivati C 27 žolčne kisline, alkoholi in derivati C 28 žolčne kisline, alkoholi in derivati Steroidni konjugati Glukuronidi Sulfati Glicin konjugati Taurin konjugati Hopanoidi Drugi 26
45 T e o r e t i č n i d e l Holesterol Holesteril estri C 18 steroidi (estrogeni) in derivati C 19 steroidi (androgeni) in derivati C 21 steroidi (gluko/mineralokortikoidi, progestogini) in derivati Sekosteroidi: vitamin D 2 in derivati Sekosteroidi: vitamin D 3 in derivati C 24 žolčne kisline, alkoholi in derivati C 26 žolčne kisline, alkoholi in derivati C 27 žolčne kisline, alkoholi in derivati Slika 1 33, a: Reprezentativne strukture sterolnih lipidov. 27
46 T e o r e t i č n i d e l Steroidni konjugati: Glukuronidi Steroidni konjugati: Taurin konjugati Steroidni konjugati: Glicin konjugati Steroidni konjugati: Sulfati Hopanoidi: diplopten Slika 1 33, b: Reprezentativne strukture sterolnih lipidov. 28
47 T e o r e t i č n i d e l Prenolni lipidi Prenoli se sintetizirajo iz prekurzorjev s petimi C-atomi izopentenil difostata. Enostavni izoprenoidi (linearni alkoholi, difosfati ) nastanejo z zaporednim dodajanjem C 5 enot. Zato jih tako tudi klasificiramo Razredi in podrazredi prenolnih lipidov Izoprenoidi C 5 izoprenoidi C 10 izoprenoidi (monoterpeni) C 15 izoprenoidi (seskviterpeni) C 20 izoprenoidi (diterpeni) C 25 izoprenoidi (sesterterpeni) C 30 izoprenoidi (triterpeni) C 40 izoprenoidi (tetraterpeni) Politerpeni Kinoni in hidrokinoni Ubikinoni Vitamin E Vitamin K Poliprenoli Baktoprenoli Baktoprenol monofosfati, difosfati Fitoprenoli Fitopreno monofosfati, difosfati Doliholi Dolihol monofosfati, difosfati Drugi C 5 izoprenoid: dimetilalil fosfat C 10 izoprenoid C 15 izoprenoid C 20 izoprenoid: retinol; vitamin A C 25 izoprenoid C 30 izoprenoid Slika 1 34, a: Reprezentativne strukture prenolnih lipidov. 29
48 T e o r e t i č n i d e l C 40 izoprenoid: β-karoten Ubikinoni: ubikinon-10 (Co-Q10) Vitamin K Vitamin E: α-tokoferol Doliholi Baktoprenol difosfati: lipidni prekurzor peptidoglikana v bakteriji E coli. Slika 1 34, b: Reprezentativne strukture prenolnih lipidov. 30
49 T e o r e t i č n i d e l 1.5 Celična membrana in strukturna organiziranost rdeče krvne celice Polovico membranske mase predstavljajo proteini, polovico pa lipidi (predvsem fosfolipidi in holesterol). Glicerofosfolipidi so glavna sestavina bioloških membran. Oblika lipidne dvoplasti je za glicerofosfolipide v vodnem mediju energijsko najugodnejša oblika. Obe plasti sta v stiku, nista pa kemijsko povezani in lahko prosto drsita ena ob drugi. Rdeče krvne celice ali eritrociti so brezjedrne krvne celice in so posebnost med človeškimi celicami, kjer membrana vpliva na njihove transportne in mehanične lastnosti. Membrane prevzemajo številne vloge, kot je pomoč pri regulaciji površinske deformacije, prožnosti, povezave z ostalimi celicami in imunske prepoznavnosti. Vse to je odvisno od njihove zgradbe, ki definira lastnosti. So v obliki bikonkavnih diskov z življenjsko dobo od 100 do 120 dni. Pri ponavljajočih prehodih snovi skozi ozke kapilare s premerom ene tretjine premera eritrocita so se sposobne močno deformirati. V svojem štirimesečnem bivanju v krvnem obtoku ji strukturna organiziranost omogoča izjemno reverzibilno prožnost. Je zelo elastična (približno 100-krat bolj od lateksa enake debeline), se hitro odziva na spremembe prekrvavitve (»fluid stress«) in je glede na pojem strukturne odpornosti močnejša od jekla. Slika 1 35: Shematski prikaz zgradbe celice in celične membrane. 31
50 T e o r e t i č n i d e l Medtem ko je celica sposobna deformacije v smeri raztezka tudi do 250 %, že 3 % do 4 % povečanje njene površine povzroči njen razpad. Raztezne deformacije ne povzročajo bistvenih sprememb v površini membran, ker je vpeta v dvodimenzionalni elastični mrežni proteinski skelet. Rdeče krvne celice imajo dejansko tri membranske plasti. Na zunanji strani je glikokaliks, ki je bogat z ogljikovodiki, sledi lipidna dvoplast, ki razen glavnih lipidnih komponent vsebuje še številne proteine. Tretjo plast naj bi predstavljal membranski skelet, ki je pripet na fosfolipidno dvoplast. Trenutno razumevanje strukture in organiziranosti normalne rdeče krvne celice je opisano v literaturi (Mohandas, 2008). Slika 1 36: Posnetek rdeče krvne celice (a), trombocita (b) in leukocita (c) z elektronskim mikroskopom. Premer diska rdeče krvne celice je od 6 do 8 μm in debeline 2 μm. Odrasel človek jih vsebuje približno od 2 do (ženske povprečno od 4 do 5 milijonov eritrocitov na μl, moški od 5 do 6 milijonov na μl). Skoraj tretjino celice zasede hemoglobin, metaloprotein, ki je zadolžen za prenos več kot 98 % kisika. Preostali kisik je raztopljen v krvni plazmi. Sposobnost rdečih krvnih celic, da nadzira koncentracijo hemoglobina znotraj ozkih mej, je odvisna od njihove sposobnosti kontrolirati prostornino. Povprečno je v rdečih krvnih celicah odraslega moškega 2,5 g železa, kar predstavlja približno 65 % vsega železa v telesu. Membranski lipidi so sestavljeni v enakem masnem razmerju holesterola in fosfolipidov. Medtem ko je holesterol enakomerno porazdeljen med obema plastema, so najpomembnejši fosfolipidi neenakomerno porazdeljeni. Na zunanji membranski strani sta fosfatidilholin (PC) in sfingomielin (SM), na notranji strani pa fosfatidiletanolamin (PE), fosfatidilserin (PS) in fosfatidilinozitol (PI) (Zwaal, 1997). Asimetrična porazdelitev fosfolipidov je rezultat delovanja fosfolipidnih transportnih proteinov, ki so energijsko odvisni ali neodvisni. Ti proteini se imenujejo flipaze, ki premikajo fosfolipide iz zunanje plasti na notranjo, in flopaze, ki počno obratno. Čeprav naj bi ti transportni proteini kontrolirali transportno aktivnost v rdeči krvni celici, si o njihovi identiteti znanstveniki še niso enotni. 32
51 T e o r e t i č n i d e l Slika 1 37: Prikaz asimetrične porazdelitve lipidov na zunanji in notranji strani membrane rdeče krvne celice. Na fizikalne lastnosti membran vplivajo vgradnje predvsem polinenasičenih maščobnih kislin. Primer je dokozaheksaenojska (22:6n3) kislina (DHA), ki se rada vgradi v membranske fosfolipide in vpliva na številne osnovne lastnosti in funkcije membrane, vključujoč interakcije z drugimi membranskimi lipidi (holesterol), vpliva na vrstni red kislinskih verig in s tem prehodnost in fluidnost membrane, elastično stisljivost ter»flipflop«in proteinsko aktivnost (Stillwell, 2003). 33
52 D o l o č a n j e l i p i d o v 2 DOLOČANJE LIPIDOV Izolacija fosfolipidov iz celokupnega lipidnega ekstrakta je postala zanimivo raziskovalno področje, ker so fosfolipidi skupaj s proteini pomemben sestavni del bioloških membran. Analizni postopek sestavljajo štirje sklopi: Ekstrakcija lipidov Izolacija fosfolipidov Hidroliza fosfolipidov in derivatizacija maščobnih kislin GC analiza in identifikacija metilnih estrov maščobnih kislin 2.1 Ekstrakcija lipidov iz bioloških materialov Večina ekstrakcijskih metod lipidov in njihove izolacije iz bioloških materialov temelji na njihovi topnosti v organskih topilih. Zaradi lipidne raznolikosti vseh razredov ni mogoče izolirati z eno samo metodo. Obstaja široka izbira ekstrakcijskih metod, ker so biološki materiali različni glede na strukturo in vsebnost lipidov. Običajni postopki, kot sta metodi po Folchu (Folch, 1957) in Blight in Dyerju (Bligh, 1959), uporabljajo mešanico kloroforma in metanola ter lipidno porazdelitev v organsko fazo. Izbira ekstrakcijskega topila je pri tem večjega pomena Ekstrakcijska topila Pri ekstrakciji lipidov iz bioloških materialov sta pomembna ekstrakcija in topnost lipidov v organski fazi ter odstranitev motečih nelipidnih spojin iz ekstrakta (proteinov, polisaharidov, amino kislin ). Za ekstrakcijo posameznega lipidnega razreda je mogoče uporabiti kombinacije različnih topil ali njihove mešanice. Ekstrakcija lipidov je odvisna tudi od njihove koncentracije v matrici. Kadar so prisotni enostavni nepolarni lipidi v presežku, se poveča sočasna ekstrakcija polarnih lipidov, ki so sicer težko topni v nepolarnih topilih. Ekstrakcijske lastnosti in ekstrakcijsko sposobnost topila je za matrico, iz katere želimo ekstrahirati lipide, težko vnaprej napovedati. Za ekstrakcijo vseh lipidov, ki so vezani v celičnih membranah ali lipoproteinih, mora biti ekstrakcijsko topilo delno polarno, a ne tako, da pride do reakcij z lipidi, ali da se triacilgliceroli in drugi nepolarni lipidi ne bi raztopili. Ekstrakcijsko topilo mora preprečiti encimsko hidrolizo ter ne sme povzročati dodatnih reakcij. Topnost lipidov v organskih topilih določata njihova strukturna dela. To sta hidrofobni ogljikovodikov del in katerakoli polarna skupina. Vsi lipidi brez polarnega dela, kot so triacilgliceroli ali holesteril estri, so zelo dobro topni v ogljikovodikih, kot so heksan, toluen ali cikloheksan ter v srednje polarnih topilih, kot sta dietileter ali kloroform. Ti lipidi so precej netopni v polarnih topilih, kot je metanol. Njihova topnost se veča z dolžino ogljikovodikove verige alkohola. Polarni lipidi so topni v metanolu, etanolu ali kloroformu. Večina kompleksnih lipidov je delno topnih v vodi ali tvori raztopino micel. Gangliozidi, polifosfoinozitidi, lizofosfolipidi acil-karnitini in koencim A estri so še posebej dobro topni v vodi. Enostavni lipidi se v telesu običajno nahajajo v maščobnem 34
53 D o l o č a n j e l i p i d o v tkivu, medtem ko se kompleksni nahajajo v skupkih s proteini in polisaharidi, s katerimi interagirajo (Van der Waalsove vezi, vodikove in ionske vezi) in se s težavo ekstrahirajo. Za uspešno ekstrakcijo lipidov iz biološkega materiala potrebujemo topilo, ki ne le da lipide raztaplja, ampak mora premagati interakcije med lipidom in matrico materiala, kjer gre za hkratne hidrofobne in polarne interakcije. V praksi nobeno čisto organsko topilo tem zahtevam ne ustreza. Večinoma se za ekstrakcijo lipidov iz živalskih, rastlinskih in bakterijskih materialov uporablja mešanica kloroforma in metanola v razmerju 2:1 (ponavadi je voda iz matrice tretja komponenta ekstrakcijskega sistema). Leta 1957 je izšla publikacija (Folch, 1957), v kateri je opisana metoda ekstrakcije postala primerjalna metoda za vse ekstrakcjske metode, ki so sledile. Ključna lastnost uspešnosti te mešanice topil je po oceni Schmida (Schmid, 1973) vzpostavljenost šibke vodikove vezi med kloroformom in vodo. Izbira ekstrakcijskih topil je bila namenjena izolaciji celičnih membransko vezanih fosfolipidov. Pri ekstrakciji polarnih lipidov s polarnim topilom pa vedno obstaja verjetnost koekstrakcije naravnih nelipidnih spojin. Veliko teh spojin lahko odstranimo iz mešanice kloroform-metanol (2:1, v/v) že s stresanjem s četrtino volumna vode ali še bolje z vodno raztopino soli (npr. 0.9 % raztopina natrijevega klorida), kot je opisano v literaturi (Folch, 1957). Topilo se porazdeli v dve plasti. Spodnja kloroform-metanolvoda je v razmerju (86:14:1, v/v/v), zgornja pa v razmerju (3:48:47, v/v/v). Lipidi se nahajajo v spodnji fazi, ki predstavlja skoraj 60 % celokupnega volumna, medtem ko zgornja faza vsebuje nelipidne moteče spojine. V nalogi nisem imela namena ohraniti proteinov pri ekstrakciji celokupnih lipidov iz eritrocitov, zato sem jih lahko v postopku ekstrakcije denaturirala in tako odstranila. Če bi želela proteine ohraniti, bi lahko pri ekstrakciji uporabila detergent TritonX-114 (Ferraz, 2004). Po Folchovi metodi biološko matrico homogeniziramo v prisotnosti mešanice obeh topil, ki povzroči trenutno denaturacijo proteinov ob hkratni ekstrakciji lipidov s kloroformom. Ekstrakcija, denaturacija in porazdelitev lipidov potekajo sočasno. Boljše ekstrakcijske rezultate dobimo, če najprej dodamo vodo in dobimo lizat (razbitje celice), nato metanol in na koncu še kloroform. Ekstrakcijska uspešnost je odvisna tako od biološke matrice kot od prisotnih lipidov. V literaturi je opisano, da lahko kloroform uspešno zamenjamo tudi z diklorometanom (Cequiez-Sanchez, 2008). 35
54 D o l o č a n j e l i p i d o v Primerjava ekstrakcijskih postopkov za izolacijo lipidov iz bioloških materialov Povzetek mnogih izvedb ekstrakcij in izolacij lipidov iz velikega števila vzorcev (membransko vezani lipidi), ki so na voljo v manjših količinah, je povzel Kolarovic (Kolarovic, 1986). Daae (Daae, 1970) ter Bjerve (Bjerve, 1974) s sodelavci sta ugotovila, da je dvofazni ekstrakcijski sistem n-butanol-voda boljši od sistema kloroform-metanol zaradi prodiranja v membransko strukturo, kjer raztaplja lipide, pri tem pa ostanejo proteini skoraj denaturirani. Hara in Radin (Hara, 1978) sta za ekstrakcijo predlagala enofazni sistem topil heksanizopropanol (3:2, v/v). Kolarovic (Kolarovic, 1986) opisuje svojo modifikacijo metode, ki sta jo predlagala Hara in Radin (Hara, 1978), kot enofazno ekstrakcijo lipidov s heksan-izopropanolom brez dodatnega postopka uporabe vode, kjer je ekstrakcija fosfolipidov učinkovitejša v enofaznem sistemu topil in kjer filtracijo nadomešča centrifugiranje. Ekstrakcijo lipidov iz rdečih krvnih celic sta opisala že Rose in Oklander (Rose, 1965). Razen dobre ekstrakcije lipidov (tudi fosfolipidov) po obstoječi metodi (Folch, 1957) je bila vsebnost izoliranega holesterola pri tej metodi prenizka. Njun predlog je bil zamenjava metanola z izopropanolom (ekstrakcijsko topilo kloroform-izopropanol (7:1, v/v)). Podobno metodo zasledimo tudi v literaturi (Freyburger, 1988) in (Broekhuyse, 1974), kjer za ekstrakcijo lipidov iz mikrobioloških kultur uporabijo heptan-izopropanol (1:4, v/v). Različne postopke ekstrakcije lipidov iz membran rdečih krvnih celic najdemo v številnih prispevkih (Greene, 2006), (Peet, 1998), (Peet, 2004). Razen klasične ekstrakcije tekoče tekoče s stresanjem se za ekstrakcijo lipidov lahko uporablja tudi mikrovalovna ekstrakcija (Vetter, 1998), (Batista, 2001) ali pospešena ekstrakcija (ASE) (Kuriki, 2008). Večina postopkov, ki so opisani v literaturi, se uporablja že leta, vendar nobeden ni privzet kot standardna metoda. 2.2 Adsorpcijska kromatografija lipidnih razredov Raznolikost lipidnih struktur zahteva pred njihovim določevanjem frakcioniranje vzorca in izolacijo želenih in iskanih lipidov. Strategija frakcioniranja je odvisna od ciljev naloge, od analitskega postopka, ki sledi frakcioniranju, in od instrumentalnih možnosti. V bioloških materialih se lipidi nahajajo kot kompleksne mešanice nevtralnih in polarnih lipidov z vsemi svojimi podrazredi. Najpogosteje lipidne razrede ločujemo s kolonsko ali s tankoplastno kromatografijo (TLC). Med prvimi objavami uporabe SPE na področju lipidov je bila izolacija gangliozidov v ekstraktu živalskega tkiva (Williams, 1980). Sledilo je frakcioniranje metabolitov arahidonske kisline (Powell, 1980). 36
55 D o l o č a n j e l i p i d o v Ekstrakcijo na trdni fazi (SPE-Si) sem uporabila zaradi želje po hitrem in enostavnem postopku ločevanja celokupnega lipidnega ekstrakta. Pri tem je za ločevanje glicerofosfolipidov, maščobnih kislin, holesteril estrov, glicerolipidov in sterolov mogoče razen silikagela uporabiti tudi druge stacionarne faze. Ekstrakcija na trdni fazi (SPE) je kolonska kromatografija, ki le zamenjuje ekstrakcijo tekoče-tekoče ter sledi osnovam tekočinske kromatografije. Trenutno je vodilna tehnika za hitro in selektivno pripravo vzorcev. SPE je uporabna tehnika tako za čiščenje vzorcev kot za izolacijo iskanih spojin. Rezultati retencije na nosilcih so posledica vodikove vezi, Van der Waalsovih sil in ionskih vezi. Značilne interakcije so npr. nepolarne interakcije. Nastopijo med C-H vezmi analita in C-H vezmi nosilca, kjer delujejo Van der Waalsove sile. Najbolj običajen nosilec za nepolarne interakcije je C18 faza, čeprav se za separacijo lipidov uporabljata tudi fazi C8 in C2. Polarne interakcije so vodikove vezi ali dipol-dipol sile. Te interakcije so značilne za nosilce, kjer je osnova ciano (CN), amino (NH 2 ) diol ali silika (Si). Tretja interakcija je ionsko izmenjevalna, ki nastane na fazi, kot so kvarterni amini, benzensulfonska kislina ali propilsulfonska kislina. Te interakcije nastopijo, kadar imajo analiti pozitiven ali negativen naboj. Lastnosti nekaterih SPE nosilcev so prikazane v Preglednici 2 1. Na teh nosilcih se lipidi zadržijo. Z naraščanjem polarnosti elucijskega topila se lipidi sproščajo z nosilca. Tako dosežemo grobo ločevanje skupnih lipidov. Na podobnih nosilcih z manjšimi delci pa lahko dosežemo tudi ločevanje posameznih lipidov. 37
56 D o l o č a n j e l i p i d o v Preglednica 2 1: Lastnosti SPE nosilcev. Princip separacije Nosilec Aktivne skupine Lastnosti silikagel adsorpcija silikagel -Si-OH nosilec je polaren, matrica nepolarna (nepolarne spojine gredo skozi polnilo glede na uporabljen eluent) modificiran silikagel (vezane skupine) porazdelitev silikagel -Si-(CH 2 ) 3 NH 2 -Si-(CH 2 )(CH 2 ) 3 CN -Si-(OH) 2 -Si-(CH 2 ) 3 OCH 2 CH(OH)CH 2 OH nosilec je srednje polaren (uporablja se kot alternativa silikagelu) porazdelitev C18 (oktadecil) -Si-C 18 H 37 nosilec je močno hidrofoben (nepolaren) (namenjen zadrževanju nepolarnih analitov iz vodnih raztopin) C8 (oktil) -Si-C 8 H 17 nosilec je srednje hidrofoben (nepolaren) (zadrži manj kot C18) C2 (etil) -Si-C 2 H 5 nosilec je nizko hidrofoben (nepolaren) fenil -Si-Ph ionska izmenjava kvarterni amin -Si-(CH 2 ) 3 N(CH 3 ) 3 + nosilec je močan anionski izmenjevalec propilbenzensulfonat propilsulfonat -Si-(CH 2 ) 3 C 6 H 4 -SO 3 - -Si-(CH 2 ) 3 SO 3 - močan kationski izmenjevalec 38
57 D o l o č a n j e l i p i d o v 2.3 Izolacija lipidnih razredov s podobno polarnostjo Najpogosteje lipidne razrede ločujemo s kolonsko kromatografijo ali s tankoplastno kromatografijo. Kolonska kromatografija na trdnem nosilcu je najpreprostejša metoda izolacije fosfolipidov od nevtralnih lipidov. Za ločevanje fosfolipidov iz celokupnega ekstrakta sem uporabila silikagel in modifikacijo metode po literaturi Juaneda in Rocquelin (1985). Za ločevanje lipidnih razredov se uporablja tudi aminski nosilec, ki so ga najprej testirali z vzorci mikrobioloških kultur (Bateman, 1997). Kmalu za tem je bil vpeljan celoten postopek separacije različnih lipidnih razredov (Kaluzny, 1985), ki so mu sledili drugi avtorji z modifikacijami metode, ki jo je predlagal Kaluzny (Ruiz, 2004), (Kim, 1990). Tudi ta postopek se, tako kot ekstrakcijski postopek lipidov po Folchu, uporablja kot osnovni postopek, s katerim so se primerjali vsi nadaljnji postopki. Za ločevanje lipidnih razredov (holesterol, holesteril ester, triglicerid, diglicerid, monoglicerid, maščobne kisline in fosfolipidi) se uporabljajo tri amino (SPE-NH 2 ) kolone in osem različnih eluentov (Kaluzny, 1985), (Ruiz-Gutierrez, 2000). Mogoča je tudi kombinacija obeh, tako SPE-Si in SPE-NH 2 nosilcev (Garcia Regueiro, 1994). Pomanjkljivost SPE-NH 2 nosilca je slabša ponovljivost in s tem majhna možnost prenosa v druge laboratorije ter močno zadrževanje fosfolipidov na nosilcu. Metoda je uporabna za izolacijo prostih maščobnih kislin iz celokupnega lipidnega ekstrakta po eluciji večine nevtralnih lipidov z mešanico topil kloroform-izopropanol (2:1, v/v). Proste maščobne kisline eluiramo z mešanico topil dietil eter-ocetna kislina (98:2, v/v). Aminska faza je uporabna tudi za izolacijo eikozanoidov (omogoča izolacijo leukotrienov E4, ki so pri človeku maščobne molekule imunskega sistema) (Kikawa, 1990). 2.4 Priprava metilnih estrov maščobnih kislin in dimetil acetalov z metanolno raztopino borovega trifluorida Med prve klasične študije priprave metilnih estrov maščobnih kislin in acetalov uvrščamo metodo, ki uporablja metanolno raztopino borovega trifluorida (BF 3 /MeOH) (Morrison, 1964) in je bila uporabljena za trigliceride, digliceride, monogliceride, proste maščobne kisline, sterolne estre, PE, PS, PC, PI in sfingomielin. S segrevanjem vzorca v metanolni raztopini borovega trifluorida se po predhodni alkalni hidrolizi v 1M raztopini natrijevega hidroksida v metanolu maščobne kisline pretvorijo v metilne estre. Pregled kromatografskih metod, ki se uporabljajo za določevanje estrov maščobnih kislin, je zbran v literaturi (Christie, 1993). Različni derivatizacijski postopki lahko vplivajo na rezultat vsebnosti maščobnih kislin. Pomanjkljivost BF 3 /MeOH reagenta opazimo v primeru določevanja maščobnih kislin v 39
58 D o l o č a n j e l i p i d o v mikroorganizmih, saj odpira obroče maščobnih kislin ter povzroča cis-trans izomerizacijo konjugiranih maščobnih kislin. Pri uporabi antioksidanta BHT (butil hidroksitoluen) lahko pride do pojavljanja dodatnih kromatografskih vrhov na kromatogramu. Možne so tudi nepopolne pretvorbe do metilnih estrov, strukturne spremembe ali nastanek drugih spojin. Prednost uporabe tega kislega reagenta je, da je reakcija hitrejša kot pri drugih reagentih, saj reagent vsebuje 20 % katalizatorja (BF 3 ) namesto 1 % do 5 %, kot ga vsebujejo ostali. Namesto metanolne raztopine borovega trifluorida lahko uporabimo metanolno žveplovo (VI) kislino (1 %) ali metanolni vodikov klorid (5 %), tako da dodajamo žveplovo (VI) kislino ali acetil klorid (CH 3 COCl) v metanol. Vendar pa noben derivatizacijski postopek ni zadovoljiv za vse tipe lipidov (Christie, 1993), (Schlechtriem, 2008) Kislinsko katalizirana esterifikacija in transesterifikacija Karboksilne kisline esterificiramo z alkoholi v prisotnosti ustreznega kislega katalizatorja, kot je prikazano na Sliki 2-1. Prva stopnja je protonacija kisline (kislina je tako bolj reaktivna), da dobimo oksonijev ion (1), kjer lahko poteče reakcija z alkoholom do intermediata (2), ki pri izgubi protona postane ester (3). Gre za reverzibilno reakcijo, kjer se v presežku alkohola ravnotežje premakne na stran esterifikacije. V prisotnosti vode reakcija ne poteče popolnoma do estrov. Po esterifikaciji katalizator odstranimo z vodo. Slika 2 1: Kislinsko katalizirana esterifikacija maščobnih kislin. Zamenjava estra ali transesterifikacija poteka pri podobnih pogojih (Slika 2-2). Pri tem začetni protonaciji estra sledi dodajanje drugega alkohola, da dobimo intermediat (4), kjer lahko preko intermediata (5) dobimo ester (6). Tudi pri teh reakcijah je potrebno odstraniti vodo. Slika 2 2: Kislinsko katalizirana transesterifikacija lipidov. 40
59 D o l o č a n j e l i p i d o v Osnovni pogoj za kislo katalizirano esterifikacijo karboksilnih kislin ali transesterifikacijo obstoječih estrov je prebitek alkohola v odsotnosti vode. Zato v reakcijsko mešanico dodajamo brezvodni natrijev sulfat. Borov trifluorid je kot Lewisova kislina v kompleksu z metanolom močen kisli katalizator za esterifikacijo maščobnih kislin. Esterifikacija je v prisotnosti BF 3 metanolnega kompleksa končana pod refluksom že po dveh minutah (Morrison, 1964). Borov trifluorid se lahko uporablja tudi z drugimi alkoholi, kjer pri tem nastajajo temu ustrezni estri (etil, propil, butil) Izolacija trans maščobnih kislin z ekstrakcijo na SPE Ag-Ion nosilcu Med določevanjem metilnih estrov maščobnih kislin kot gradnikov membranskih fosfolipidov so razen cis izomer v končnem ekstraktu po metiliranju prisotne v sledovih tudi trans izomeri maščobnih kislin. Za ločevanje trans maščobnih kislin sem uporabila SPE kolone s srebrovimi ioni (srebrovi ioni so vezani na SCX), ki tvorijo polarne komplekse z dvojnimi vezmi nenasičenih metilnih estrov maščobnih kislin (Slika 2 3, Ag-Ion SPE). Moč interakcije (nastanek π-vezi) narašča s številom dvojnih vezi. π-elektroni dvojnih vezi delujejo kot elektron donor, srebrovi ioni pa kot elektron akceptor. Slika 2 3: Shematski prikaz interakcij med Ag + in cis dvojnimi vezmi. Pri ločevanju maščobnih kislin iz ekstrakta kompleksne mešanice cis/trans izomer maščobnih kislin, sem sledila postopku v Preglednici 2 2. Preglednica 2 2: Ločevanje maščobnih kislin glede na število in cis/trans izomerizacijo dvojnih vezi na SPE Ag-Ion kolonah. Postopek SPE Ag-Ion Rezultat postopka Kondicioniranje 4 ml acetona 4 ml heksana Odstranimo vodo iz SPE faze. Priprava kolone na vzorec. Nanos vzorca 1mL (maks. 1mg FAME) pri 1 kapljici / sekundo Z večjim nanosom vzorca lahko zmanjšamo sposobnost ločevanja. 1. frakcija 6 ml heksana-acetona (95:5, v/v) Nasičene mašč. kisline trans-monoeni 2. frakcija 5 ml heksana-acetona (90:10, v/v) cis-monoeni trans-dieni 3. frakcija 5 ml acetona-acetonitrila (97:3, v/v) cis-dieni cis/trans-dieni trans-trieni cis/trans-trieni 4. frakcija 5 ml acetona-acetonitrila (94:6, v/v) cis-trieni 5. frakcija 5 ml acetona-acetonitrila (60:40, v/v) cis-tetraeni, pentaeni, heksaeni 41
60 D o l o č a n j e l i p i d o v Na Sliki 2-4 so prikazani kromatogrami standardne raztopine Supelco 37 FAME Mix U in petih frakcij. Slika 2 4: GC-FID kromatogram standardne raztopine Supelco 37 FAME Mix U a), kromatogram izoliranih nasičenih in trans monoen maščobnih kislin b), kromatogram izoliranih cis monoen maščobnih kislin in trans dien maščobnih kislin c), kromatogram izoliranih cis dien, cis/trans dien maščobnih kislin, trans trien ter cis/trans trien maščobnih kislin d), kromatogram izoliranih cis trien maščobnih kislin e) in kromatogram izoliranih cis tetraen, penta in heksaen maščobnih kislin f). Iz kromatogramov vidimo, da med nasičenimi maščobnimi kislinami in nosilcem ni interakcij. Zato pa so med cis dvojnimi vezmi maščobnih kislin in Ag-Ion nosilcem interakcije večje kot med trans dvojnimi vezmi maščobnih kislin. 42
61 D o l o č a n j e l i p i d o v Razlike v moči zadrževanja med različnimi skupinami maščobnih kislin in Ag-Ion nosilcem so tisti mehanizmi, ki omogočajo ločevanje cis in trans izomer tudi pri zelo kompleksnih vzorcih, kot je hidrogenirano rastlinsko olje (Slika 2-5). Slika 2 5: GC-FID kromatogram rastlinskega olja a), kromatogram izoliranih nasičenih in trans monoenskih maščobnih kislin (18:1 trans izomere 1. frakcija) b), kromatogram izoliranih cis monoenskih maščobnih kislin (18:1 cis izomere 2. frakcija) c). 43
62 E k s p e r i m e n t a l n i d e l 3 EKSPERIMENTALNI DEL 3.1 Materiali in metode Pribor in aparati Plinski kromatograf s plamensko ionizacijskim detektorjem (FID) proizvajalca Agilent Technologies, AT 6890N (Wilmington, DE, ZDA) z avtomatskim injektorjem AT 7683B proizvajalca Agilent Technologies (Wilmington, DE, ZDA). Plinski kromatograf AT 6890N z masno selektivnim kvadrupolnim detektorjem Agilent Technologies, AT 5973N (Wilmington, DE, ZDA). Analitska tehtnica, Mettler Toledo, AX205DR/M (Greifensee, Švica). Električni grelni blok za epruvete, TBTE, Krokter Marijan s.p. Rotacijski stresalnik, Vibromix10, Tehtnica Železniki (Železniki, Slovenija). Centrifuga, 3-18K, Sigma (Osterode am Harz, Nemčija). Uparjevalnik, Caliper, TurboVap LV (Massachusetts, ZDA). Steklena vakuumska SPE enota, Visiprep, U, Supelco (Bellefonte, ZDA). Kromatografska kapilarna kolona (kapilarna kolona, SP 2560, 75 m, 0,14 m debelina filma, 0,18 mm I.D.), U, Supelco (Bellefonte, ZDA). SPE Bond Elut-Si kolone 3 ml / 500 mg, , Varian (Middelburf, Nizozemska). SPE Discovery Ag-Ion SPE kolone, 750 mg / 6ml, U, Supelco (Bellefonte, ZDA). Steklenička za avtomatski injektor (2ml). Epruvete z obrusom (10 ml, 20 ml). Zračni hladilnik. Vrelni kamenčki. Pipete. TLC plošče silika gel (20 x 20 cm), debelina nanosa 250 μm, , Merck (Darmstadt, Nemčija). Steklena dvoprekatna kadička s steklenim pokrovom za razvijanje TLC plošč, , Camag (Muttenz, Švica). Steklena kadička za potapljanje TLC plošč 20 x 20 cm, , Camag (Muttenz, Švica). Steklene kapilare za nanos na TLC plošče, 5 μl, , Camag (Muttenz, Švica) Kemikalije in reagenti n-heksan, CAS , C 6 H 14, J.T. Baker 9262 (Deventer, Nizozemska). Kloroform, CAS , CHCl 3, J.T.Baker 7018 (Deventer, Nizozemska) ali Fluka (Buchs, Švica). Metanol, CAS , CH 3 OH, Sigma Aldrich (Steinheim, Nemčija) ali J.T. Baker 8402 (Deventer, Nizozemska). Etanol, CAS , C 2 H 5 OH, Sigma Aldrich (Steinheim, Nemčija). Dietileter, CAS , (CH 3 CH 2 ) 2 O, J.T. Baker 9259 (Deventer, Nizozemska). 44
63 E k s p e r i m e n t a l n i d e l Etanojska kislina (ocetna kislina), CAS , CH 3 COOH, Fluka (Buchs, Švica). Voda, ultra resi, CAS , H 2 O, J.T. Baker 4219 (Deventer, Nizozemska). Fosformolibdenova kislina, CAS , H 3 PMo 12 O 40 aq., Fluka (Buchs, Švica). Pripravila sem etanolno raztopino tako, da sem raztopila 8,5 g fosformolibdenove kisline v 200 ml etanola. Natrijev sulfat, brezvodni, CAS , Na 2 SO 4, Merck (Darmstadt, Nemčija). Žarila sem ga 4 h ± 30 min pri 500 C ± 20 C ter nato ohladila v žarilni peči. Natrijev klorid, CAS , NaCl, Merck (Darmstadt, Nemčija) ali J.T. Baker 0278 (Deventer, Nizozemska). Pri delu sem uporabila nasičeno raztopino natrijevega klorida in 0,9 % raztopino, ki sem jo pripravila tako, da sem raztopila 0,9 g natrijeve soli in dopolnila z vodo do 100 ml v stekleno merilno bučko. Natrijev hidroksid, CAS , NaOH, J.T. Baker 0288 (Deventer, Nizozemska). Raztopina natrijevega hidroksida v metanolu (0,5 mol L -1 ). Pripravila sem jo tako, da sem raztopila 2 g natrijevega hidroksida v 100 ml metanola v stekleni merilni bučki. Raztopina borovega trifluorida v metanolu (BF 3 /MeOH), Merck , 20 % raztopina (Darmstadt, Nemčija). Reagent je stabilen pri temperaturi od 4 ºC do 8 ºC in obstojen nekaj mesecev. Raztopina fosfatnega pufra (PBS, ph = 7,4), Medicago (Upsala, Švedska), ki se uporablja v bioloških raziskavah. Vsebuje NaCl (8,00 g L -1 ), KCl (0,20 g L -1 ), Na 2 HPO 4 (1,44 g L -1 ), KH 2 PO 4 (0,24 g L -1 ). Ficoll-Paque PLUS reagent, GE Healthcare (Upsala, Švedska). Reagent se uporablja za izolacijo levkocitov Priprava steklovine Večja občutljivost analitskih tehnik in nizke koncentracije lipidov v bioloških materialih zahtevajo uporabo zelo čistih topil in steklovine. Pri delu sem se poskušala izogniti kontaminaciji z mineralnimi olji, maščobami, plastično embalažo in detergentom. Vse postopke sem izvajala v stekleni opremi (epruvete, zamaški, kadičke, pipete). Razen teflona nisem uporabljala druge plastične opreme, zaradi katere bi lahko nastale neznane lise na TLC ploščah ali dodatni vrhovi pri plinski kromatografiji Ekstrakcijska topila Za analizne postopke sem uporabljala topila čistote, ki je namenjena analitiki sledov. Da bi se izognila kontaminaciji lipidov z nehlapnimi snovmi iz topila, sem poskušala delati s topili z vsebnostjo manj kot 5 mg suhe snovi na liter topila. Najbolj sprejemljiva koncentracija suhe snovi je 1 mg L
64 E k s p e r i m e n t a l n i d e l V ekstraktu so lahko prisotne tudi moteče nelipofilne molekule (npr. proteini). Te lahko iz lipidnega ekstrakta odstranimo tako, da ekstrakt posušimo do suhega, dodamo majhno količino metanola, ki je zelo dobro denaturacijsko sredstvo, in ponovno posušimo. Ponovno raztopimo suhi lipidni ekstrakt v mešanici topil kloroform-metanol (2:1, v/v) in ga prenesemo v drugo epruveto. Končna lipidna faza v kloroformu po centrifugiranju ne vsebuje ostankov proteinov Standardni materiali metilnih estrov maščobnih kislin Supelco 37 FAME Mix U. Restek AOCS standard : 14:0, 1,0 %; 16:0, 4,0 %; 18:0, 3,0 %; 18:1n9, 45,0 %; 18:2n6, 15,0 %; 18:3n3 ALA, 3,0 %; 20:0, 3,0 %; 22:0, 3,0 %; 22:1n9, 20,0 % in 24:0 3,0 % ali Supelco FAME Mix A: 14:0, 1,0 %; 16:0, 4,0 %; 18:0, 3,0 %; 18:1n9, 60,0 %; 18:2n6, 12,0 %; 18:3n3 ALA, 5,0 %; 20:0, 3,0 %; 20:1n9, 1,0 %; 22:0, 3,0 %; 22:1n9, 5,0 % in 24:0 3,0 %. Restek cis/trans FAME Mix 35079: 18:0, 20,0%; 18:1 6t, 8,0 %; 18:1 9t, 10,0 %; 18:1 11t, 12,0 %; 18:1 6c, 8,0 %; 18:1 9c, 10,0 %; 18:1 11c, 12,0 %, 18:2n6, 20,0 %. Supelco 18:2 (linolna) cis/trans FAME Mix 47791: 18:2 9t12t, 50,0 %; 18:2 9c12t, 20,0 %; 18:2 9t12c, 20,0 %; 18:2n6, 10,0 %. Supelco 18:3 (linolenska) cis/trans FAME Mix 47792: 18:3 9t12t15t, 30,0 %; 18:3 9t12t15c, 18:3 9t12c15t, 18:3 9c12t15t, 45,0 %; 18:3 9c12c15t, 18:3 9c12t15c, 18:3 9t12c15c, 21,0 %; 18:3n3 ALA, 4,0 %. Standardne materiale sem hranila v zamrzovalniku pri 20 ºC Standardni materiali predstavnikov lipidnih razredov HC: alifatski ogljikovodiki tetrakozaheksaen Sigma-Aldrich, CAS molekulska formula C 30 H 50. WE: estri voskov stearil palmitat stearil ester palmitinske kisline Sigma-Aldrich, P3512 CAS molekulska formula C 34 H 68 O 2. SE: sterolni estri holesteril stearat 5-holesten-3β-il oktadekanoat holest-5-en-3-beta-il oktadekanoat Sigma-Aldrich C79409 CAS molekulska formula C 45 H 80 O 2. Slika 3 1: Skvalen. Slika 3 2: Stearil palmitat. Slika 3 3: Holesteril stearat. 46
65 E k s p e r i m e n t a l n i d e l KET: ketoni 3-heksadekanon Sigma-Aldrich H7504 CAS molekulska formula C 16 H 32 O. TAG: triacilgliceroli gliceril tripalmitat glicerol tripalmitat tripalmitin Sigma-Aldrich CAS molekulska formula C 51 H 98 O 6. MAG: monoacilglicerol DL-α-palmitin α-monopalmitin 1-monopalmitoil-rac-glicerol 1-monoheksadekanoilrac-glicerol rac-glicerol-1-palmitat gliceril monopalmitat Sigma-Aldrich M1640 CAS molekulska formula C 19 H 38 O 4. FFA: proste maščobne kisline palmitinska kislina heksadekanojska kislina Sigma-Aldrich P0500 CAS molekulska formula C 16 H 32 O 2. FA: maščobni alkohol cetil alkohol 1-heksadekanol palmitil alkohol Sigma-Aldrich CAS molekulska formula C 16 H 34 O. ST: sterolni lipidi holesterol (HST) 3β-hidroksi-5-holesten 5-holesten-3β-ol Sigma-Aldrich C8667 CAS molekulska formula C 27 H 46 O. Slika 3 4: 3-heksadekanon. Slika 3 5: Gliceril tripalmitat. Slika 3 6: Gliceril monopalmitat. Slika 3 7: Palmitinska kislina. Slika 3 8: Cetil alkohol. Slika 3 9: Holesterol. 47
66 E k s p e r i m e n t a l n i d e l Fosfolipidi (PL): PC: L-α-fosfatidilholin 1,2-diacil-sn-glicero-3-fosfoholin 3-sn-fosfatidilholin L-α-lecitin Sigma-Aldrich CAS molekulska formula C 42 H 80 NO 8 P. izvor: jajčni beljak. PE: L-α-fosfatidiletanolamin 1,2-diacil-sn-glicero-3 fosfoetanolamin 3-sn-fosfatidiletanolamin L-α-kefalin Sigma-Aldrich P8068 CAS molekulska formula C 41 H 78 NO 8 P. izvor: Escherichija coli. PS: 3-sn-fosfatidil-L-serin L-α-fosfatidil-L-serin Sigma-Aldrich molekulska formula C 42 H 78 NO 10 P. izvor: možganovina govedi. SM: Sfingomielin Sigma-Aldrich S7004 CAS molekulska formula C 41 H 84 N 2 O 6 P. izvor: možganovina govedi. Slika 3 10: L-α-lecitin. Slika 3 11: L-α kefalin. Slika 3 12: 3-sn-fosfatidil-L-serin. Slika 3 13: Sfingomielin. 48
67 E k s p e r i m e n t a l n i d e l Priprava osnovnih standardnih raztopin lipidov Metodo ločevanja lipidov s SPE sem optimizirala z metodo tankoplastne kromatografije s standardnimi raztopinami predstavnikov lipidnih razredov. Natehtala sem približno 10 mg čiste spojine lipida in jo raztopila v kloroformu v 10 ml merilni bučki. Koncentracija posameznega lipida je bila približno 1 mg ml Priprava delovne standardne raztopine lipidov Iz vsake osnovne standardne raztopine sem z injekcijsko brizgo odvzela 5 μl raztopine lipida v kloroformu (tetrakozaheksaen - HC, stearil palmitat - WE, holesterilstearata - SE, gliceril monopalmitat - MAG, heksadekanojska kislina - FFA, cetil alkohol - FA, holesterol - HST, 3-sn-fosfatidiletanolamin - PE, 3-sn-fosfatidilholin - PC, sfingomielin - SM in 3-sn-fosfatidilserin - PS) in jih prenesla v 2 ml stekleničko, kjer sem jih skoncentrirala do suhega ter ponovno raztopila v 10 μl kloroforma. za točkovni nanos na TLC ploščo sem uporabila 5 μl kapilaro za nanos na silika SPE nosilec sem mešanico delovne standardne raztopine raztopila v 500 μl kloroforma Pred vsako uporabo sem standardne raztopine termostatirala pri sobni temperaturi 30 minut. 3.2 Priprava vzorcev Etična ustreznost Vzorce eritrocitov, ki so bili izolirani iz krvi ljudi z različnimi boleznimi, sem dobila od predhodno opravljenih genetskih študij s Fakultete za medicino, Centra za humano molekularno genetiko in farmakogenomiko Univerze v Mariboru, za katere je bila pridobljena etična ustreznost (Potočnik, 2004), (Berce, 2008), (Pakiz, 2010). Shranila sem jih pri temperaturi 80 ºC Izolacija eritrocitov Vzorci krvi so bili pripravljeni po naslednjem postopku : 9 ml krvi v epruveti z EDTA dodamo 9 ml solnice fosfatnega pufra (PBS) in 9 ml Ficoll-Paque PLUS reagenta. Sledi stresanje na rotacijskem stresalniku. Po 30 min centrifugiranju pri 1800 obratih pri 18 ºC odvzamemo zgornje plasti, ki vsebujejo serum, levkocite in Ficoll reagent. Na dnu ostanejo eritrociti (Slika 3-14). Slika 3 14: Shematski prikaz vzorca krvi po centrifugiranju. 49
68 E k s p e r i m e n t a l n i d e l Postopek ekstrakcije lipidov rdečih krvnih celic Do začetka analize sem vzorce eritrocitov hranila v teflonskih epruvetah pri 80 ºC. Pred ekstrakcijo celokupnih lipidov sem vzorec eritrocitov odmrznila in ga pustila stati pri sobni temperaturi 30 min. Sledila je 15- sekundna homogenizacija na rotacijskem stresalniku. S pipeto sem odvzela 500 μl homogenega vzorca eritrocitov in jih prenesla v stekleno epruveto (Slika 3 15, a). Lipide sem ekstrahirala po modificirani metodi (Folch, 1957), tako da sem uporabila končno razmerje topil 0,9 % NaCl raztopine-kloroform-metanol (0.2:2:1, v/v/v). Pri tem postopku je pomembno, da sem ekstrakcijska topila dodajala postopoma in ne kot skupno mešanico, kot je to v uporabi pri vseh do sedaj uporabljenih metodah ekstrakcij tekoče-tekoče. Pri tem sem se izognila hitri in hkratni denaturaciji beljakovin, kar vpliva na izkoristek ekstrakcije lipidov. Boljši izkoristek sem dobila pri postopnem dodajanju topil. K vzorcu sem najprej dodala 500 μl 0,9 % raztopine NaCl in dobila raztopino, ki je vsebovala»razbite«celične membrane ter vsebino celice»lizat«(slika 3-15, b). Vzorec sem stresala 15 sekund na rotacijskem stresalniku. Postopoma sem med stresanjem po kapljicah dodajala najprej 2,5 ml metanola in nato še 5 ml kloroforma, kjer je najprej potekala denaturacija proteinov, ki mu je sledila ekstrakcija lipidov (Slika 3-15, c). a b c Slika 3-15: Prenos vzorca rdečih krvnih celic v epruveto a), dodajanje solnice in priprava»lizata«b), postopno dodajanje ekstrakcijskih topil c). Za ločitev ekstrakta sem potrebovala 15- minutno centrifugiranje pri 3000 obr min -1 (Slika 3-16, a) pri temperaturi 22 ºC. V epruveti je po centrifugiranju med obema fazama ostal proteinski obroč, mimo katerega sem odvzela spodnjo fazo kloroforma, ki je vseboval celokupne lipide in ga prenesla v drugo epruveto (Slika 3-16, b, c). Nato sem odstranila vodo z dodatkom brezvodnega natrijevega sulfata, prenesla ekstrakt v drugo epruveto in pustila stati v hladilniku nekaj ur, da se je na vrhu ekstrakcijskega topila izločilo še približno 100 μl metanola z raztopljenimi naravnimi nelipidnimi 50
69 E k s p e r i m e n t a l n i d e l spojinami (glej 3.1.4). Lipidni ekstrakt v kloroformu sem koncentrirala 10 minut pod tokom dušika v vodni kopeli pri 35 ºC do suhega. a b c Slika 3-16: Prenos epruvet v centrifugo a), vzorci po centrifugiranju b), prenos lipidnega ekstrakta v kloroformu c). Izkoristek ekstrakcije po postopnem dodajanju ekstrakcijskih topil v primerjavi s hkratnim dodajanjem mešanice topil sem preskusila na dveh nizih vzorcev rdečih krvnih celic. Vsak niz je vseboval pet dvojic vzorcev. Prvih pet vzorcev obeh nizov sem pripravila tako, da sem ekstrakcijska topila dodajala postopoma, drugim petim vzorcem obeh nizov vzorcev pa sem dodala mešanico ekstrakcijskih topil (Folch, 1957). Vsebnost lipidov sem v končnem ekstraktu kloroforma po sušenju in koncentriranju določila s tehtanjem. Na Sliki 3-17 vidimo ekstrakte pred centrifugiranjem (epruveti A in B) in po centrifugiranju (epruveti C in D), ko sem vzorcu eritrocitov dodajala ekstrakcijska topila postopoma (epruveti A in C), in ko sem jih dodala kot mešanico topil (epruveti B in D). V prvem primeru je ekstrakcija lipidov potekala ves čas mešanja na rotacijskem stresalniku. Denaturirane beljakovine so bile ves čas porazdeljene po celotnem ekstraktu. Ko pa sem dodala k vzorcu mešanico topil, so se beljakovine v trenutku zgostile v trdo kepasto snov, ki se ni porazdelila po ekstrakcijskem topilu. Razlika med obema postopkoma je bila vidna tudi po centrifugiranju. Slika 3-17: V epruveti A in C je vzorec eritrocitov pred in po centrifugiranju, pripravljen po postopnem dodajanju topil metanola (2,5 ml) in kloroforma (5 ml). V epruveti B in D je vzorec eritrocitov pred in po centrifugiranju, pripravljen po ekstrakciji z mešanico topil 7,5 ml, metanol-kloroform (1:2, v/v/). 51
70 E k s p e r i m e n t a l n i d e l Shranjevanje lipidnih ekstraktov Ekstrakte izoliranih lipidov ne smemo puščati v suhem stanju, ampak morajo biti raztopljeni v topilu (npr. kloroform). Z dodatkom topila se upočasni oksidativni razpad. Ekstrakte zaščitimo pred zrakom in svetlobo. Shranjevanje vzorcev pri 80 ºC ne spremeni sestave maščobnih kislin eritrocitov do 4 let (Hodson, 2002) Izolacija fosfolipidov z ekstrakcijo na trdni fazi (SPE) Po končani ekstrakciji kompleksne mešanice celokupnih lipidov eritrocitov sem morala le še izolirati fosfolipide, v katerih sem želela določevati maščobne kisline in njihove profile pri skupinah bolnikov. Skoncentrirani lipidni ekstrakt sem raztopila v 500 μl kloroforma (Slika 3-18, a) in ga stresala na rotacijskem stresalniku, da se je ekstrakt raztopil in homogeniziral. SPE-silika sem kondicionirala s 5 ml metanola in nato še s 5 ml kloroforma in pri tem uporabila podtlak do 1 mm Hg (Slika 3-18, b). Nato sem nanesla vzorec na SPE (Slika 3-18, c). Epruveto sem še dvakrat oplaknila s 500 μl kloroforma in nanesla v SPE ter pustila, da je topilo brez podtlaka pronicalo skozi polnilo. Ko je topilo steklo skozi polnilo, sem s podtlakom odsesala preostanek topila. Pri tem so lipidi ostali na polnilu. Sledilo je spiranje SPE kolone s 5 ml kloroforma in 5 ml mešanice topil kloroform-metanol (49:1, v/v), tako da sem odstranila nevtralne lipide skupaj s prostimi maščobnimi kislinami. Ko sem odstranila podtlak, sem v kolono nanesla 5 ml metanola in eluirala fosfolipide. Pustila sem, da je metanol prosto pronical skozi polnilo ter na koncu s podtlakom odsesala še preostanek topila. V metanolnem eluatu sem dobila izolirane fosfolipide. a b c d Slika 3-18: Lipidni ekstrakt v kloroformu a), postopek kondicioniranja SPE b), nanos ekstrakta na SPE c). Postopek izolacije fosfolipidov je prikazan v Preglednici
71 E k s p e r i m e n t a l n i d e l Preglednica 3 1: Ločitev fosfolipidov (PL) na SPE-Si koloni. Kondicioniranje Nanos vzorca Spiranje polnila (eluat I) Elucija PL (eluat II) 5 ml metanola 5 ml kloroforma 500 μl v kloroformu. Speremo epruveto z 2 x 500 μl kloroforma, premešamo in dodamo na SPE. 5 ml kloroforma 5 ml kloroforma-metanola (49:1, v/v) Uporaba podtlaka manj kot 1 mm Hg. Polnila ne posušimo. Pustimo prosto teči. Vključimo podtlak.* Pustimo prosto teči. Vključimo podtlak.* 5 ml metanola Pustimo prosto teči. Vključimo podtlak.* * šele ko vse topilo prosto steče skozi adsorbent, odsesamo preostanek topila s podtlakom. Pri postopku spiranja polnila eluiramo nevtralne lipide (mono-, di- in triacilglicerole, holesteril estre, holesterol in proste maščobne kisline) Priprava metilnih estrov maščobnih kislin Estre maščobnih kislin sem pripravila po mednarodnih standardih ISO 5508/9 (Animal and vegetable fats and oils, ISO 5508:1990(E), ISO 5509:2000 (E)). Fosfolipide rdečih krvnih celic sem najprej hidrolizirala v alkalnem in pri tem sprostila maščobne kisline iz sn-1 in sn-2 glicerolne osnove. Fosfolipidni ekstrakt v metanolu sem skoncentrirala do približno 500 μl in mu dodala 2 ml 0,5 M raztopine natrijevega hidroksida v metanolu ter vrelni kamenček. Epruveto sem povezala z zračnim hladilnikom. Vreti sem pustila 15 minut pri temperaturi 70 C (Slika 3-19, a). Skozi zračni hladilnik sem dodala kisli katalizator metanolno raztopino borovega trifluorida (BF 3 /MeOH) in pustila vreti še vsaj 5 minut. Vzorce sem odstranila iz grelnega bloka v stojalo in skozi zračni hladilnik dodala 5 ml heksana (Slika 3-19, b). Takoj, ko sem odstranila zračni hladilnik, sem dodala 5 ml nasičene raztopine natrijevega klorida (Slika 3-19, c). Epruveto sem stresala 15 sekund in pustila, da sta se fazi ločili. Heksansko plast sem prenesla v epruveto, ki sem ji dodala približno pol čajne žličke brezvodnega natrijevega sulfata. 1 ml heksanskega ekstrakta sem prenesla v graduirano epruveto ali 5 ml merilno bučko in jo dopolnila do 5 ml. Tako pripravljen vzorec je bil pripravljen za GC/FID analizo. Za kontrolo analiznega postopka sem vzporedno pripravila slepi vzorec, kjer sem uporabila le reagente. 53
72 E k s p e r i m e n t a l n i d e l a b c Slika 3-19: Alkalna hidroliza fosfolipidov v grelnem bloku a), dodajanje heksana b), dodajanje nasičene raztopine natrijevega klorida c). Za ločevanje trans maščobnih kislin sem uporabila SPE s polnilom Ag-Ion po postopku, ki je prikazan v Preglednici 3 2. Uporabila sem modificirano metodo ISO (SIST EN ISO 15304, Animal and vegetable fats and oils, 2002). Preglednica 3 2: Ločevanje trans maščobnih kislin (TFA) na SPE Ag-Ion. Kondicioniranje 4 ml acetona 4 ml heksana Odstrani vodo iz SPE faze. Priprava kolone na vzorec. Nanos vzorca 1 ml FAME v heksanu Pustimo prosto teči. (maks. 1 mg FAME) 1. elucija 6 ml heksan-aceton (95:5, v/v) Pustimo prosto teči. Vključimo podtlak 2. elucija 5 ml heksan-aceton (90:10, v/v) Pustimo prosto teči. Vključimo podtlak. Nanos vzorca in vse elucije so potekale pri hitrosti pretoka ena kapljica na sekundo. Pomembno je, da po vsaki eluciji topilo s podtlakom popolnoma odsesamo iz polnila, vendar le do trenutka, ko opazimo, da je SPE kolona že suha in da topila v polnilu ni več. Končna prostornina posameznih frakcij je bila 1 ml. 54
73 E k s p e r i m e n t a l n i d e l 3.3 Plinska kromatografija Metilne estre maščobnih kislin sem določila na plinskem kromatografu AT6890 s plamensko ionizacijskim detektorjem (FID). Primerljivost določevanja estrov maščobnih kislin s plamensko ionizacijskim detektorjem in masno selektivnim detektorjem je opisana v literaturi (Dodds, 2005) Instrumentalni pogoji T inj : 230 ºC T det : 300 ºC Temperaturni 140 ºC (1 min), 10 ºC min -1 do 180 ºC (5 min), 1.5 ºC min -1 do 230 ºC program: (1,1 min), 5 ºC min -1 do 235 ºC (12,57 min). Čas analize: 58 min Nosilni plin: He 6,0 (40 psi, 0,4 ml min -1 ) Detektor: FID; (zrak 300 ml min -1, H 2 35 ml min -1, make up He 6,0 (10 ml min -1 ) Razdelitveno razmerje: 100:1 (»split«). 3.4 Določevanje maščobnih kislin fosfolipidov Metoda izračuna masnega deleža metilnih estrov maščobnih kislin Vsebnost estrov maščobnih kislin sem izrazila v odstotkih (masni delež, %) po enačbi (1) glede na vse identificirane maščobne kisline. Pri tem sem uporabila metodo normalizacije, kjer je vsota ploščin kromatografskih vrhov, ki predstavljajo maščobne kisline, 100 %. Ci masni delež spojine i Ai ploščina vrha i A... vsota ploščin vseh vrhov Ci = (Ai / Ai ) 100 (1) Masni delež (%) dimetil acetalov izračunamo glede na vse identificirane maščobne kisline po enačbi (1) Identifikacija maščobnih kislin Estre maščobnih kislin v vzorcih sem identificirala s primerjanjem njihovih retencijskih časov na kromatogramu in retencijskih časov estrov maščobnih kislin na kromatogramu standardnih raztopin spojin. Na spodnjih slikah so kromatogrami standardnih spojin metilnih estrov maščobnih kislin. 55
74 E k s p e r i m e n t a l n i d e l Slika 3 20: GC-FID kromatogram standardne raztopine mešanice 37 metilnih estrov maščobnih kislin. (Supelco 37 FAME Mix U), mešanice cis/trans izomer 18:1 kisline (Restek cis/trans FAME Mix 35079), mešanice cis/trans izomer 18:2 kislin (Supelco 18:2 (linolna) cis/trans FAME Mix 47791) in mešanice cis/trans izomer 18:3 kislin (Supelco 18:3 (linolenska) cis/trans FAME Mix 47792). Identifikacija spojin posameznih kromatografskih vrhov je razvidna iz kromatogramov na Slikah 3 21, 3 22, 3 23,
75 E k s p e r i m e n t a l n i d e l Slika 3 21: GC-FID kromatogram standardne raztopine mešanice 37 metilnih estrov maščobnih kislin (Supelco 37 FAME Mix U). Identifikacija kromatografskih vrhov: (1) 4:0, (2) 6:0, (3) 8:0, (4) 10:0, (5) 11:0, (6) 12:0, (7) 13:0, (8) 14:0, (9) 14:1n5, (10) 15:0, (11) 15:1n5, (12) 16:0, (13) 16:1n7, (14) 17:0, (15) 17:1n7, (16) 18:0, (17) 18:1n9t, (18) 18:1n9c, (19) 18:2n6t, (20) 18:2n6c, (21) 20:0, (22) 18:3n6 GLA, (23) 20:1n9, (24) 18:3n3 ALA, (25) 21:0, (26) 20:2n6, (27) 22:0, (28) 20:3n6 DGLA, (29) 22:1n9, (30) 20:3n3, (31) 20:4n6 AA, (32) 23:0, (33) 22:2n6, (34) 24:0, (35) 20:5n3 EPA, (36) 24:1n9, (37) 22:6n3 DHA. 57
76 E k s p e r i m e n t a l n i d e l Slika 3 22: GC-FID kromatogram standardne raztopine mešanice cis/trans izomer 18:1 kislin (Restek cis/trans FAME Mix 35079). Identifikacija kromatografskih vrhov: (1) 18:0, (2) 18:1n12t, (3) 18:1n9t, (4) 18:1n7t, (5) 18:1n12c, (6) 18:1n9c, (7) 18:1n7c, (8) 18:2n6. Slika 3 23: GC-FID kromatogram standardne mešanice cis/trans izomer 18:2 kislin (Supelco 18:2 (linolna) cis/trans FAME Mix 47791). Identifikacija kromatografskih vrhov: (1) 18:2n6t, (2) 18:2-9c12t, (3) 18:2-9t12c, (4) 18:2n6c. Slika 3 24: GC-FID kromatogram standardne mešanice cis/trans izomer 18:3 kislin (Supelco 18:3 (linolenska) cis/trans FAME Mix 47792). Identifikacija kromatografskih vrhov: (1) 18:3n3t, (2) 18:3-9t12t15c, (3) 18:3-9t12c15t, (4) 18:3-9c12t15t, (5) 18:3-9c12c15t, (6) 18:3-9c12t15c, (7) 18:3-9t12c15c, (8) 18:3n3c ALA. 58
77 E k s p e r i m e n t a l n i d e l Identifikacija dimetil acetalov Dimetil acetale (16:0 DMA and 18:0 DMA) sem identificirala s plinsko kromatografijo z masno selektivnim detektorjem. Spojine sem ionizirala z elektroni energije 70 ev. Kromatogrami in EI masna spektra obeh dimetil acetalov so prikazani na Sliki 3 25 in Slikah 3 26, Abundance Ion (74.70 to 75.70): D Time--> Abundance Ion ( to ): D Time--> Abundance Ion ( to ): D Time--> Slika 3 25: GC-MS kromatogrami izbranih fragmentnih ionov (za heksadekanal dimetil acetal (16:0 DMA) in oktadekanal dimetil acetal (18:0 DMA) (m/z = 75, m/z = 255 in m/z = 283)) ekstrakta fosfolipidov rdečih krvnih celic. 59
78 E k s p e r i m e n t a l n i d e l Abundance Average of to min.: D (-) m/z--> Slika 3 26: Masni spekter heksadekanal dimetil acetala (16:0 DMA) z značilnim fragmentnim ionom m/z = 75 (CH(CH 3 O) 2 + ) in m/z = 255 (M + = 286). Abundance Average of to min.: D (-) m/z--> Slika 3 27: Masni spekter oktadekanal dimetil acetala (18:0 DMA) z značilnim fragmentnim ionom m/z = 75 (CH(CH 3 O) 2 + ) in m/z = 283 (M + = 314). 3.5 Optimizacija ločevanja lipidnih razredov s TLC in SPE-Si Tankoplastna kromatografija (TLC) je ena najučinkovitejših in hitrih tehnik za ločevanje kompleksnih lipidnih mešanic. V nalogi sem jo uporabila za ločevanje in kvalitativno določevanje različnih lipidnih razredov in kontrolo ločevanja lipidnih razredov na SPE- Si Tankoplastna kromatografija (TLC) Standardno raztopino mešanice lipidov in posamezne standardne raztopine lipidov, ki sem jih raztopila v kloroformu, sem enakomerno točkovno nanesla s 5 μl kapilaro na črto približno 2 cm od spodnjega roba plošče in oddaljeno ena od druge približno 2 cm. Po nanosu standardnih raztopin spojin sem ploščo potopila v razvijalno raztopino v dvoprekatno kadičko, ki je bila nasičena s hlapi topil. Kadičko sem pokrila s steklenim pokrovom. Topilo sem pustila potovati po plošči do označene razdalje (enostopenjsko enodimenzionalno razvijanje). Ploščo sem nato vzela iz kadičke in jo pustila, da se je v digestoriju posušila. Nato sem jo potopila v derivatizacijsko etanolno raztopino hidrata fosformolibdenove kisline. Ploščo sem nato sušila v peči 30 min pri 150 ºC. 60
79 E k s p e r i m e n t a l n i d e l Preskušanje razvijalnih raztopin za TLC Za TLC razvijanje sem preskušala nekaj mešanic topil. Izbor TLC razvijalnih raztopin: 1: Kloroform-metanol-voda (65:25:4, v/v/v) 2: Kloroform-metanol-ocetna kislina (100:5:2, v/v/v) 3: Heksan-dietileter-metanol-ocetna kislina (90:20:5 : 2, v/v/v/v) 4: Heksan-dietileter (65:35, v/v) A) Uporaba različnih razvijalnih raztopin za ločevanje lipidov Za nanos na ploščo sem uporabila osnovne standardne raztopine lipidov (glej 3.1.8). Slika 3 28: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini 1. Slika 3 29: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini 2. Slika 3 30: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini 3. Slika 3 31: TLC kromatogram lipidov standardnih raztopin v razvijalni raztopini 4. 61
80 E k s p e r i m e n t a l n i d e l Razvijalna raztopina 1: Razvijalna raztopina 2: Razvijalna raztopina 3: Razvijalna raztopina 4: Ločeni razredi PL od drugih lipidnih razredov in med seboj. Razen PL medsebojna ločljivost ostalih lipidnih razredov ni zadovoljiva. Ločeni razredi PL od drugih lipidnih razredov. PL med seboj niso ločeni in ostanejo na bazni liniji. Ostali lipidni razredi so med seboj zadovoljivo ločeni. Slabo ločeni razredi PL od drugih lipidnih razredov. PL med seboj niso ločeni in ostanejo na bazni liniji. MAG ostane na bazni liniji. Ločeni razredi PL od drugih lipidnih razredov. PL med seboj niso ločeni in ostanejo na bazni liniji. MAG ostane na bazni liniji. Ostali lipidni razredi so med seboj zadovoljivo ločeni. Najbolje ločeni med seboj so HST, FFA in FA. Samo pri uporabi razvijalne raztopine 1 so se PL med seboj ločili. Razvijalne raztopine 2, 3 in 4 ne ločijo posameznih PL, ki ostanejo na bazni liniji. Razvijalni raztopini 2 in 3 najmanj zadovoljivo ločita preostale lipidne razrede. Za nadaljnje delo sem uporabljala razvijalni raztopini 1 in 4. B) Uporaba dvodimenzionalnega razvijanja za ločevanje lipidov in identifikacijo lipidnega ekstrakta Ločevanje in identifikacijo spojin izboljšamo z dvodimenzionalno kromatografijo, kjer ploščo najprej razvijamo v raztopini v eni smeri, posušimo in jo nato razvijamo še v drugi razvijalni raztopini, potem ko smo ploščo zasukali za 90 º. Topilo sem pustila potovati do označene razdalje (70 mm) (enostopenjsko dvodimenzionalno razvijanje; 2D). Postopku sem zaradi boljše identifikacije dodala še razvijanje v tretjo smer. Na ploščo sem nanesla tako posamezne lipidne standarde kot njihove mešanice in jih razvijala v obeh raztopinah. V vogalno izhodišče 1. in 4. kvadranta sem točkovno nanesla standardno mešanico lipidov (PE, PC, PS, SM, HST, FFA, SE, MAG, FA in HC). Namesto testne mešanice lipidov lahko nanesemo lipidni ekstrakt realnega vzorca. V 2. in 3. kvadrant sem na črto nanesla standardne raztopine posameznih lipidov Ploščo sem najprej razvijala v raztopini heksan-dietileter (65:35, v/v) v smeri a) do označene višine. Nato sem ploščo posušila ter jo zasukano za 90 º razvijala ponovno v raztopini heksan-dietileter (65:35, v/v) v smeri b). Ploščo sem ponovno posušila in jo razvijala v raztopini kloroform-metanol-voda (65:25:4, v/v/v) v smeri c). Ploščo sem posušila ter potopila v reagent fosfor molibdenove kisline za obarvanje. Nato sem ploščo sušila 30 minut pri 150 ºC. Določevanje lipidov v ekstraktu je mogoče, če med seboj primerjamo lise v kvadrantih (1. in 2., 4. in 3. ter posredno 1. in 4.). Dokaz enakomernih pogojev pri kromatografiji je diagonala v 1. kvadrantu. 62
81 E k s p e r i m e n t a l n i d e l 2. kvadrant 3. kvadrant 1. kvadrant 4. kvadrant Slika 3 32: TLC-2D kromatogram ločevanja standardnih raztopin lipidov. Plošča je najprej razvita v smeri a) z raztopino heksan-dietileter (65:35, v/v), nato v smeri b) z raztopino heksan-dietileter (65:35, v/v) in nato v smeri c) z raztopino kloroformmetanol-voda (65:25:4, v/v/v). C) TLC analiza frakcij po ločevanju lipidnega ekstrakta s SPE-Si Vzorec 1 (VZ1) in vzorec 2 (VZ2) rdečih krvnih celic sem pripravila po postopku ekstrakcije (3.2.3). Vzporedno sem po enakem postopku pripravila še vzorec, ki ni vseboval rdečih krvnih celic (slepi vzorec). Po ekstrakciji celokupnih lipidov sem izvedla ločevanje nepolarnih lipidov in polarnih fosfolipidov na SPE-Si kolonah. Pri tem sem dobila eluat I ter eluat II (fosfolipidi). Proste maščobne kisline (FFA), ki bi lahko vplivale na določevanje sestave maščobnih kislin, če bi se eluirale skupaj s fosfolipidi, v eluatu II. niso bile prisotne. Prav tako nisem opazila motenj iz sistema (slepi vzorec I in slepi vzorec II). 63
82 E k s p e r i m e n t a l n i d e l Slika 3 33: TLC kromatogram standardnih raztopin lipidov v primerjavi s spojinami, ki jih dobim po ločevanju s SPE-Si. Ločitev prostih maščobnih kislin na SPE-Si v eluatu I in II sem potrdila še s plinsko kromatografijo. Za preskušanje sem uporabila standardno raztopino FFA (palmitinska kislina; C16:0). Iz standardne raztopine palmitinske kisline koncentracije 1 mg ml -1 v kloroformu sem odvzela 50 μl in dodala še 450 μl kloroforma. Sledilo je ločevanje na SPE-Si. Eluat I sem skoncentrirala do suhega. Dodala sem 500 μl metanola in vzorec metilirala. Eluat II, ki je že v metanolu, sem samo metilirala. S plinsko kromatografijo sem ugotavljala prisotnost metilnega estra palmitinske kisline v eluatu I in v eluatu II, kjer estra palmitinske kisline ne bi smelo biti (Slika 3-34). Slika 3 34: GC-FID kromatogram eluata I (prisoten metilni ester palmitinske kisline) a) in eluata II (metil ester palmitinske kisline ni prisoten) b). V eluatu II po metiliranju nisem določila metilnega estra palmitinske kisline nad mejo zaznave, kar pomeni, da bodo vse maščobne kisline, določene v eluatu II, izključno iz membranskih fosfolipidov rdečih krvnih celic. 64
83 E k s p e r i m e n t a l n i d e l D) TLC analiza frakcij po ločevanju ekstrakta eritrocitov s SPE-Si Ekstrahirane celokupne lipide rdečih krvnih celic sem ločevala s SPE-Si, da bi izolirala fosfolipide. Po ločevanju sem analizirala eluat I ter eluat II (Preglednica 3 1). Na sliki 3-35 je TLC kromatogram surovega vzorca, na Sliki 3 36 je TLC kromatogram eluata I, na Sliki 3 37 je TLC kromatogram fosfolipidov. Vzorec je nanešen točkovno v desni spodnji vogal z oznako VZ. Ploščo sem razvila najprej v smeri a) v raztopini heksan-dietileter (65:35, v/v) in nato v smeri b) v raztopini kloroform-metanol-voda (65:25:4, v/v/v). Slika 3 35: TLC-2D kromatogram (vzorec: surov lipidni ekstrakt eritrocitov). Slika 3 36: TLC-2D kromatogram (vzorec: eluat I). V eluatu ni fosfolipidov (PL). Slika 3 37: TLC-2D kromatogram (vzorec: eluat II). V eluatu so fosfolipidi (PL). 65
84 R e z u l t a t i i n d i s k u s i j a 4 REZULTATI IN DISKUSIJA 4.1 Opis vzorcev V študijo sem vključila 342 donorjev krvi, ki so imeli različne bolezni, in kontrolno skupino, v kateri donorji niso oboleli za nobeno od naštetih bolezni (Preglednica 4-1). Izbira bolnikov je bila naključna in neodvisna od njihovih prehranjevalnih navad ali dodatnega vnosa lipidov v prehrano. Vzorci eritrocitov so tako pripadali eni kontrolni skupini in šestim skupinam bolnikov z različnimi boleznimi. Preglednica 4 1: Lastnosti in oznake vzorcev krvi. Število vzorcev Starost (leta ± s) Spol (ženski, %) Bolezen in oznaka vzorca Oznaka ± brez bolezni (kontrolni): KON ± 9 71 vnetna črevesna bolezen I: KVČB-I ± 3 43 astma: AST ± miomi na maternici: GIN ± brez miomov na maternici: GIN(KON) ± vnetna črevesna bolezen II: KVČB-II ± črevesni polipi: (POL) 6 s: standardni odmik. Bolniki s kronično vnetno črevesno boleznijo vrste I (KVČB-I - skupina z oznako 1) predstavljajo skupino bolnikov s Crohnovo boleznijo, ki se ne odzivajo na standardno zdravljenje s kortikosteroidi in pri katerih se lahko razvije še hujša oblika bolezni. Bolniki s kronično vnetno črevesno boleznijo vrste II (KVČB-II - skupina z oznako 5) predstavljajo vse ostale bolnike z različnimi črevesnimi boleznimi. Vzorce 342 donorjev sem opisala s sestavo 28 maščobnih kislin, dveh dimetil acetalov, šestih skupinskih parametrov (S: vsota nasičenih maščobnih kislin, M: vsota mononenasičenih maščobnih kislin, P: vsota polinenasičenih maščobnih kislin, T: vsota trans maščobnih kislin, n3: vsota omega-3 polinenasičenih maščobnih kislin in n6: vsota omega-6 polinenasičenih maščobnih kislin) in s tremi razmerji skupinskih parametrov (M/S, M/P in n3/n6) (Preglednica 4-2). Kromatogram metilnih estrov maščobnih kislin (FAME) in dimetil acetalov (DMA) fosfolipidov rdečih krvnih celic je prikazan na Sliki
85 R e z u l t a t i i n d i s k u s i j a Preglednica 4 2: Seznam maščobnih kislin in dimetil acetalov določenih v fosfolipidih membran rdečih krvnih celic. Maščobne kisline Trivialno ime Oznaka Nasičene (SFA) miristinska 14:0 pentadekanojska 15:0 palmitinska 16:0 margarinska 17:0 stearinska 18:0 arašidinska 20:0 behenska lignocerinska 22:0 24:0 Mononenasičene (MUFA) n7 16:1 (9c) palmitoleinska 16:1n7 18:1 (11c) vakcenska 18:1n7 n9 18:1 (9c) oleinska 18:1n9 20:1 (11c) eikozenojska 20:1n9 22:1 (13c) eruka 22:1n9 24:1 (15c) nervonska 24:1n9 Polinenasičene (PUFA) n6 18:2 (9,12)c linolna 18:2n6 18:3 (6,9,12)c γ-linolenska (GLA) 18:3n6 20:2 (11,14)c eikozadienojska 20:2n6 20:3 (8,11,14)c dihomo gama-linolenska (DGLA) 20:3n6 20:4 (5,8,11,14)c arahidonska (AA) 20:4n6 22:4 (7,10,13,16)c adrenska 22:4n6 22:5 (4,7,10,13,16)c dokozapentaenojska 22:5n6 n3 18:3 (9,12,15)c α-linolenska (ALA) 18:3n3 18:4 (6, 9, 12, 15)c stearidonska (STD) 18:4n3 20:5 (5,8,11,14,17)c eikozapentaenojska (EPA) 20:5n3 22:5 (7,10,13,16,19)c dokozapentaenojska (DPA) 22:5n3 22:6 (4,7,10,13,16,19)c Trans maščobne kisline (TFA) 18 :1 (6+9+11)t 18 :3 (9t, 12c, 15t) Dimetil acetali (DMA) Maščobne kisline Vsota nasičenih (SFA) Vsota mononenasičenih (MUFA) Vsota polinenasičenih (PUFA) Vsota trans (TFA) Vsota n-3 PUFA Vsota n-6 PUFA dokozaheksaenojska (DHA) 22:6n3 heksadekanal dimetil acetal oktadekanal dimetil acetal 16:0 DMA 18:0 DMA Okrajšava S M P T n3 n6 67
86 R e z u l t a t i i n d i s k u s i j a Slika 4 1: GC-FID kromatogram FAME in DMA fosfolipidov rdečih krvnih celic. Identifikacija kromatografskih vrhov: (1) 14:0, (2) 15:0, (3) 16:0, (4) 16:0 DMA, (5) 16:1n7, (6) 17:0, (7) 18:0, (8) 18:0 DMA, (9) sum18:1 trans, (10) 18:1n9, (11) 18:1n7, (12) 18:2n6, (13) 20:0, (14) 18:3(9t, 12c, 15t), (15) 18:3n6 GLA, (16) 20:1n9, (17) 18:3n3 ALA, (18) 18:4n3 STD, (19) 20:2n6, (20) 22:0, (21) 20:3n6 DGLA, (22) 22:1n9, (23) 20:4n6 AA, (24) 20:5n3 EPA, (25) 24:0, (26) 24:1n9, (27) 22:4n6, (28) 22:5n6, (29) 22:5n3 DPA, (30) 22:6n3 DHA. 68
87 R e z u l t a t i i n d i s k u s i j a 4.2 Statistična analiza podatkov Metoda glavnih osi (PCA) Da bi poiskala medsebojne korelacije vseh 342 vzorcev, sem uporabila multivariantno metodo - metodo glavnih osi (PCA). To je tehnika zmanjševanja števila podatkov, ampak le, če so ti v korelaciji. Pri tej metodi gre za linearno transformacijo večdimenzionalnega prostora, ki pomaga preslikati lego objektov iz večdimenzionalnega v dvodimenzionalni prostor. Pri preslikavi izberemo tisti dve koordinati, pri katerih bo nova preslikava prikazala kar največ originalne informacije sistema. Najprej poiščemo tisto smer ali prvo glavno os, okoli katere je zbrana največja varianca, ki je merilo celotne, skupne informacije sistema. Pri tem ne gre za originalno spremenljivko, ampak za linearno kombinacijo vseh prejšnjih osi. Naslednja os je pravokotna na osnovno, ker mora biti od prejšnje linearno neodvisna. V veliki večini kemijskih problemov so spremenljivke, s katerimi opisujemo objekte, med seboj odvisne, zato lahko že prvi dve glavni osi vsebujeta več kot 75 % informacije sistema (Zupan, 2009). Obe prvi osi opisujeta 96,4 % informacije sistema. Podatke sem obdelala z metodo centriranja (»column - mean centering«). Pri tem nove spremenljivke dobimo tako, da od vrednosti posamezne spremenljivke vsakega od 342 elementov odštejemo povprečno vrednost vsake spremenljivke. 342 vzorcev eritrocitov sem opisala z 39 spremenljivkami in izvedla PCA z matriko, sestavljeno iz 342 x 39 elementov. Slika 4-2 prikazuje rezultat PC1 vs. PC2. Slika 4 2: Rezultat 342 vzorcev in 39 spremenljivk v PC1 PC2 koordinatnem sistemu. Iz Slike 4-2 je razvidna delitev na tri večje skupine. Spodnja skupina vsebuje vzorce nekaj žensk iz skupin z miomi in brez miomov na maternici (GIN(3) in GIN(KON)(4)). 69
88 R e z u l t a t i i n d i s k u s i j a Ta ločena skupina predstavlja 16 od skupno 67 vzorcev obeh skupin in je ne morem povezati z nobeno izbrano boleznijo v študiji. Značilnost te skupine je visoka vsebnost linolne (18:2n6) kisline (Slika 4-7) in nizka vsebnost stearinske (18:0) kisline, arahidonske (20:4n6) kisline (AA) ter adrenske (22:4n6) kisline (Slika 4-14). V zgornjem delu slike sta razvidni dve podskupini (v obliki osmice - ). Skupini bolnikov KVČB-I(1) in AST(2) sta v levem delu grupe, medtem ko sta skupini bolnikov KVČB-II(5) in POL(6) na desnem delu grupe. Večina kontrolnih vzorcev je razporejenih v levem delu grupe. Za oceno vpliva originalnih spremenljivk na PC osi in posledično na porazdelitev bolnikov v skupine sem naredila še projekcijo vsebnosti spremenljivk (»loading plot«) (Slika 4-3). S to metodo lahko posredujemo informacijo, koliko osnovne komponente spremenljivke, vsebuje glavna os. Če za informacijo, ki jo iščemo, nismo izbrali pravih spremenljivk, ali jih nismo primerno pretvorili, potem ne bomo dobili želene informacije. Ko dosežemo ustrezno preslikavo v dvodimenzionalni prostor (ravnina PC1-PC2), lahko začnemo z analizo faktorjev vsebnosti (»loadings«) na obeh glavnih oseh, ki sta dali iskano grupiranje (Zupan, 2009). Čim bolj so spremenljivke oddaljene od sredine koordinatnega sistema, tem večji vpliv imajo na glavni osi. Iz Slike 4 3 je razvidno, da prvo os PC1 najbolje opisujejo spremenljivke 31 (S), 33 (P) in 38 (omega-6). S (vsota nasičenih maščobnih kislin) kaže na visoke vsebnosti v vzorcih (KVČB-II(5) in POL(6)) v zgornjem desnem delu grupe), medtem ko P (vsota polinenasičenih maščobnih kislin) in omega-6 (vsota omega-6 maščobnih kislin) kažeta na višje vsebnosti teh kislin pri vzorcih (KVČB-I(1) in AST(2)) v zgornjem levem delu grupe. Druga os PC2 je najbolje opisana s spremenljivkami 7 (stearinska (18:0) kislina), 23 (arahidonska (20:4n6) kislina (AA)), 12 (linolna (18:2n6) kislina) in 3 (palmitinska (16:0) kislina). Vzorci podrazredov GIN(3) in GIN(KON)(4) imajo visoke vsebnosti linolne (18:2n6) kisline in palmitinske (16:0) kisline ter nižje vsebnosti stearinske (18:0) kisline in arahidonske (20:4n6) kisline (AA)). 70
89 R e z u l t a t i i n d i s k u s i j a Slika 4 3: Faktorji vsebnosti (»loadings«) 342 vzorcev in 39 spremenljivk v PC1 PC2 koordinatnem sistemu Ponovljivost metode Ker je bila količina eritrocitov posameznega bolnika omejena, sem ponovljivost analizne metode preskušala tako, da sem zaporedoma analizirala šest vzorcev eritrocitov istega bolnika pri enakih eksperimentalnih pogojih. Relativni standardni odmik je bil za maščobne kisline v mejah od 0,8 % do 9,7 % pri njihovi vsebnosti od 0,1 % do 24 % masnega deleža. Za vsebnosti dimetil acetalov 1,1 % masnega deleža in 2,0 % masnega deleža je bil relativni standardni odmik 25 % in 28 %. 4.3 Testi signifikantnosti Parametrični testi Za primerjanje rezultatov spremenljivk sem uporabila dve vrsti parametričnih testov: analizo variance (ANOVA) in t-test, pri čemer sem privzela verjetnostno mejo 5 %, da je razlika med povprečji meritev posledica naključne napake (verjetnost, da bi nastala razlika med povprečji zaradi naključne napake, je manjša od 5 %). V teh primerih lahko rečem, da je razlika signifikantna na stopnji P = 0,05 (Zupan, 2009), (Miller, 2005), (Massart, 1997). Za ANOVO in parni t-test sem najprej uporabila rezultate 23 vzorcev skupine KVČB- II(5), ki predstavljajo bolnike s črevesnimi boleznimi vrste II (Preglednica 4-1). Podatki so bili pridobljeni s ponovitvami analiz istih vzorcev eritrocitov, opravljenih z različnimi analitiki v različnem časovnem obdobju. 71
90 R e z u l t a t i i n d i s k u s i j a Z ANOVO sem primerjala varianci vseh dvojic nizov rezultatov in preverila, ali obstaja med njimi signifikantna razlika v natančnosti analitskega postopka. Uporabila sem F-test ali test primerjave razpršenosti glede na vse spremenljivke pri 23 vzorcih razreda KVČB-II(5). F-test je pokazal, da med obema nizoma rezultatov ne obstajajo signifikantne razlike natančnosti metode določanja za 28 spremenljivk od 30. Razlika je bila signifikantna v 95 % intervalu zaupanja (P=0,05) le za dve spremenljivki (maščobni kislini 14:0 in 20:0), katerih vsebnost je bila manjša od 1 %, kar je blizu meje določljivosti uporabljene metode. Število spremenljivk (39) sem v Preglednici 4-2 z rezultati označila z naslednjimi okrajšavami: 140 (14:0 miristinska kislina, 150 (15:0 pentadekanojska), 160 (16:0 palmitinska), 160DMA (16:0 DMA heksadekanal dimetil acetal), 161 (16:1 palmitoleinska), 170 (17:0 margarinska), 180 (18:0 stearinska), 180DMA (18:0 DMA oktadekanal dimetil acetal), sum181t (vsota 18:1 trans ), 1819c (18:1n9 oleinska), 18111c (18:1n7 vakcenska), 182 (18:2n6 linolna), 200 (20:0 arašidinska), 183t (18:3 9t, 12c, 15t), 183GLA (18:3n6 γ-linolenska), 20111c (20:1n9 eikozenojska), 183ALA (18:3n3 α- linolenska), 184 (18:4n3 stearidonska), 202 (20:2n6 eikozadienojska), 220 (22:0 behenska), 203DGLA (20:3n6 dihomo γ-linolenska), 221 (22:1n9 eruka), 204 (20:4n6 arahidonska), 205EPA (20:5n3 eikozapentaenojska), 240 (24:0 lignocerinska), 241 (24:1 nervonska), 224 (22:4n6 adrenska), 225 (22:5n6 dokozapentaenojska), 225DPA (22:5n3 dokozapentaenojska), 226DHA (22:6n3 dokozaheksaenojska), S (vsota nasičenih), M (vsota mononenasičenih), T (vsota trans), M/S (razmerje vsot mononenasičenih in nasičenih), M/P (razmerje vsot mononenasičenih in vsoto polinenasičenih), n3 (vsota omega-3), n6 (vsota omega-6), n3/n6 (razmerje vsot omega-3 in omega-6) maščobnih kislin. Vsebnosti posameznih spremenljivk sem zapisala v stolpcih pod pripadajočimi okrajšavami spojin. Rezultati so zapisani v treh vrsticah glede na spremenljivke v glavi preglednic k vsakemu zaporednemu vzorcu. Vzorci si zaporedoma sledijo glede na analitika in glede na zaporedno številko vzorca (od 180 do 202) in so označeni po sistemu X-Y, kjer X pomeni oznako analitika, Y pa zaporedno številko vzorca (npr pomeni zaporedno številko vzorca vzorec ( ki pripada skupini bolnikov z oznako KVČB-II(5)) in analitika 2. V Preglednici 4-3 so podane sestave maščobnih kislin fosfolipidov 46 vzorcev rdečih krvnih celic. 72
91 R e z u l t a t i i n d i s k u s i j a Preglednica 4 3:. Sestava maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) 39 spremenljivk pri 23 bolnikih KVČB(5) z oznakami od zaporedne številke 180 do 202. Števka 1 pomeni analitika 1 (opravil analizo 23 vzorcev z zaporedno številko od 180 do 202), števka 2 pa analitika 2 (opravil analizo 23 vzorcev z zaporedno številko od 180 do 202) DMA DMA sum181t 1819c 18111c t 183GLA 20111c 183ALA DGLA EPA DPA 226DHA S M P T M/S M/P n3 n6 n3/n ,60 0,33 34,24 1,81 0,40 0,68 24,21 2,91 0,83 21,77 1,73 8,21 0,14 0,05 0,00 0,27 0,10 0,34 0,39 0,10 0,56 0,00 2,71 0,33 0,22 0,35 0,48 0,00 0,22 0,22 60,52 25,87 13,62 0,88 0,43 1,90 1,21 12,35 0, ,34 0,34 27,72 2,25 0,28 0,68 26,09 3,78 0,89 20,44 1,59 9,31 0,20 0,17 0,00 0,49 0,16 0,21 0,46 0,18 1,36 0,10 5,35 0,40 0,25 0,21 1,38 0,22 0,33 0,39 55,79 24,46 19,75 1,06 0,44 1,24 1,50 18,08 0, ,44 0,31 33,71 1,98 0,38 0,65 25,08 3,49 0,79 22,52 1,48 7,60 0,17 0,06 0,00 0,32 0,14 0,54 0,40 0,13 0,51 0,05 2,54 0,26 0,27 0,37 0,56 0,07 0,21 0,16 60,76 26,19 13,05 0,85 0,43 2,01 1,31 11,69 0, ,41 0,39 37,03 1,91 0,59 0,68 24,58 2,69 1,00 21,02 2,22 5,74 0,13 0,00 0,00 0,45 0,13 0,85 0,25 0,11 0,35 0,00 1,99 0,29 0,27 0,33 0,47 0,11 0,10 0,17 63,59 25,97 10,44 1,00 0,41 2,49 1,54 8,90 0, ,39 0,35 30,64 2,30 0,28 0,67 24,95 3,66 0,75 21,07 1,52 7,75 0,19 0,11 0,00 0,44 0,11 0,55 0,41 0,15 0,69 0,07 5,57 0,09 0,22 0,31 1,10 0,15 0,46 0,69 57,55 24,79 17,66 0,86 0,43 1,40 1,88 15,67 0, ,35 0,24 28,58 2,33 0,36 0,52 20,44 4,28 0,62 17,64 1,56 11,89 0,15 0,09 0,00 0,33 0,13 0,24 0,39 0,12 1,37 0,06 9,43 0,15 0,16 0,24 2,19 0,32 0,77 1,30 50,56 21,17 28,27 0,71 0,42 0,75 2,59 25,59 0, ,32 0,24 28,05 1,81 0,66 0,47 21,05 2,69 0,61 18,87 1,91 9,82 0,14 0,09 0,00 0,30 0,18 0,19 0,32 0,10 1,01 0,05 9,37 0,19 0,13 0,18 2,20 0,28 0,88 2,09 50,49 22,88 26,63 0,70 0,45 0,86 3,53 23,01 0, ,43 0,26 28,37 2,13 0,41 0,56 24,19 3,85 0,71 19,92 1,27 8,33 0,15 0,10 0,06 0,29 0,10 0,31 0,28 0,11 0,99 0,06 8,56 0,13 0,17 0,24 1,83 0,21 0,57 1,01 54,26 23,27 22,48 0,81 0,43 1,04 2,12 20,26 0, ,65 0,45 35,55 2,01 0,47 0,73 22,67 2,92 1,04 21,57 1,69 7,53 0,17 0,07 0,00 0,31 0,10 0,75 0,28 0,11 0,88 0,05 2,61 0,08 0,23 0,34 0,49 0,10 0,26 0,37 60,55 25,95 13,50 1,11 0,43 1,92 1,56 11,88 0, ,42 0,19 30,74 2,06 0,59 0,50 22,27 3,83 0,51 23,53 1,48 6,29 0,15 0,14 0,00 0,46 0,15 0,54 0,27 0,11 0,69 0,07 7,19 0,13 0,12 0,26 1,53 0,21 0,47 0,78 54,49 27,11 18,39 0,65 0,50 1,47 2,08 16,18 0, ,35 0,34 37,88 1,29 0,40 0,72 23,71 2,12 0,89 22,43 1,65 4,87 0,15 0,00 0,00 0,41 0,14 0,83 0,25 0,14 0,28 0,00 2,18 0,77 0,15 0,32 0,43 0,00 0,10 0,28 63,43 26,44 10,13 0,89 0,42 2,61 2,11 8,02 0,26 73
92 R e z u l t a t i i n d i s k u s i j a DMA DMA sum181t 1819c 18111c t 183GLA 20111c 183ALA DGLA EPA DPA 226DHA S M P T M/S M/P n3 n6 n3/n ,39 0,34 29,23 1,48 0,32 0,66 22,23 2,72 1,07 21,95 1,49 10,44 0,23 0,00 0,00 0,34 0,23 0,24 0,33 0,17 1,34 0,05 4,79 0,73 0,18 0,16 1,61 0,00 0,51 0,61 53,45 25,73 20,82 1,07 0,48 1,24 2,32 18,50 0, ,34 0,22 22,88 2,56 0,23 0,44 18,57 4,63 0,61 15,76 1,19 12,55 0,18 0,10 0,05 0,26 0,23 0,00 0,38 0,14 1,44 0,05 14,62 0,53 0,12 0,09 3,14 0,45 1,49 3,54 42,89 18,59 38,52 0,71 0,43 0,48 5,79 32,63 0, ,40 0,22 29,16 2,19 0,64 0,46 20,27 3,43 0,80 18,33 2,19 9,77 0,15 0,08 0,00 0,39 0,16 0,20 0,40 0,12 1,78 0,06 8,01 0,31 0,11 0,06 1,86 0,23 1,03 2,37 50,89 22,90 26,21 0,88 0,45 0,87 4,08 22,05 0, ,40 0,31 27,94 2,26 0,41 0,56 20,82 3,60 0,57 19,12 1,46 10,05 0,14 0,07 0,08 0,29 0,24 0,15 0,29 0,12 1,38 0,10 9,03 0,14 0,12 0,15 2,94 0,35 1,24 1,17 50,40 22,48 27,12 0,64 0,45 0,83 2,93 24,12 0, ,42 0,37 27,56 1,95 0,44 0,65 22,86 2,72 1,02 20,82 1,57 9,05 0,19 0,00 0,00 0,38 0,27 0,22 0,28 0,16 1,09 0,09 7,23 0,18 0,17 0,14 2,57 0,31 0,69 0,80 52,37 24,93 22,69 1,02 0,48 1,10 2,16 20,54 0, ,40 0,33 28,86 1,92 0,42 0,62 25,61 3,78 0,78 20,48 1,46 7,54 0,14 0,00 0,00 0,72 0,00 0,51 0,20 0,18 1,12 0,00 6,44 0,59 0,23 0,17 1,38 0,25 0,39 0,85 56,36 24,37 19,27 0,78 0,43 1,26 2,33 16,94 0, ,39 0,28 27,81 2,22 0,37 0,58 24,36 4,02 0,72 18,42 1,39 12,05 0,21 0,12 0,00 0,36 0,26 0,18 0,35 0,21 1,09 0,00 6,65 0,13 0,21 0,20 1,84 0,13 0,55 0,71 54,05 21,89 24,06 0,84 0,40 0,91 1,84 22,11 0, ,46 0,33 30,26 2,70 0,38 0,60 20,85 4,33 0,79 14,36 1,24 11,00 0,18 0,07 0,06 0,22 0,26 0,09 0,33 0,15 1,51 0,04 13,52 0,74 0,10 0,11 3,29 0,40 2,15 2,92 45,93 17,72 36,35 0,86 0,39 0,49 6,16 30,11 0, ,42 0,30 26,23 2,24 0,33 0,60 22,78 3,58 0,66 17,27 1,33 10,35 0,15 0,06 0,08 0,37 0,29 0,13 0,35 0,14 1,82 0,00 9,94 0,17 0,13 0,11 3,16 0,36 0,92 1,19 50,74 20,45 28,81 0,72 0,40 0,71 2,70 26,06 0, ,40 0,20 22,37 2,63 0,38 0,40 20,67 4,02 0,54 16,29 1,75 11,85 0,17 0,07 0,07 0,33 0,19 0,10 0,37 0,13 1,56 0,05 14,06 0,23 0,08 0,05 3,58 0,51 1,39 1,89 44,43 19,71 35,87 0,61 0,44 0,55 3,80 32,00 0, ,41 0,26 27,89 2,12 0,61 0,51 18,50 3,25 1,12 18,14 1,63 11,05 0,11 0,00 0,00 0,32 0,17 0,00 0,31 0,08 1,40 0,00 11,03 0,22 0,13 0,00 2,55 0,36 1,04 1,57 47,89 22,41 29,71 1,12 0,47 0,75 3,00 26,70 0, ,29 0,18 27,25 2,76 0,54 0,48 23,32 4,85 0,44 17,52 1,66 10,92 0,18 0,11 0,00 0,46 0,23 0,17 0,39 0,16 1,44 0,06 8,73 0,15 0,16 0,22 2,63 0,28 0,82 0,93 52,01 21,18 26,81 0,55 0,41 0,79 2,29 24,40 0,09 74
93 R e z u l t a t i i n d i s k u s i j a DMA DMA sum181t 1819c 18111c t 183GLA 20111c 183ALA DGLA EPA DPA 226DHA S M P T M/S M/P n3 n6 n3/n ,70 0,40 32,66 1,69 0,34 0,81 27,16 2,92 0,91 20,50 1,61 6,92 0,19 0,06 0,00 0,30 0,12 0,34 0,40 0,12 0,54 0,00 2,70 1,00 0,31 0,37 0,52 0,00 0,20 0,24 62,33 24,63 13,03 0,97 0,40 1,89 1,89 11,08 0, ,50 0,42 33,47 2,34 0,28 0,73 24,12 4,02 0,88 19,27 1,71 9,55 0,19 0,06 0,00 0,34 0,09 0,37 0,34 0,11 1,04 0,06 3,28 0,62 0,23 0,34 0,91 0,09 0,19 0,23 59,77 23,45 16,78 0,95 0,39 1,40 1,51 15,21 0, ,49 0,30 34,25 1,88 0,39 0,69 25,13 3,31 0,71 20,97 1,41 7,47 0,18 0,08 0,00 0,33 0,15 0,63 0,31 0,12 0,42 0,00 2,36 0,45 0,20 0,36 0,52 0,00 0,17 1,67 61,35 24,42 14,23 0,80 0,40 1,72 3,07 11,08 0, ,60 0,41 38,54 1,96 0,64 0,77 23,74 2,73 0,92 19,82 2,14 5,64 0,16 0,00 0,00 0,35 0,00 0,84 0,27 0,13 0,31 0,08 1,86 1,14 0,15 0,38 0,44 0,00 0,14 0,17 64,51 24,68 10,81 0,92 0,38 2,28 2,29 8,52 0, ,43 0,32 31,86 2,25 0,30 0,70 23,30 3,62 0,70 20,79 1,56 8,59 0,19 0,13 0,00 0,44 0,14 0,49 0,42 0,14 0,67 0,06 5,36 0,09 0,17 0,33 1,13 0,15 0,45 0,83 57,11 24,46 18,43 0,83 0,43 1,33 2,00 16,31 0, ,45 0,25 29,80 2,20 0,35 0,54 20,41 3,92 0,62 17,14 1,56 12,18 0,17 0,08 0,07 0,31 0,12 0,26 0,39 0,11 1,27 0,07 8,75 0,15 0,16 0,26 1,98 0,27 0,74 1,21 51,88 20,65 27,47 0,71 0,40 0,75 2,47 24,92 0, ,38 0,30 28,15 0,92 0,66 0,48 18,52 1,22 0,57 18,19 1,83 9,98 0,09 0,04 0,04 0,28 0,11 0,12 0,35 0,09 1,04 0,06 11,00 0,27 0,15 0,22 2,53 0,35 1,06 2,90 48,17 22,05 29,78 0,60 0,46 0,74 4,45 25,29 0, ,46 0,26 29,37 2,34 0,47 0,55 23,24 4,14 0,70 19,35 1,26 8,70 0,17 0,09 0,07 0,28 0,09 0,37 0,22 0,11 1,02 0,06 8,50 0,16 0,18 0,24 1,83 0,22 0,61 1,05 54,33 22,74 22,93 0,79 0,42 0,99 2,28 20,55 0, ,72 0,46 35,87 2,09 0,48 0,73 22,16 2,98 0,94 20,30 1,62 7,96 0,17 0,09 0,00 0,32 0,14 0,68 0,31 0,12 0,89 0,06 2,87 0,09 0,26 0,40 0,51 0,71 0,28 0,41 60,48 24,59 14,93 1,03 0,41 1,65 1,60 13,24 0, ,64 0,29 33,80 1,49 0,56 0,64 20,89 2,69 0,52 23,18 1,54 6,14 0,16 0,10 0,00 0,45 0,14 0,60 0,27 0,13 0,61 0,08 5,89 0,10 0,20 0,30 1,29 0,18 0,36 0,63 56,77 26,92 16,31 0,61 0,47 1,65 1,83 14,38 0, ,57 0,44 37,83 1,37 0,40 0,81 24,07 2,28 0,93 21,02 1,59 4,47 0,20 0,00 0,00 0,41 0,10 1,01 0,19 0,13 0,41 0,00 2,18 1,49 0,21 0,33 0,50 0,00 0,00 0,25 64,26 25,12 10,62 0,93 0,39 2,37 2,86 7,76 0, ,28 0,19 23,52 2,05 0,25 0,40 16,60 3,82 0,68 17,56 1,27 12,59 0,18 0,06 0,06 0,06 0,12 0,08 0,39 0,11 2,10 0,05 13,21 0,18 0,10 0,07 3,94 0,63 1,73 3,23 41,38 20,29 38,33 0,74 0,49 0,53 5,34 32,93 0,16 75
94 R e z u l t a t i i n d i s k u s i j a DMA DMA sum181t 1819c 18111c t 183GLA 20111c 183ALA DGLA EPA DPA 226DHA S M P T M/S M/P n3 n6 n3/n ,50 0,30 26,51 2,23 0,28 0,59 22,57 4,25 0,71 17,72 1,31 12,07 0,21 0,10 0,04 0,31 0,23 0,11 0,37 0,15 1,16 0,04 8,94 0,27 0,17 0,17 2,11 0,25 0,81 1,62 50,99 20,93 28,08 0,82 0,41 0,75 3,04 24,93 0, ,55 0,33 31,50 1,62 0,71 0,62 21,50 2,49 0,85 18,78 2,25 9,62 0,18 0,06 0,00 0,39 0,18 0,25 0,38 0,14 1,50 0,05 5,65 0,21 0,14 0,18 1,42 0,18 0,70 1,30 54,96 23,59 21,45 0,91 0,43 1,10 2,64 18,75 0, ,44 0,30 25,57 2,28 0,47 0,50 17,09 3,83 0,49 17,16 1,30 10,24 0,17 0,08 0,10 0,29 0,17 0,12 0,28 0,11 1,54 0,04 13,75 0,25 0,09 0,06 4,05 0,61 1,96 2,42 44,27 20,16 35,57 0,57 0,46 0,57 4,92 30,56 0, ,62 0,39 29,24 1,92 0,42 0,64 21,59 2,63 0,92 19,74 1,59 9,79 0,19 0,07 0,00 0,37 0,25 0,20 0,27 0,17 1,09 0,08 7,06 0,17 0,16 0,18 2,36 0,28 0,67 1,00 53,00 23,79 23,21 0,98 0,45 1,02 2,29 20,86 0, ,59 0,37 30,23 1,94 0,31 0,75 25,60 3,86 0,72 19,92 1,43 7,57 0,18 0,10 0,00 0,32 0,14 0,58 0,21 0,13 1,02 0,00 6,17 0,09 0,19 0,24 1,33 0,22 0,38 0,90 58,03 23,26 18,71 0,82 0,40 1,24 2,09 16,52 0, ,47 0,32 28,50 2,27 0,32 0,65 24,74 4,18 0,79 18,45 1,39 11,52 0,25 0,10 0,00 0,37 0,26 0,18 0,35 0,25 0,97 0,05 6,11 0,11 0,20 0,26 1,67 0,09 0,49 0,68 55,37 22,11 22,52 0,89 0,40 0,98 1,71 20,70 0, ,81 0,52 29,56 2,41 0,46 0,80 24,77 3,84 0,98 16,69 1,43 10,34 0,21 0,08 0,00 0,25 0,26 0,15 0,30 0,17 1,05 0,00 6,31 0,28 0,20 0,20 1,69 0,15 0,83 0,80 57,04 20,71 22,25 1,06 0,36 0,93 2,32 19,84 0, ,64 0,33 28,74 2,40 0,41 0,64 24,89 3,83 0,61 17,96 1,36 10,05 0,21 0,07 0,05 0,29 0,24 0,21 0,33 0,15 1,46 0,07 6,79 0,13 0,18 0,17 2,32 0,20 0,58 0,59 55,77 21,21 23,02 0,68 0,38 0,92 1,74 21,20 0, ,47 0,24 25,89 2,28 0,58 0,54 23,08 3,50 0,61 17,82 1,91 11,90 0,21 0,07 0,07 0,36 0,16 0,14 0,37 0,14 1,32 0,05 9,00 0,14 0,13 0,18 2,45 0,30 0,78 0,81 50,69 21,79 27,51 0,68 0,43 0,79 2,03 25,41 0, ,63 0,34 30,20 1,99 0,70 0,62 20,80 3,07 1,26 18,79 1,72 10,19 0,15 0,00 0,00 0,34 0,18 0,29 0,28 0,10 1,15 0,00 7,70 0,11 0,11 0,00 1,91 0,22 0,69 0,85 52,94 23,49 23,57 1,26 0,44 1,00 2,12 21,45 0, ,35 0,19 26,94 2,81 0,38 0,44 22,49 5,06 0,44 16,68 1,58 11,41 0,22 0,11 0,00 0,42 0,21 0,10 0,41 0,15 1,60 0,07 9,97 0,21 0,18 0,09 2,90 0,30 0,90 1,01 50,95 19,93 29,11 0,55 0,39 0,68 2,43 26,58 0,09 76
95 R e z u l t a t i i n d i s k u s i j a Primer izračuna primerjave varianc rezultatov obeh analitikov za linolno (18:2n6) kislino je v Preglednici 4 4. Preglednica 4 4: ANOVA F-test za linolno (18:2n6) kislino. Analitik1 Analitik Povprečje S (st.dev): S relat.: Število skupin: 2 Število meritev v j-ti skupini = nj Skupno število meritev = N 46 Vsota v j-ti skupini = SXj Skupna vsota = SX 429 SXj * SXj (SXj * SXj)/nj (j-to povprečje kvadratov) Vsota (SXj * SXj)/nj Vsota SXj * SXj Izvor varianc Vsota kvadratov Prostostna stopnja Povprečje kvadratov Med skupinami Znotraj skupin Skupno alfa = stopnja signifikantnosti 0.05 F-eksperim. (izračunan) F-teor. (tabelaričen) ZAKLJUČEK: Fizrač. < Fteor.: Med skupinama meritev ni signifikantnih razlik. Potem sem s parnim t-testom (test dvojic) ugotavljala, ali se dvojice meritev med seboj signifikantno razlikujejo (test obnovljivosti meritev). Primer izračuna parnega t-testa za linolno (18:2n6) kislino je v Preglednici
96 R e z u l t a t i i n d i s k u s i j a Preglednica 4 5: Parni t-test dveh setov meritev dveh analitikov za linolno (18:2n6) kislino. Analitik1 Analitik2 razlika število meritev 23 povprečje standardni odmik stopnja signifikantnosti 0.05 prost. stopnja 22 t-test (izrač.) t-teor ZAKLJUČEK t-izrač < t-teor: Med načinoma ni signifikantnih razlik. Test ni pokazal signifikantnih razlik za 25 spremenljivk od 30. Razlika je bila signifikantna znotraj 95 % intervala zaupanja (P = 0,05) le za pet spremenljivk (maščobne kisline 14:0, 15:0, 17:0, 20:0 in 24:1n9), katerih vsebnost je bila od 0,2 % do 0,6 %, kar je blizu meje določljivosti uporabljene metode. Na osnovi teh rezultatov sem prišla do zaključka, da je metoda robustna in dosega zadovoljivo ponovljivost meritev. Izvajanje metode pri različnih pogojih (izbira analitika, čas analize) ne vpliva na rezultate analize. Naslednji test, ki sem ga izvedla, je bila analiza variance (ANOVA-test) na vseh 342 vzorcih, ki pripadajo sedmim različnim skupinam, ki so označene z oznakami od 0 do 6 (v tem primeru primerjam med seboj več varianc). Za vseh 30 spremenljivk (razen za eikozadienojsko (20:2n6) kislino) obstaja signifikantna razlika med povprečji merjenih vrednosti za vseh 7 skupin, ki pripadajo različnim bolnikom znotraj 95 % intervala zaupanja, kar pomeni, da se vse skupine bolnikov glede na izbrane merjene spremenljivke med seboj razlikujejo. Primer izračuna primerjave varianc za linolno (18:2n6) kislino pri vseh 7 skupinah je v Preglednici
97 R e z u l t a t i i n d i s k u s i j a Preglednica 4 6: ANOVA F-test za linolno (18:2n6) kislino za vseh sedem skupin. KVČB-I (1) AST (2) GIN (3) GIN(KON) (4) KVČB-II (5) KON (0) POL (6) Povprečje S (st.dev): S relat.: Število skupin: 7 Število meritev v j-ti skupini = nj Skupno število meritev = N 342 Vsota v j-ti skupini = SXj Skupna vsota = SX 3379 SXj * SXj (SXj * SXj)/nj (j-to povprečje kvadratov) Vsota (SXj * SXj)/nj Vsota SXj * SXj Izvor varianc Vsota kvadratov Prostostna stopnja Povprečje kvadratov Med skupinami Znotraj skupin Skupno alfa = stopnja signifikantnosti 0.05 F-eksperim. (izračunan) F-teor. (tabelaričen) ZAKLJUČEK: Fizrač. > Fteor.: Med skupinama meritev so signifikantne razlike. 79
98 R e z u l t a t i i n d i s k u s i j a Z naslednjim t-testom, ki sem ga uporabila, sem primerjala povprečne vrednosti posameznih spremenljivk (S, M, P, T, n-3 PUFA in n-6 PUFA) med dvema skupinama vzorcev (predvsem med posameznimi skupinami in kontrolno skupino). Rezultati so v Preglednici 4-7. Preglednica 4 7: Rezultati t-testa primerjave povprečnih vrednosti različnih skupin vzorcev. Primerjava skupin S M P T n-3 PUFA n-6 PUFA x x - x - - x 4-0 x - x - x x x x x x x 6-0 x x x x x x 1-5 x x x x x x x - x signifikantna razlika pri intervalu zaupanja (P = 0,05) -. ni razlik pri intervalu zaupanja (P = 0,05) Primer izračuna t-testa v primeru skupine 1 (KVČB-I(1)) in kontrolne skupine 5 (KVČB-II(5)) je v Preglednici 4-8. Iz Preglednice 4-7 je razvidno, da se ženske, ki imajo miome (GIN(3)), in tiste, ki jih nimajo (GIN(KON)(4)), razlikujejo glede na vsebnost omega-3 maščobnih kislin. Tudi bolniki z astmo AST(2), ženske brez miomov GIN(KON)(4), bolniki s črevesno boleznijo vrste-ii KVČB-II(5) in bolniki s polipi POL(6) se od kontrolne skupine KON(0) razlikujejo glede na vsebnost omega-3 maščobnih kislin. Glede na vsebnosti omega-6 kislin se razlikuje kontrolna skupina KON(0) od žensk z miomi GIN(3), od bolnikov s črevesnimi boleznimi vrste-ii KVČB-II(5) in bolnikov s polipi POL(6). Obe skupini bolnikov s črevesnimi boleznimi vrste-i KVČB-I(1) in vrste-ii KVČB-II(5) se med seboj razlikujeta glede na vse merjene spremenljivke. 80
99 R e z u l t a t i i n d i s k u s i j a Preglednica 4 8: Primerjava povprečnih vrednosti meritev posamezne spremenljivke (S) med skupinama KVČB-I(1) in KVČB-II(5). KVČB-I (1) KVČB-II (5) F-teor F-izrač F-test ustreza Število meritev: Povprečje: Standardni odmik: Stopnja signifikantnosti Prostostna stopnja (skupno): Standardni odmik (skupno): t-test (izrač.) t-teoret ZAKLJUČEK: t-izrač. > t-teoret.: Med skupinama meritev so signifikantne razlike
100 R e z u l t a t i i n d i s k u s i j a 4.4 Izboljšava ekstrakcije lipidov iz rdečih krvnih celic Za preskušanje ekstrakcije lipidov po metodi postopnega dodajanja ekstrakcijskih topil, ki predstavlja izboljšavo doslej uporabljenih metod, kjer ekstrakcija poteka z dodatkom mešanice topil, sem naključno izbrala deset vzorcev eritrocitov dveh bolnikov z različnima boleznima (glej 3.2.3). Ekstrahirane lipide iz dveh nizov vzorcev petih dvojic sem določila s tehtanjem. Rezultate sem predstavila v Preglednici 4-9. Preglednica 4 9: Primerjava ekstrakcije lipidov po izboljšani metodi in konvencionalni metodi po Folchu. Vzorec 1- A (n=5) m (g) lipidov Vzorec 2- A (n=5) m (g) lipidov Skupna masa lipidov 0,018 Skupna masa lipidov 0,018 Vzorec 1- B (n=5) m (g) lipidov Vzorec 2- B (n=5) m (g) lipidov Skupna masa lipidov 0,012 Skupna masa lipidov 0,009 A) Izboljšana metoda ekstrakcije (ekstrakcijska topila dodajam postopoma) B) Konvencionalna metoda ekstrakcije po Folchu (dodam mešanico ekstrakcijskih topil) Z izboljšano metodo sem dobila več ekstrahiranih lipidov glede na doslej največkrat uporabljeno metodo ekstrakcije lipidov z mešanico topil (Folch, 1957). 4.5 Rezultati analiz vzorcev fosfolipidov rdečih krvnih celic V Preglednici 4-10 so podane sestave maščobnih kislin fosfolipidov 342 vzorcev rdečih krvnih celic (Priloga). Maščobne kisline in dimetil acetali predstavljajo spremenljivke, ki sem jih uporabila v kemometrijski analizi (Miller, 2005), (Massart, 1997). Vsi izračuni in izrisi so bili narejeni s programom»teach/me«in z uporabo»teach/me Data Analysis«1 Medsebojne korelacijske koeficiente vsebnosti maščobnih kislin sem izračunala po Pearsonu (Zupan, 2009). S korelacijo sem opisala linearno zvezo med dvema spremenljivkama. Izračun korelacijskih koeficientov lahko uporabljamo le, ko primerjamo podobne vrste podatkov. Korelacijske vrednosti kateregakoli para dveh spremenljivk se vedno nahajajo v intervalu vrednosti od 1 do 1. Čim večja je absolutna vrednost korelacijskega koeficienta, tem večja je njuna zveza v obeh nizih podatkov ali meritev. Če sta spremenljivki med seboj linearno povsem neodvisni, je korelacija med njima enaka nič. Korelacija spremenljivke same s seboj je enaka ena. Če je korelacija enaka 1 ali 1, potem sta niza linearno odvisna. Korelacija je negativna, če se vrednosti v enem nizu zvišujejo, v drugem pa padajo. (Zupan, 2009). 1 Teach/Me, SDL - Software Development Lohninger; Teach/Me DataLab Springer, Berlin, Developed by H. Lohninger and the Teach/Me people. 82
101 R e z u l t a t i i n d i s k u s i j a Preglednica 4 11: Vrednosti medsebojnih korelacijskih koeficientov 39 spremenljivk maščobnih kislin in njihovih razmerij DMA DMA vsota181 t 181 9c c t 183 GLA c 183 ALA DGLA EPA DPA 226 DHA S M P T M / S M / P n3 n6 n3 /n DMA DMA vsota181 t c c t GLA c ALA DGLA EPA DPA DHA S M P T M / S M / P n n n3 / n
102 R e z u l t a t i i n d i s k u s i j a Iz Preglednice 4 11, Slike 4-4 in Slike 4-5 je razvidna negativna korelacija med nasičenimi maščobnimi kislinami (S) in arahidonsko (20:4n6) kislino (r = - 0,964) ter nasičenimi maščobnimi kislinami (S) in adrensko (22:4n6) kislino (r = - 0,902). Slika 4 4: Razmerje vsebnosti vsote nasičenih maščobnih kislin (S) in arahidonske (20:4n6) kisline (AA) (r = - 0,964). Slika 4 5: Razmerje vsebnosti vsote nasičenih maščobnih kislin (S) in adrenske (22:4n6) kisline (r = - 0,902). 84
103 R e z u l t a t i i n d i s k u s i j a Na Sliki 4-5 in Sliki 4-6 sem opazila izstopajoče vzorce iz skupin z oznakami 3 in 4. ki predstavljajo bolnice z miomi na maternici (GIN(3)) in njihove kontrolne vzorce (GIN(KON)(4)). Že na osnovi teh dveh spremenljivk (adrenske (22:4n6) kisline in palmitinske (16:0) kisline) sta se med seboj ločili različni skupini vzorcev in vsi ostali vzorci. Palmitinska (16:0) kislina ima od vseh nasičenih maščobnih kislin največji negativni korelacijski koeficient glede na arahidonsko (20:4n6) kislino (AA) (- 0,932). Velik negativni korelacijski koeficient ima palmitinska (16:0) kislina tudi glede na adrensko (22:4n6) kislino (- 0,909). Slika 4-6 prikazuje razmerje vsebnosti nasičene maščobne kisline (palmitinska (16:0) kislina) in vsote omega-6 maščobnih kislin. K vsoti omega-6 kislin največ prispevata arahidonska (20:4n6) kislina (AA) in adrenska (22:4n6) kislina. Izstopajoča skupina predstavlja nekaj bolnic z miomi (3) in njihove kontrolne vzorce (4). Slika 4 6: Razmerje vsebnosti palmitinske (16:0) kisline in vsote omega-6 polinenasičenih maščobnih kislin. Teh odstopanj obeh podskupin nisem opazila, ko sem primerjala razmerja med nasičenimi maščobnimi kislinami in vsoto omega-3 maščobnih kislin. Pri pregledu koncentracij linolne (18:2n6) kisline pri vseh 342 vzorcih sem opazila isto izstopajočo skupino bolnic z miomi in njihovo kontrolno skupino brez miomov (skupina z oznakama 3 in 4) (Slika 4-7). Vsebnost linolne (18:2n6) kisline je bila pri teh vzorcih precej nad povprečjem ostalih vzorcev. Iz tega lahko sklepam na prekinjen naravni 85
104 R e z u l t a t i i n d i s k u s i j a proces podaljšanja verig in desaturacije pri biosintezi omega-6 maščobnih kislin iz starševske linolne (18:2n6) kisline. Morda že lahko govorimo o motnji metabolizma. Slika 4 7: Vsebnost linolne (18:2n6) kisline pri 342 donorjih (za sedem skupin bolnikov z oznakami od 1 do 6 in kontrolno skupino z oznako 0). Podobno motnjo so opazili tudi pri bolnikih z diabetesom tipa 1, kjer je bila vsebnost linolne (18:2n6) kisline precej nad vsebnostjo te kisline pri kontrolnih vzorcih. Inzulin aktivira metabolizem maščobnih kislin, zato obstaja verjetnost oviranja metabolizma zaradi pomanjkanja inzulina ter posledično nižje vsebnosti metabolnih dolgoverižnih maščobnih kislin, kot je arahidonska (20:4n6) kislina in adrenska (22:4n6) kislina (Decsi, 2002). Primerljive rezultate so dobili tudi pri bolnikih z diabetesom tipa 2, kjer tudi obstaja povezava med aktivnostjo inzulina in nastajanjem dolgoverižnih omega-6 maščobnih kislin (Rodríguez, 2005). Odstopanje od povprečja vsebnosti linolne (18:2n6) kisline sem opazila še pri bolnikih s črevesnimi polipi (6) (Slika 4-7). Ti bolniki imajo najnižje vsebnosti linolne (18:2n6) kisline. Nekatere študije so pokazale povezavo med sestavo maščobnih kislin in rakom na črevesju. Visoke vsebnosti linolne (18:2n6) kisline, arahidonske (20:4n6) kisline in omega-6 polinenasičenih maščobnih kislin v membranah eritrocitov zmanjšujejo tveganje raka na črevesju, medtem ko kažejo višje vsebnosti palmitinske (16:0) kisline, stearinske (18:0) kisline in oleinske (18:1n9) kisline pozitivno korelacijo nastanka raka na črevesju (Kuriki, 2006), (Kuriki, 2008). Bolnikih s črevesnimi polipi (6) imajo zelo nizke vsebnosti polinenasičenih maščobnih kislin (vsote omega-3 in vsote omega-6) (Slika 4-8, Slika 4-9 in Slika 4-10.). Vsebnosti omega-3 maščobnih kislin so pri vseh 342 vzorcih med 1,0 % in 10,0 %, razen pri bolnikih s polipi (6), kjer so vsebnosti do največ 4,0 %. 86
105 R e z u l t a t i i n d i s k u s i j a Bolniki s črevesnimi polipi (6) imajo razmerja vsebnosti omega-3 in omega-6 maščobnih kislin primerljiva z ostalimi bolniki (Slika 4-11), vendar so vsebnosti polinenasičenih maščobnih kislin (vsota omega-3 in vsota omega-6 kislin) nižje glede na vse ostale bolnike in kontrolno skupino. Polinenasičene maščobne kisline lahko imajo pomembno vlogo pri nastanku polipov na črevesju. Slika 4 8: Vsebnost polinenasičenih kislin (P) pri 342 donorjih (kontrolni vzorci in bolniki). Slika 4 9: Vsebnost omega-3 kislin (n3) pri 342 donorjih (kontrolni vzorci in bolniki). Slika 4 10: Vsebnost omega-6 kislin (n6) pri 342 donorjih (kontrolni vzorci in bolniki). Slika 4 11: Vsebnost razmerij omega-3 in omega-6 kislin (n3 / n6) pri 342 donorjih (kontrolni vzorci in bolniki). 87
106 R e z u l t a t i i n d i s k u s i j a Najpomembnejše maščobne kisline (palmitinska (16:0) kislina, polinenasičene maščobne kisline (P) in linolna (18:2n6) kislina), glede na katere odstopajo nekateri vzorci od ostalih vzorcev, sem prikazala na Sliki Slika 4 12: Vsebnosti maščobnih kislin 342 donorjev glede na najbolj diskriminatorne spremenljivke (palmitinska (16:0) kislina, linolna (18:2n6) kislina in vsota polinenasičenih maščobnih kislin (P)). Večina bolnikov s črevesnimi polipi (skupina z oznako POL(6) ( )) ima visoke vsebnosti palmitinske (16:0) kisline ter nizke vsebnosti polinenasičenih maščobnih kislin (P). Iz Slike 4 12 je razvidna tudi izstopajoča skupina bolnic z miomi (GIN(3) - podskupina ( )) in brez miomov na maternici (GIN(KON)(4) - podskupina ( )). Študija, ki je bila izvedena v Italiji, je pokazala, da imajo ženske z nižjim tveganjem raka na dojkah povišane vsebnosti linolne (18:2n6) kisline. Korelacije med nasičenimi maščobnimi kislinami in tveganjem raka na dojkah ni opaziti (Pala, 2001). Povprečne vsebnosti maščobnih kislin in njihove standardne odmike za vse skupine vzorcev sem vnesla v Preglednico 4-12 ter njihove profile prikazala na Sliki
107 R e z u l t a t i i n d i s k u s i j a Preglednica 4 12: Povprečne vsebnosti sestav maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) za donorje KVČB-I(1), AST(2), GIN(3), GIN(KON)(4), KVČB-II(5), POL(6) in KON(0) kontrolne vzorce. Maščobne kisline KVČB-I(1) (povp ± s) n=60 AST(2) (povp ± s) n=52 GIN(3) (povp ± s) n=53 GIN(KON)(4) (povp ± s) n=14 KVČB-II(5) (povp ± s) n=75 POL(6) (povp ± s) n=18 KON(0) (povp ± s) n=70 SFA 14:0 15:0 16:0 17:0 18:0 20:0 22:0 24:0 S n-7 MUFA 16:1n7 18:1n7 n-9 MUFA 18:1n9 20:1n9 22:1n9 24:1n9 M n-6 PUFA 18:2n6 18:3n6 (GLA) 20:2n6 20:3n6 (DGLA) 20:4n6 (AA) 22:4n6 22:5n6 n6 0,34 ± 0,12 0,24 ± 0,11 22,17 ± 4,90 0,44 ± 0,23 18,97 ± 3,56 0,16 ± 0,04 0,13 ± 0,04 0,13 ± 0,09 42,59 ± 8,31 0,38 ± 0,19 1,37 ± 0,28 16,82 ± 2,73 0,32 ± 0,07 0,05 ± 0,03 0,08 ± 0,09 20,04 ± 3,36 9,81 ± 1,78 0,06 ± 0,05 0,33 ± 0,08 1,74 ± 0,50 15,26 ± 6,49 3,86 ± 1,72 0,61 ± 0,31 31,67 ± 8,93 0,38 ± 0,13 0,24 ± 0,09 22,77 ± 4,18 0,44 ± 0,13 20,68 ± 3,33 0,18 ± 0,03 0,14 ± 0,02 0,15 ± 0,05 44,97 ± 7,44 0,35 ± 0,13 1,31 ± 0,27 16,75 ± 2,64 0,33 ± 0,07 0,06 ± 0,03 0,09 ± 0,05 19,81± 3,03 10,28 ± 1,29 0,05 ± 0,04 0,35 ± 0,06 1,57 ± 0,46 14,20 ± 5,77 3,82 ± 1,51 0,62 ± 0,33 30,89 ± 8,31 0,44 ± 0,14 0,27 ± 0,07 25,77 ± 5,45 0,50 ± 0,12 21,30 ± 4,54 0,16 ± 0,05 0,13 ± 0,06 0,16 ± 0,08 48,74 ± 8,42 0,37 ± 0,13 1,38 ± 0,20 16,57 ± 3,01 0,30 ± 0,09 0,05 ± 0,04 0,10 ± 0,12 18,77 ± 3,39 10,14 ± 4,64 < 0,05 0,34 ± 0,07 1,44 ± 0,55 11,85 ± 6,01 2,75 ± 1,83 0,52 ± 0,37 27,08 ± 9,47 0,56 ± 0,21 0,30 ± 0,09 32,28 ± 8,08 0,53 ± 0,11 16,72 ± 4,10 0,14 ± 0,07 0,14 ± 0,04 0,24 ± 0,11 50,92 ± 7,53 0,62 ± 0,31 1,63 ± 0,25 15,89 ± 2,60 0,25 ± 0,13 < 0,05 0,14 ± 0,08 19,56 ± 3,18 14,94 ± 5,95 < 0,05 0,33 ± 0,12 1,65 ± 0,59 8,13 ± 6,03 1,30 ± 1,69 0,23 ± 0,27 26,60 ± 9,14 0,45 ± 0,15 0,31 ± 0,10 28,06 ± 5,34 0,55 ± 0,14 21,26 ± 2,88 0,16 ± 0,03 0,14 ± 0,04 0,19 ± 0,09 51,12 ± 7,89 0,41 ± 0,14 1,50 ± 0,28 19,31 ± 2,61 0,35 ± 0,08 < 0,05 0,17 ± 0,11 22,95 ± 3,07 9,29 ± 2,17 < 0,05 0,36 ± 0,07 1,22 ± 0,47 9,10 ± 5,06 2,23 ± 1,29 0,33 ± 0,24 22,55 ± 8,54 0,58 ± 0,21 0,33 ± 0,09 31,31 ± 3,30 0,63 ± 0,13 25,24 ± 1,93 0,19 ± 0,03 0,18 ± 0,04 0,30 ± 0,09 58,75 ± 4,85 0,52 ± 0,22 1,70 ± 0,32 20,86 ± 2,10 0,37 ± 0,06 < 0,05 0,22 ± 0,11 24,83 ± 2,51 6,87 ± 1,62 < 0,05 0,37 ± 0,12 0,83 ± 0,40 5,18 ± 3,25 1,12 ± 0,77 0,15 ± 0,14 14,52 ± 6,03 0,40 ± 0,14 0,24 ± 0,09 22,26 ± 4,57 0,44 ± 0,13 20,32 ± 2,96 0,17 ± 0,04 0,13 ± 0,03 0,14 ± 0,08 44,10 ± 7,51 0,39 ± 0,17 1,29 ± 0,25 16,63 ± 2,95 0,35 ± 0,08 0,06 ± 0,03 0,08 ± 0,09 19,66 ± 3,54 9,85 ± 1,60 < 0,05 0,37 ± 0,07 1,49 ± 0,49 15,08 ± 6,02 3,65 ± 1,64 0,55 ± 0,26 31,02 ± 8,78 89
108 R e z u l t a t i i n d i s k u s i j a n-3 PUFA 18:3n3 (ALA) 18:4n3 (STD) 20:5n3 (EPA) 22:5n3 (DPA) 22:6n3 (DHA) n3 P TFA 18 :1 (6+9+11) t 18 :3 (9t,12c,15t) T DMA 16:0 DMA 18:0 DMA M/S M/P n3/n6 s: standardni odmik 0,18 ± 0,09 0,13 ± 0,13 0,45 ± 0,25 1,99 ± 0,98 2,87 ± 1,74 5,62 ± 2,79 37,38 ± 11,32 0,60 ± 0,25 0,09 ± 0,06 0,69 ± 0,23 2,55 ± 0,84 4,11 ± 1,56 0,47 ± 0,04 0,65 ± 0,40 0,17 ± 0,06 0,16 ± 0,04 0,10 ± 0,11 0,29 ± 0,15 1,34 ± 0,70 2,35 ± 1,37 4,24 ± 2,07 35,23 ± 10,20 0,55 ± 0,20 0,10 ± 0,03 0,65 ± 0,20 2,66 ± 0,83 4,56 ± 1,42 0,44 ± 0,04 0,65± 0,34 0,13 ± 0,04 0,17 ± 0,07 0,22 ± 0,24 0,37 ± 0,28 1,25 ± 0,85 2,45 ± 1,72 4,47 ± 2,49 31,54 ± 11,37 0,55 ± 0,21 0,06 ± 0,05 0,61 ± 0,22 2,07 ± 0,79 3,40 ± 1,47 0,39 ± 0,04 0,60 ± 0,45 0,16 ± 0,06 0,13 ± 0,11 0,20 ± 0,26 0,40 ± 0,48 0,77 ± 0,71 1,39 ± 1,25 2,89 ± 1,89 29,52 ± 10,14 0,54 ± 0,16 < 0,05 0,56 ± 0,17 1,11 ± 1,02 1,73 ± 2,17 0,39 ± 0,05 0,84 ± 0,62 0,12 ± 0,07 0,16 ± 0,08 0,21 ± 0,21 0,28 ± 0,20 0,99 ± 0,72 1,67 ± 1,42 3,31 ± 2,16 25,93 ± 10,50 0,75 ± 0,22 0,06 ± 0,05 0,81 ± 0,21 1,80 ± 0,72 3,01 ± 1,24 0,45 ± 0,04 1,10 ± 0,58 0,14 ± 0,05 0,13 ± 0,05 0,43 ± 0,23 0,31 ± 0,19 0,41 ± 0,36 0,58 ± 0,50 1,86 ± 0,71 16,42 ± 6,71 0,78 ± 0,30 0,05 ± 0,05 0,83 ± 0,28 1,81 ± 0,61 3,05 ± 1,05 0,42 ± 0,03 1,75 ± 0,67 0,13 ± 0,03 0,18 ± 0,06 0,11 ± 0,14 0,39 ± 0,20 1,70 ± 0,82 2,76 ± 1,52 5,13 ± 2,33 36,24 ± 10,87 0,55 ± 0,21 0,09 ± 0,06 0,64 ± 0,20 2,31 ± 0,78 3,92 ± 1,45 0,45 ± 0,03 0,67 ± 0,46 0,16 ± 0,04 SFA, nasičene maščobne kisline; MUFA, mononenasičene maščobne kisline; PUFA, polinenasičene maščobne kisline; TFA, trans maščobne kisline; S, vsota nasičenih maščobnih kislin; M, vsota mononenasičenih maščobnih kislin; (n6), vsota n-6 polinenasičenih maščobnih kislin; (n3), vsota n-3 polinenasičenih maščobnih kislin; (P), vsota polinenasičenih maščobnih kislin; (T), vsota trans maščobnih kislin, 16:0 DMA heksadekanal dimetil acetal, 18:0 DMA oktadekanal dimetil acetal 90
109 R e z u l t a t i i n d i s k u s i j a KVČB-I (1) AST (2) GIN(3) GIN(KON) (4) KVČB-II (5) POL(6) KON(0) c DGLA 204 (AA) EPA 225DPA 226DHA S M P n3 n6 M/S M/P n3/n6 ut. % maščobnih kislin c DGLA 204 (AA) EPA 225DPA 226DHA S M P n3 n6 M/S M/P n3/n6 log skala (ut. % maščobnih kislin 0.10 Slika 4 13: Profili maščobnih kislin bolnikov z različnimi boleznimi v primerjavi s kontrolno skupino KON(0) ( ) (izraženi v masnem deležu (%) in logaritmu masnega deleža). 91
110 R e z u l t a t i i n d i s k u s i j a Glede na profile maščobnih kislin najbolj izstopa skupina bolnikov s polipi na črevesju (POL(6)). Skupina ima najvišjo vsebnost nasičenih maščobnih kislin, najnižje vsebnosti omega-3 in omega-6 maščobnih kislin ter najnižjo vsebnost linolne (18:2n6) kisline. Posledično so nizke vsebnosti dihomo γ-linolenske (20:3n6) kisline (DGLA), arahidonske (20:4n6) kisline (AA) in adrenske (22:4n6) kisline. Od omega-3 maščobnih kislin ima skupina bolnikov s polipi na črevesju (POL(6)) najnižje vsebnosti dokozapentaenojske (22:5n3) kisline (DPA) in dokozaheksaenojske (22:6n3) kisline (DHA). Izrazito odstopa razmerje mononenasičenih kislin glede na polinenasičene maščobne kisline, kar pripisujem visoki vsebnosti oleinske (18:1n9) kisline. Povišano vsebnost oleinske (18:1n9) najdem tudi pri bolnikih s črevesnimi boleznimi tipa II (KVČB-II(5)). Kontrolna skupina, ki ne vsebujejo miomov na maternici (GIN(KON)(4)) ima visoko vsebnosti palmitinske (16:0) kisline, ki je primerljiva z vsebnostjo pri bolnikih s polipi na črevesju (POL(6)). Vsebnosti stearinske (18:0) kisline in oleinske (18:1n9) kisline sta pri skupini GIN(KON)(4) najnižji. Ista skupina ima najvišjo vsebnost linolne (18:2n6) kisline. Zaradi precejšnjega odstopanja 16 vzorcev od 67 vzorcev (bolnice z miomi na maternici (GIN(3)) in njihovi kontrolni vzorci (GIN(KON)(4)) sem se odločila podrobneje pregledati izstopajoče vzorce obeh skupin glede na izbrane spremenljivke (od Slika 4-15 do Slika 4-22). Povprečne vsebnosti maščobnih kislin in standardne odmike analiziranih vzorcev skupin GIN(3), GIN(3)-podskupina, GIN(KON)(4), GIN(KON)(4)-podskupina in kontrolno skupino KON(0) sem vnesla v Preglednico 4-13 ter njihove profile maščobnih kislin prikazala na Sliki
111 R e z u l t a t i i n d i s k u s i j a Preglednica 4 13: Povprečne vsebnosti sestav maščobnih kislin fosfolipidov rdečih krvnih celic (masni delež, %) za donorje GIN(3), GIN(3)- podskupina, GIN(KON)(4), GIN(KON)(4)-podskupina in KON(0) kontrolne vzorce. Maščobne kisline GIN(3) (povp ± s) n=45 GIN(3)-podskupina (povp ± s) n=8 GIN(KON)(4) (povp ± s) n=6 GIN(KON)(4)-podskupina (povp ± s) n=8 KON(0) (povp ± s) n=70 SFA 14:0 15:0 16:0 17:0 18:0 20:0 22:0 24:0 S n-7 MUFA 16:1n7 18:1n7 n-9 MUFA 18:1n9 20:1n9 22:1n9 24:1n9 M n-6 PUFA 18:2n6 18:3n6 (GLA) 20:2n6 20:3n6 (DGLA) 20:4n6 (AA) 22:4n6 22:5n6 n6 n-3 PUFA 0,43 ± 0,14 0,27 ± 0,08 24,77 ± 5,21 0,50 ± 0,13 22,39 ± 4,03 0,18 ± 0,04 0,14 ± 0,06 0,17 ± 0,09 48,85 ± 9,11 0,37 ± 0,13 1,36 ± 0,21 17,09 ± 2,96 0,31 ± 0,08 0,06 ± 0,04 0,12 ± 0,12 20,23 ± 3,34 8,35 ± 1,88 < 0,05 0,34 ± 0,07 1,37 ± 0,54 12,42 ± 6,34 3,06 ± 1,81 0,57 ± 0,37 26,13 ± 9,94 0,49 ± 0,08 0,31 ± 0,04 31,38 ± 2,67 0,50 ± 0,05 15,19 ± 0,76 0,09 ± 0,04 0,08 ± 0,01 0,12 ± 0,03 48,15 ± 2,06 0,38 ± 0,14 1,44 ± 0,16 13,67 ± 0,90 0,20 ± 0,03 < 0,05 < 0,05 16,44 ± 1,02 20,19 ± 1,27 0,06 ± 0,06 0,38 ± 0,03 1,88 ± 0,39 8,67 ± 1,49 0,98 ± 0,42 0,23 ± 0,11 32,39 ± 2,51 0,54 ± 0,31 0,27 ± 0,12 29,61 ± 12,09 0,51 ± 0,14 19,95 ± 3,87 0,19 ± 0,05 0,16 ± 0,03 0,25 ± 0,14 51,48 ± 11,72 0,62 ± 0,38 1,62 ± 0,32 17,42 ± 3,04 0,34 ± 0,15 < 0,05 0,15 ± 0,07 21,29 ± 3,80 8,88 ± 2,05 < 0,05 0,28 ± 0,17 1,25 ± 0,58 9,98 ± 9,03 2,30 ± 2,28 0,34 ± 0,39 23,05 ± 13,16 0,58 ± 0,11 0,33 ± 0,06 34,28 ± 2,46 0,54 ± 0,09 14,30 ± 2,20 0,11 ± 0,05 0,13 ± 0,04 0,23 ± 0,09 50,49 ± 2,60 0,61 ± 0,28 1,64 ± 0,21 14,74 ± 1,56 0,18 ± 0,04 < 0,05 0,14 ± 0,10 18,26 ± 1,97 19,49 ± 2,77 < 0,05 0,36 ± 0,03 1,95 ± 0,40 6,73 ± 2,04 0,54 ± 0,31 0,15 ± 0,10 29,27 ± 3,53 0,40 ± 0,14 0,24 ± 0,09 22,26 ± 4,57 0,44 ± 0,13 20,32 ± 2,96 0,17 ± 0,04 0,13 ± 0,03 0,14 ± 0,08 44,10 ± 7,51 0,39 ± 0,17 1,29 ± 0,25 16,63 ± 2,95 0,35 ± 0,08 0,06 ± 0,03 0,08 ± 0,09 19,66 ± 3,54 9,85 ± 1,60 < 0,05 0,37 ± 0,07 1,49 ± 0,49 15,08 ± 6,02 3,65 ± 1,64 0,55 ± 0,26 31,02 ± 8,78 93
112 R e z u l t a t i i n d i s k u s i j a 18:3n3 (ALA) 18:4n3 (STD) 20:5n3 (EPA) 22:5n3 (DPA) 22:6n3 (DHA) n3 P TFA 18 :1 (6+9+11) t 18 :3 (9t,12c,15t) T DMA 16:0 DMA 18:0 DMA M/S M/P n3/n6 s: standardni odmik 0,17 ± 0,08 0,26 ± 0,24 0,39 ± 0,30 1,34 ± 0,88 2,56 ± 1,85 4,72 ± 2,61 30,92 ± 12,18 0,58 ± 0,21 0,07 ± 0,05 0,65 ± 0,21 2,29 ± 0,64 3,87 ± 1,02 0,42 ± 0,03 0,83 ± 0,47 0,18 ± 0,06 0,15 ± 0,04 < 0,05 0,30 ± 0,10 0,72 ± 0,23 1,84 ± 0,28 3,01 ± 0,55 35,41 ± 2,94 0,38 ± 0,06 < 0,05 0,39 ± 0,07 0,84 ± 0,19 0,79 ± 0,40 0,34 ± 0,01 0,47 ± 0,07 0,09 ± 0,01 0,18 ± 0,12 0,38 ± 0,29 0,63 ± 0,69 1,15 ± 0,99 1,76 ± 1,89 4,10 ± 2,42 27,21 ± 15,39 0,62 ± 0,21 0,06 ± 0,05 0,68 ± 0,20 1,72 ± 1,39 3,47 ± 2,38 0,42 ± 0,03 1,16 ± 0,87 0,19 ± 0,06 0,10 ± 0,09 < 0,05 0,23 ± 0,06 0,49 ± 0,13 1,11 ± 0,40 1,97 ± 0,46 31,25 ± 3,72 0,48 ± 0,08 < 0,05 0,48 ± 0,08 0,66 ± 0,12 0,42 ± 0,29 0,36 ± 0,04 0,60 ± 0,14 0,07 ± 0,01 0,18 ± 0,06 0,11 ± 0,14 0,39 ± 0,20 1,70 ± 0,82 2,76 ± 1,52 5,13 ± 2,33 36,24 ± 10,87 0,55 ± 0,21 0,09 ± 0,06 0,64 ± 0,20 2,31 ± 0,78 3,92 ± 1,45 0,45 ± 0,03 0,67 ± 0,46 0,16 ± 0,04 SFA, nasičene maščobne kisline; MUFA, mononenasičene maščobne kisline; PUFA, polinenasičene maščobne kisline; TFA, trans maščobne kisline; S, vsota nasičenih maščobnih kislin; M, vsota mononenasičenih maščobnih kislin; (n6), vsota n-6 polinenasičenih maščobnih kislin; (n3), vsota n-3 polinenasičenih maščobnih kislin; (P), vsota polinenasičenih maščobnih kislin; (T), vsota trans maščobnih kislin, 16:0 DMA heksadekanal dimetil acetal, 18:0 DMA oktadekanal dimetil acetal. 94
113 R e z u l t a t i i n d i s k u s i j a GIN(3) GIN(3)-podsk. GIN(KON) (4) GIN(KON) (4)-podsk. KON(0) c DGLA 204 (AA) EPA 225DPA 226DHA S M P n3 n6 M/S M/P n3/n6 160DMA 180DMA 160DMA/ DMA/180 ut. % maščobnih kislin c DGLA 204 (AA) EPA 225DPA 226DHA S M P n3 n6 M/S M/P n3/n6 160DMA 180DMA 160DMA/ DMA/ log skala (ut. % maščobnih kislin 0.01 Slika 4 14: Profili maščobnih kislin bolnic z miomi maternice, bolnic brez miomov maternice in kontrolno skupino KON(0) (izraženi v masnem deležu (%) in logaritmu masnega deleža). 95
114 R e z u l t a t i i n d i s k u s i j a Obe skupini GIN(3) in GIN(KON)(4) in njuni podskupini imajo višje vsebnosti palmitinske (16:0) kisline glede na kontrolno skupino. Pri obeh podskupinah je nižja vsebnost stearinske (18:0) kisline. Oznako 31 sem uporabila za podskupino bolnic z miomi GIN(3) in oznako 41 za podskupino žensk, ki nimajo miomov na maternici GIN(KON)(4) (Slika 4 15 do Slika 4-22). Slika 4 15: Vsebnost stearinske (18:0) kisline pri bolnicah z miomi (3, 31- podskupina) in brez miomov (4, 41- podskupina) v primerjavi s kontrolnimi vzorci (0). Slika 4 16: Vsebnost linolne (18:2n6) kisline pri bolnicah z miomi (3, 31- podskupina) in brez miomov (4, 41- podskupina) v primerjavi s kontrolnimi vzorci (0). Podskupini obeh skupin (GIN(3) in GIN(KON)(4)) imata nižje vsebnosti mononenasičenih maščobnih kislin glede na ostale bolnike in kontrolne vzorce. Pri obeh podskupinah je izstopajoča visoka vsebnost linolne (18:2n6) kisline (Slika 4-16). Nekoliko višje so še vsebnosti dihomo γ-linolenske (20:3n6) kisline, ne pa tudi arahidonske (20:4n6) kisline (AA) in adrenske (22:4n6) kisline, ki sta precej nižji od kontrolnih vrednosti (Slika 4-17 in Slika 4-18). Metabolna pot od linolne (18:2n6) kisline do arahidonske (20:4n6) kisline (AA) je verjetno prekinjena. Višje vsebnosti omega-6 kislin so pri obeh podskupinah izključno posledica višje vsebnosti linolne (18:2n6) kisline in ne njenih metabolnih produktov. 96
115 R e z u l t a t i i n d i s k u s i j a Slika 4 17: Vsebnost arahidonske (20:4n6) kisline pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41- podskupina) v primerjavi s kontrolnimi vzorci (0). Slika 4 18: Vsebnost adrenske (22:4n6) kisline pri bolnicah z miomi (3, 31- podskupina) in brez miomov (4, 41- podskupina) v primerjavi s kontrolnimi vzorci (0). Obe podskupini imata nižje vsebnosti omega-3 kislin v primerjavi s kontrolnimi vzorci (Slika 4-19). Razmerje med omega-3 in omega-6 kislinami je pri obeh podskupinah nižje od ostalih skupin (Slika 4-20). Slika 4 19: Vsebnost omega-3 kislin pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0). Slika 4 20: Vsebnost razmerja omega-3 in omega-6 kislin pri bolnicah miomi (3, 31-podskupina) in brez miomov (4, 41- podskupina) v primerjavi s kontrolnimi vzorci (0). 97
116 R e z u l t a t i i n d i s k u s i j a Največje odstopanje obeh podskupin sem opazila glede na vsebnostih dimetil acetalov (Slika 4-21 in Slika 4-22) ter njihovih razmerij s pripadajočimi maščobnimi kislinami (Preglednica 4 14, Slika 4-23). Slika 4 21: Vsebnost 16:0 DMA pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0). Slika 4 22: Vsebnost 18:0 DMA pri bolnicah z miomi (3, 31-podskupina) in brez miomov (4, 41-podskupina) v primerjavi s kontrolnimi vzorci (0). Pri vzorcih obeh podskupin (GIN(31-podskupina) in GIN(KON)(41-podskupina) so vsebnosti plazmalogenskih fosfolipidov (posledično dimetil acetalov) nizke in sklepam na povišan oksidativni stres oziroma na oksidativno prizadetost celice. Glede na vsebnost dimetil acetalov v primerjavi s kontrolnimi vzorci odstopata tudi skupini bolnikov s črevesnimi boleznimi KVČB-II(5) in polipi POL(6). V Preglednici 4-14 so prikazana razmerja med vsebnostjo acetalov in pripadajočih kislin (16:0 dimetil acetal in palmitinska (16:0) kislina ter 18:0 dimetil acetal ter stearinska (18:0) kislina), ki bi lahko glede na raziskave (Stenvinkel, 2004) predstavljala biološki označevalec tveganja tudi v primeru opisanih bolezni. 98
LIPIDI. Različne skupine molekul, skupna lastnost: netopnost v vodi.
 LIPIDI Različne skupine molekul, skupna lastnost: netopnost v vodi. maščobe, olja sestavine bioloških membran kofaktorji, prenašalci elektronov, pigmenti za absorpcijo svetlobe, hidrofobna sidra, emulzifikatorji,
LIPIDI Različne skupine molekul, skupna lastnost: netopnost v vodi. maščobe, olja sestavine bioloških membran kofaktorji, prenašalci elektronov, pigmenti za absorpcijo svetlobe, hidrofobna sidra, emulzifikatorji,
Lipid Analysis. Andréina Laffargue, IRD CRYMCEPT Montpellier workshop, October 17th Introduction to lipid structures
 Lipid Analysis Andréina Laffargue, IRD CRYMCEPT Montpellier workshop, October 17th 2005 Introduction to lipid structures Fatty acids Acylglycerols Glycerophospholipids Sterols Strategies involved in lipid
Lipid Analysis Andréina Laffargue, IRD CRYMCEPT Montpellier workshop, October 17th 2005 Introduction to lipid structures Fatty acids Acylglycerols Glycerophospholipids Sterols Strategies involved in lipid
Slika 1: Vzorci zemlje
 DELOVNI LIST INŠTITUT HAIDEGG Inštitut Haidegg je inštitut za raziskavo zemlje oz. tal. Bili so prvi, ki so leta 1987 pričeli z raziskavami. Od leta 2006 jemljejo vzorce na 1000 različnih mestih po Avstriji.
DELOVNI LIST INŠTITUT HAIDEGG Inštitut Haidegg je inštitut za raziskavo zemlje oz. tal. Bili so prvi, ki so leta 1987 pričeli z raziskavami. Od leta 2006 jemljejo vzorce na 1000 različnih mestih po Avstriji.
Celični razdelki in transport proteinov
 Celični razdelki in transport proteinov Kompartmentalizacija celic Kompartmentalizacija celic Kompartmentalizacija celic Celične membrane Glavni celični organeli Evolucijski izvor topologije celic Topology
Celični razdelki in transport proteinov Kompartmentalizacija celic Kompartmentalizacija celic Kompartmentalizacija celic Celične membrane Glavni celični organeli Evolucijski izvor topologije celic Topology
EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND ORGANOLEPTIC TRAITS OF EGGS
 Acta agriculturae Slovenica, suplement 2 (september 2008), 129 134. http://aas.bf.uni-lj.si Agris category codes: L02, Q04 COBISS Code 1.08 EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND
Acta agriculturae Slovenica, suplement 2 (september 2008), 129 134. http://aas.bf.uni-lj.si Agris category codes: L02, Q04 COBISS Code 1.08 EFFECT OF DIFFERENT SOURCE OF OILS ON FATTY ACID PROFILE AND
Lipid Analysis ISOLATION, SEPARATION, IDENTIFICATION AND. Bridgwater, England LIPIDOMIC ANALYSIS. Fourth Edition. Invergowrie, Dundee, Scotland
 Lipid Analysis ISOLATION, SEPARATION, IDENTIFICATION AND LIPIDOMIC ANALYSIS Fourth Edition WILLIAM W.CHRISTIE MRS Lipid Analysis Unit, Scottish Crop Research Institute, Dundee, Scotland Invergowrie, and
Lipid Analysis ISOLATION, SEPARATION, IDENTIFICATION AND LIPIDOMIC ANALYSIS Fourth Edition WILLIAM W.CHRISTIE MRS Lipid Analysis Unit, Scottish Crop Research Institute, Dundee, Scotland Invergowrie, and
The use of mass spectrometry in lipidomics. Outlines
 The use of mass spectrometry in lipidomics Jeevan Prasain jprasain@uab.edu 6-2612 utlines Brief introduction to lipidomics Analytical methodology: MS/MS structure elucidation of phospholipids Phospholipid
The use of mass spectrometry in lipidomics Jeevan Prasain jprasain@uab.edu 6-2612 utlines Brief introduction to lipidomics Analytical methodology: MS/MS structure elucidation of phospholipids Phospholipid
Rapid Analysis of 37 FAMEs with the Agilent 8860 Gas Chromatograph
 Application Note Food Rapid Analysis of 37 FAMEs with the Agilent 88 Gas Chromatograph Author Youjuan Zhang Agilent Technologies (Shanghai) Co. Ltd., Shanghai 131 P. R. China Abstract An Agilent 88 GC
Application Note Food Rapid Analysis of 37 FAMEs with the Agilent 88 Gas Chromatograph Author Youjuan Zhang Agilent Technologies (Shanghai) Co. Ltd., Shanghai 131 P. R. China Abstract An Agilent 88 GC
PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND. Pirjo-Liisa PENTTILÄ 1
 Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 28-33 Zreče, 4. 6. marec 2003 PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND Pirjo-Liisa PENTTILÄ 1 Ministry of
Zbornik predavanj in referatov 6. slovenskega posvetovanja o varstvu rastlin, str. 28-33 Zreče, 4. 6. marec 2003 PESTICIDE INTAKE FROM VEGETABLES AND GRAIN IN FINLAND Pirjo-Liisa PENTTILÄ 1 Ministry of
Lipids. Lipids. Jiří Jonák and Lenka Fialová Institute of Medical Biochemistry, 1st Medical Faculty of the Charles University, Prague
 Lipids Jiří Jonák and Lenka Fialová Institute of Medical Biochemistry, 1st Medical Faculty of the Charles University, Prague Lipids 1. General introduction 2. Nomenclature of fatty acids 3. Degradation
Lipids Jiří Jonák and Lenka Fialová Institute of Medical Biochemistry, 1st Medical Faculty of the Charles University, Prague Lipids 1. General introduction 2. Nomenclature of fatty acids 3. Degradation
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE. Diana DRAKSLER
 UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Diana DRAKSLER VPLIV GOJIŠČA NA SESTAVO DOLGOVERIŽNIH MAŠČOBNIH KISLIN IN MAŠČOBNIH ALDEHIDOV PRI VAMPNIH BAKTERIJAH
UNIVERZA V LJUBLJANI BIOTEHNIŠKA FAKULTETA ENOTA MEDODDELČNEGA ŠTUDIJA MIKROBIOLOGIJE Diana DRAKSLER VPLIV GOJIŠČA NA SESTAVO DOLGOVERIŽNIH MAŠČOBNIH KISLIN IN MAŠČOBNIH ALDEHIDOV PRI VAMPNIH BAKTERIJAH
Mass Spectrometry based metabolomics
 Mass Spectrometry based metabolomics Metabolomics- A realm of small molecules (
Mass Spectrometry based metabolomics Metabolomics- A realm of small molecules (
Introduction to the Study of Lipids
 Introduction to the Study of Lipids Factors to Consider in the Study of Biomolecules What are the features of the basic building blocks? (ex: monosaccharides, alcohols, fatty acids, amino acids) 1) General
Introduction to the Study of Lipids Factors to Consider in the Study of Biomolecules What are the features of the basic building blocks? (ex: monosaccharides, alcohols, fatty acids, amino acids) 1) General
OBJECTIVE. Lipids are largely hydrocarbon derivatives and thus represent
 Paper 4. Biomolecules and their interactions Module 20: Saturated and unsaturated fatty acids, Nomenclature of fatty acids and Essential and non-essential fatty acids OBJECTIVE The main aim of this module
Paper 4. Biomolecules and their interactions Module 20: Saturated and unsaturated fatty acids, Nomenclature of fatty acids and Essential and non-essential fatty acids OBJECTIVE The main aim of this module
Automated Sample Preparation for Profiling Fatty Acids in Blood and Plasma using the Agilent 7693 ALS
 Automated Sample Preparation for Profiling Fatty Acids in Blood and Plasma using the Agilent 7693 ALS Application Note Clinical Research Authors Frank David and Bart Tienpont, Research Institute for Chromatography,
Automated Sample Preparation for Profiling Fatty Acids in Blood and Plasma using the Agilent 7693 ALS Application Note Clinical Research Authors Frank David and Bart Tienpont, Research Institute for Chromatography,
LIPIDS Introduction - complex lipids. Marek Vecka
 LIPIDS Introduction - complex lipids Marek Vecka CLASSIFICATION OF LIPIDS IV - biosynthetic route Lipid class Fatty acyls Glycerolipids Glycerophospholipids Sphingolipids Sterol lipids Prenol lipids Other
LIPIDS Introduction - complex lipids Marek Vecka CLASSIFICATION OF LIPIDS IV - biosynthetic route Lipid class Fatty acyls Glycerolipids Glycerophospholipids Sphingolipids Sterol lipids Prenol lipids Other
Determination of red blood cell fatty acid profiles in clinical research
 Application Note Clinical Research Determination of red blood cell fatty acid profiles in clinical research Chemical ionization gas chromatography tandem mass spectrometry Authors Yvonne Schober 1, Hans
Application Note Clinical Research Determination of red blood cell fatty acid profiles in clinical research Chemical ionization gas chromatography tandem mass spectrometry Authors Yvonne Schober 1, Hans
Biological role of lipids
 Lipids Lipids Organic compounds present in living organisms, insoluble in water but able to be extracted by organic solvents such as: chloroform, acetone, benzene. Extraction = the action of taking out
Lipids Lipids Organic compounds present in living organisms, insoluble in water but able to be extracted by organic solvents such as: chloroform, acetone, benzene. Extraction = the action of taking out
Lipids and Classification:
 Lipids and Classification: Lipids: Biological lipids are a chemically diverse group of organic compounds which are insoluble or only poorly soluble in water. They are readily soluble in non-polar solvents
Lipids and Classification: Lipids: Biological lipids are a chemically diverse group of organic compounds which are insoluble or only poorly soluble in water. They are readily soluble in non-polar solvents
Determination of Nicotine and Cotinine in Urine by Headspace Solid Phase Microextraction Gas Chromatography with Mass Spectrometric Detection
 74 Acta Chim. Slov. 2007, 54, 74 78 Abstract Scientific paper Determination of Nicotine and Cotinine in Urine by Headspace Solid Phase Microextraction Gas Chromatography with Mass Spectrometric Detection
74 Acta Chim. Slov. 2007, 54, 74 78 Abstract Scientific paper Determination of Nicotine and Cotinine in Urine by Headspace Solid Phase Microextraction Gas Chromatography with Mass Spectrometric Detection
Classification, functions and structure
 Classification, functions and structure Elena Rivneac PhD, Associate Professor Department of Biochemistry and Clinical Biochemistry State University of Medicine and Pharmacy "Nicolae Testemitanu" Lipids
Classification, functions and structure Elena Rivneac PhD, Associate Professor Department of Biochemistry and Clinical Biochemistry State University of Medicine and Pharmacy "Nicolae Testemitanu" Lipids
Blood and brain fatty acid contents in aged rats supplemented with n-3 long-chain polyunsaturated fatty acids
 Blood and brain fatty acid contents in aged rats supplemented with n-3 long-chain polyunsaturated fatty acids Anne Létondor 1,2,3, Benjamin Buaud 3, Carole Vaysse 3, Laurence Fonseca 3,Coralie Herrouin
Blood and brain fatty acid contents in aged rats supplemented with n-3 long-chain polyunsaturated fatty acids Anne Létondor 1,2,3, Benjamin Buaud 3, Carole Vaysse 3, Laurence Fonseca 3,Coralie Herrouin
PHOSPHOLIPID MEMBRANE ABNORMALITIES AND REDUCED NIACIN SKIN FLUSH RESPONSE IN SCHIZOPHRENIA
 PHOSPHOLIPID MEMBRANE ABNORMALITIES AND REDUCED NIACIN SKIN FLUSH RESPONSE IN SCHIZOPHRENIA Alena Buretić-Tomljanović 1, Jasminka Giacometti 1, Sergej Nadalin 1, Gordana Rubeša 2, Mirjana Vulin 3, Draško
PHOSPHOLIPID MEMBRANE ABNORMALITIES AND REDUCED NIACIN SKIN FLUSH RESPONSE IN SCHIZOPHRENIA Alena Buretić-Tomljanović 1, Jasminka Giacometti 1, Sergej Nadalin 1, Gordana Rubeša 2, Mirjana Vulin 3, Draško
SUPPLEMENTARY DATA. Materials and Methods
 SUPPLEMENTARY DATA Materials and Methods HPLC-UV of phospholipid classes and HETE isomer determination. Fractionation of platelet lipid classes was undertaken on a Spherisorb S5W 150 x 4.6 mm column (Waters
SUPPLEMENTARY DATA Materials and Methods HPLC-UV of phospholipid classes and HETE isomer determination. Fractionation of platelet lipid classes was undertaken on a Spherisorb S5W 150 x 4.6 mm column (Waters
Principles of Shotgun Lipidomics
 Principles of Shotgun Lipidomics Xianlin Han Diabetes and Obesity Research Center Sanford-Burnham Medical Research Institute Lake Nona Orlando, FL 32827 What is shotgun lipidomics? Original definition
Principles of Shotgun Lipidomics Xianlin Han Diabetes and Obesity Research Center Sanford-Burnham Medical Research Institute Lake Nona Orlando, FL 32827 What is shotgun lipidomics? Original definition
Lipid and Bile Acids as NAFLD- Related Biomarkers
 Lipid and Bile Acids as NAFLD- Related Biomarkers Puneet Puri, MBBS, MD Division of Gastroenterology, Hepatology and Nutrition Virginia Commonwealth University, Richmond, VA 1st International Workshop
Lipid and Bile Acids as NAFLD- Related Biomarkers Puneet Puri, MBBS, MD Division of Gastroenterology, Hepatology and Nutrition Virginia Commonwealth University, Richmond, VA 1st International Workshop
Factors to Consider in the Study of Biomolecules
 Factors to Consider in the Study of Biomolecules What are the features of the basic building blocks? (ex: monosaccharides, alcohols, fatty acids, amino acids) 1) General structure and functional groups
Factors to Consider in the Study of Biomolecules What are the features of the basic building blocks? (ex: monosaccharides, alcohols, fatty acids, amino acids) 1) General structure and functional groups
Table S1: Fatty acid composition (% total lipids) of the oil extracted from Thraustochytrium
 Supplementary Information Table S: Fatty acid composition (% total lipids) of the oil extracted from Thraustochytrium sp. AH-2 (PRA-296 TM ) by GC-FAME technique according to the protocol and conditions
Supplementary Information Table S: Fatty acid composition (% total lipids) of the oil extracted from Thraustochytrium sp. AH-2 (PRA-296 TM ) by GC-FAME technique according to the protocol and conditions
Test Bank for Lehninger Principles of Biochemistry 5th Edition by Nelson
 Test Bank for Lehninger Principles of Biochemistry 5th Edition by Nelson Link download full: http://testbankair.com/download/test-bank-forlehninger-principles-of-biochemistry-5th-edition-by-nelson/ Chapter
Test Bank for Lehninger Principles of Biochemistry 5th Edition by Nelson Link download full: http://testbankair.com/download/test-bank-forlehninger-principles-of-biochemistry-5th-edition-by-nelson/ Chapter
Lipids Analysis. Lipids
 Lipids Analysis Stephen Barnes 3 5 15 Lipids Lipids are mostly very hydrophobic Most are conjugates of fatty acids of a variety of chain lengths, which have different degrees of unsaturation, cis trans
Lipids Analysis Stephen Barnes 3 5 15 Lipids Lipids are mostly very hydrophobic Most are conjugates of fatty acids of a variety of chain lengths, which have different degrees of unsaturation, cis trans
Analysis of Omega 3 and Omega 6 FAMEs in Fish Oil and Animal Fat Using an Agilent J&W DB-FATWAX Ultra Inert GC Column
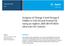 Application Note Food Analysis of Omega 3 and Omega 6 FAMEs in Fish Oil and Animal Fat Using an Agilent J&W DB-FATWAX Ultra Inert GC Column Authors Ingrid Van Der Meer, Yun Zou, and Gustavo Serrano Agilent
Application Note Food Analysis of Omega 3 and Omega 6 FAMEs in Fish Oil and Animal Fat Using an Agilent J&W DB-FATWAX Ultra Inert GC Column Authors Ingrid Van Der Meer, Yun Zou, and Gustavo Serrano Agilent
Facts on Fats. Ronald P. Mensink
 Facts on Fats Ronald P. Mensink Department of Human Biology NUTRIM, School for Nutrition, Toxicology and Metabolism Maastricht University Maastricht The Netherlands Outline of the Presentation Saturated
Facts on Fats Ronald P. Mensink Department of Human Biology NUTRIM, School for Nutrition, Toxicology and Metabolism Maastricht University Maastricht The Netherlands Outline of the Presentation Saturated
Ahmad O. Olimat. Abdallah Al-Qawasmeh. Dr.Mamoun
 10 Ahmad O. Olimat Abdallah Al-Qawasmeh Mohammed Yousef Dr.Mamoun A QUICK RECAP Eicosanoids They are derived from Arachidonic acid, a fatty acid that contains 20 carbon atoms and four double bonds. They
10 Ahmad O. Olimat Abdallah Al-Qawasmeh Mohammed Yousef Dr.Mamoun A QUICK RECAP Eicosanoids They are derived from Arachidonic acid, a fatty acid that contains 20 carbon atoms and four double bonds. They
Janussan Gunasingham. A thesis. presented to the University of Waterloo. in fulfillment of the. thesis requirement for the degree of
 Dried Blood Spot Fatty Acid Quantitation: Developing Methods for Determining Unknown Volumes, Identifying Contaminants and Assessing Fatty Acid Stability During Storage by Janussan Gunasingham A thesis
Dried Blood Spot Fatty Acid Quantitation: Developing Methods for Determining Unknown Volumes, Identifying Contaminants and Assessing Fatty Acid Stability During Storage by Janussan Gunasingham A thesis
Supplementary Information. Effects of Perfluorooctanoic Acid on Metabolic Profiles in Brain and Liver of Mouse by a
 Supplementary Information Effects of Perfluorooctanoic Acid on Metabolic Profiles in Brain and Liver of Mouse by a High-throughput Targeted Metabolomics Approach Nanyang Yu, Si Wei, *, Meiying Li, Jingping
Supplementary Information Effects of Perfluorooctanoic Acid on Metabolic Profiles in Brain and Liver of Mouse by a High-throughput Targeted Metabolomics Approach Nanyang Yu, Si Wei, *, Meiying Li, Jingping
Supplementary Information
 Supplementary Information Serum and synovial fluid lipidomic profiles predict obesity-associated osteoarthritis, synovitis, and wound repair Chia-Lung Wu 1,2, Kelly A. Kimmerling 1,2, Dianne Little 3,
Supplementary Information Serum and synovial fluid lipidomic profiles predict obesity-associated osteoarthritis, synovitis, and wound repair Chia-Lung Wu 1,2, Kelly A. Kimmerling 1,2, Dianne Little 3,
Glycerolipid Analysis. LC/MS/MS Analytical Services
 Glycerolipid Analysis LC/MS/MS Analytical Services Molecular Characterization and Quantitation of Glycerophospholipids in Commercial Lecithins by High Performance Liquid Chromatography with Mass Spectrometric
Glycerolipid Analysis LC/MS/MS Analytical Services Molecular Characterization and Quantitation of Glycerophospholipids in Commercial Lecithins by High Performance Liquid Chromatography with Mass Spectrometric
Pripravki levkocitov. Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana
 Pripravki levkocitov Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana Razdelitev levkocitov Granulociti polimorfonuklearni levkociti Nevtrofilci Bazofilci Eozinofilci Agranulociti
Pripravki levkocitov Dr. Dragoslav Domanovič, dr.med. Zavod RS za transfuzijsko medicino Ljubljana Razdelitev levkocitov Granulociti polimorfonuklearni levkociti Nevtrofilci Bazofilci Eozinofilci Agranulociti
Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond s strength
 RMZ Materials and Geoenvironment, Vol. 55, No. 2, pp. 191-197, 2008 191 Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond
RMZ Materials and Geoenvironment, Vol. 55, No. 2, pp. 191-197, 2008 191 Artificial tooth and polymer-base bond in removable dentures: the influence of pre-treatment on technological parameters to the bond
DETERMINATION OF FATTY ACIDS IN EDIBLE OILS BY CAPILARY GC
 DETERMINATION OF FATTY ACIDS IN EDIBLE OILS BY CAPILARY GC Vesna Kostik 1 University Goce Delcev Stip Faculty of Medicine Department of Pharmacy 1 WHY FATTY ACID (FA) ANALYSIS IN EDIBLE OILS The content
DETERMINATION OF FATTY ACIDS IN EDIBLE OILS BY CAPILARY GC Vesna Kostik 1 University Goce Delcev Stip Faculty of Medicine Department of Pharmacy 1 WHY FATTY ACID (FA) ANALYSIS IN EDIBLE OILS The content
Chapter 20 Lipids. Organic and Biochem
 Chapter 20 Lipids rganic and Biochem 20.1 Introduction Found in living organisms Insoluble in water but Soluble in non-polar substances Example of Lipid Solvent: diethyl ether Polar groups in lipids are
Chapter 20 Lipids rganic and Biochem 20.1 Introduction Found in living organisms Insoluble in water but Soluble in non-polar substances Example of Lipid Solvent: diethyl ether Polar groups in lipids are
Fats and Lipids (Ans570)
 Fats and Lipids (Ans570) Outlines Fats and Lipids Structure, nomenclature Phospholipids, Sterols, and Lipid Derivatives Lipid Oxidation Roles of fat in food processing and dietary fat Lipid and fat analysis:
Fats and Lipids (Ans570) Outlines Fats and Lipids Structure, nomenclature Phospholipids, Sterols, and Lipid Derivatives Lipid Oxidation Roles of fat in food processing and dietary fat Lipid and fat analysis:
FATTY ACIDS (FAs) SIMPLE AND COMPLEX LIPIDS
 FATTY ACIDS (FAs) SIMPLE AND COMPLEX LIPIDS Dicarboxylic acids, ketone bodies. Department of General Chemistry Structure and classification of lipids Lipids can be divided into five categories, on the
FATTY ACIDS (FAs) SIMPLE AND COMPLEX LIPIDS Dicarboxylic acids, ketone bodies. Department of General Chemistry Structure and classification of lipids Lipids can be divided into five categories, on the
Skeletal muscle metabolism was studied by measuring arterio-venous concentration differences
 Supplemental Data Dual stable-isotope experiment Skeletal muscle metabolism was studied by measuring arterio-venous concentration differences across the forearm, adjusted for forearm blood flow (FBF) (1).
Supplemental Data Dual stable-isotope experiment Skeletal muscle metabolism was studied by measuring arterio-venous concentration differences across the forearm, adjusted for forearm blood flow (FBF) (1).
Chapter 11: Lipids. Voet & Voet: Pages
 Chapter 11: Lipids Voet & Voet: Pages 380-394 Slide 1 Lipids Lipids are distinguished by their high solubility in non polar solvents and low solubility in H2O Diverse group of compounds including Fats,
Chapter 11: Lipids Voet & Voet: Pages 380-394 Slide 1 Lipids Lipids are distinguished by their high solubility in non polar solvents and low solubility in H2O Diverse group of compounds including Fats,
Organism. Organ and organ systems. Tissue. Cells. Carbohydrates Proteins Lipids Nucleic Acids
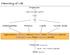 hemistry of Life rganism rgan and organ systems Tissue ells arbohydrates Proteins Lipids Nucleic Acids Hydrocarbons, Alcohols, Phenols, Ethers, Thiols, Aldehydes, Ketones, arboxylic Acids, Esters, Amines,
hemistry of Life rganism rgan and organ systems Tissue ells arbohydrates Proteins Lipids Nucleic Acids Hydrocarbons, Alcohols, Phenols, Ethers, Thiols, Aldehydes, Ketones, arboxylic Acids, Esters, Amines,
GINKGO BILOBA IN MISELNE SPOSOBNOSTI. Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015
 GINKGO BILOBA IN MISELNE SPOSOBNOSTI Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015 KLINIČNO VPRAŠANJE Ali uporaba standardiziranih pripravkov Ginkgo bilobe izboljšuje
GINKGO BILOBA IN MISELNE SPOSOBNOSTI Avtorji: Jelena Raković, Božica Ljušanin Grbavac 18. modularna skupina April 2015 KLINIČNO VPRAŠANJE Ali uporaba standardiziranih pripravkov Ginkgo bilobe izboljšuje
CHAPTER 28 LIPIDS SOLUTIONS TO REVIEW QUESTIONS
 HAPTER 28 LIPIDS SLUTINS T REVIEW QUESTINS 1. The lipids, which are dissimilar substances, are arbitrarily classified as a group on the basis of their solubility in fat solvents and their insolubility
HAPTER 28 LIPIDS SLUTINS T REVIEW QUESTINS 1. The lipids, which are dissimilar substances, are arbitrarily classified as a group on the basis of their solubility in fat solvents and their insolubility
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANA TITAN DIPLOMSKA NALOGA. Univerzitetni študij farmacije
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANA TITAN DIPLOMSKA NALOGA Univerzitetni študij farmacije Ljubljana, 2011 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANA TITAN DOLOČANJE MALONDIALDEHIDA V PLAZMI
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANA TITAN DIPLOMSKA NALOGA Univerzitetni študij farmacije Ljubljana, 2011 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ANA TITAN DOLOČANJE MALONDIALDEHIDA V PLAZMI
Zillillah, a Guowei Tan, a,b and Zhi Li* a,b. 4 Engineering Drive 4, Singapore Fax: ; Tel:
 Highly Active, Stable, and Recyclable Magnetic Nano-size Solid Acid Catalysts: Efficient Esterification of Free Fatty Acid in Grease to Produce Biodiesel Zillillah, a Guowei Tan, a,b and Zhi Li* a,b a
Highly Active, Stable, and Recyclable Magnetic Nano-size Solid Acid Catalysts: Efficient Esterification of Free Fatty Acid in Grease to Produce Biodiesel Zillillah, a Guowei Tan, a,b and Zhi Li* a,b a
General Biochemistry-1 BCH 202
 General Biochemistry-1 BCH 202 1 I would like to acknowledge Dr. Farid Ataya for his valuable input & help in this course. 2 Outline Lipids Definition, function, fatty acids, classification: simple lipids:
General Biochemistry-1 BCH 202 1 I would like to acknowledge Dr. Farid Ataya for his valuable input & help in this course. 2 Outline Lipids Definition, function, fatty acids, classification: simple lipids:
BIOB111_CHBIO - Tutorial activity for Session 12
 BIOB111_CHBIO - Tutorial activity for Session 12 General topic for week 6 Session 12 Lipids Useful Links: 1. Animations on Cholesterol (its synthesis, lifestyle factors, LDL) http://www.wiley.com/college/boyer/0470003790/animations/cholesterol/cholesterol.htm
BIOB111_CHBIO - Tutorial activity for Session 12 General topic for week 6 Session 12 Lipids Useful Links: 1. Animations on Cholesterol (its synthesis, lifestyle factors, LDL) http://www.wiley.com/college/boyer/0470003790/animations/cholesterol/cholesterol.htm
Enrichment of Phospholipids from Biological Matrices with Zirconium Oxide-Modified Silica Sorbents
 Enrichment of Phospholipids from Biological Matrices with Zirconium Oxide-Modified Silica Sorbents Xiaoning Lu, Jennifer E. Claus, and David S. Bell Supelco, Div. of Sigma-Aldrich Bellefonte, PA 16823
Enrichment of Phospholipids from Biological Matrices with Zirconium Oxide-Modified Silica Sorbents Xiaoning Lu, Jennifer E. Claus, and David S. Bell Supelco, Div. of Sigma-Aldrich Bellefonte, PA 16823
MPS Advanced Plant Biochemistry Course
 MPS 587 - Advanced Plant Biochemistry Course Lipids section guest lecture: Philip Bates Post-doc Browse lab Office: 453 Clark Hall Email: phil_bates@wsu.edu Lecture 9 Lipids I 1. What is a lipid? 2. Fatty
MPS 587 - Advanced Plant Biochemistry Course Lipids section guest lecture: Philip Bates Post-doc Browse lab Office: 453 Clark Hall Email: phil_bates@wsu.edu Lecture 9 Lipids I 1. What is a lipid? 2. Fatty
CHAPTER 28 LIPIDS SOLUTIONS TO REVIEW QUESTIONS
 28 09/16/2013 17:44:40 Page 415 APTER 28 LIPIDS SLUTINS T REVIEW QUESTINS 1. The lipids, which are dissimilar substances, are arbitrarily classified as a group on the basis of their solubility in fat solvents
28 09/16/2013 17:44:40 Page 415 APTER 28 LIPIDS SLUTINS T REVIEW QUESTINS 1. The lipids, which are dissimilar substances, are arbitrarily classified as a group on the basis of their solubility in fat solvents
Metabolomic fingerprinting of serum samples by direct infusion mass spectrometry
 Metabolomic fingerprinting of serum samples by direct infusion mass spectrometry Raúl González-Domínguez * Department of Chemistry, Faculty of Experimental Sciences. University of Huelva, Spain. * Corresponding
Metabolomic fingerprinting of serum samples by direct infusion mass spectrometry Raúl González-Domínguez * Department of Chemistry, Faculty of Experimental Sciences. University of Huelva, Spain. * Corresponding
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ŠPELA PERČIČ MAGISTRSKA NALOGA ENOVITI MAGISTRSKI ŠTUDIJ FARMACIJE
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ŠPELA PERČIČ MAGISTRSKA NALOGA ENOVITI MAGISTRSKI ŠTUDIJ FARMACIJE Ljubljana, 2015 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ŠPELA PERČIČ MAŠČOBNOKISLINSKA
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ŠPELA PERČIČ MAGISTRSKA NALOGA ENOVITI MAGISTRSKI ŠTUDIJ FARMACIJE Ljubljana, 2015 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO ŠPELA PERČIČ MAŠČOBNOKISLINSKA
By: Dr Hadi Mozafari 1
 Biological lipids are a chemically diverse group of compounds, the common and defining feature of which is their insolubility in water. By: Dr Hadi Mozafari 1 Fats and oils are the principal stored forms
Biological lipids are a chemically diverse group of compounds, the common and defining feature of which is their insolubility in water. By: Dr Hadi Mozafari 1 Fats and oils are the principal stored forms
Agilent Solutions for Lipidomics. Greater Insight into
 Agilent Solutions for Lipidomics Greater Insight into Lipid Metabolism Understanding Lipidomics What is Lipidomics? The term "lipidome" refers to all the lipids that exist in an organism and their effects
Agilent Solutions for Lipidomics Greater Insight into Lipid Metabolism Understanding Lipidomics What is Lipidomics? The term "lipidome" refers to all the lipids that exist in an organism and their effects
2013 W. H. Freeman and Company. 10 Lipids
 2013 W. H. Freeman and Company 10 Lipids CHAPTER 10 Lipids Key topics: Biological roles of lipids Structure and properties of storage lipids Structure and properties of membrane lipids Structure and properties
2013 W. H. Freeman and Company 10 Lipids CHAPTER 10 Lipids Key topics: Biological roles of lipids Structure and properties of storage lipids Structure and properties of membrane lipids Structure and properties
Electronic supplementary information (ESI) Materials and Methods Lipid extraction 1 ml ammonium hydroxide was added to 5 ml breast milk, shaken at 65
 Electronic Supplementary Material (ESI) for Food & Function. This journal is The Royal Society of Chemistry 2018 Electronic supplementary information (ESI) Materials and Methods Lipid extraction 1 ml ammonium
Electronic Supplementary Material (ESI) for Food & Function. This journal is The Royal Society of Chemistry 2018 Electronic supplementary information (ESI) Materials and Methods Lipid extraction 1 ml ammonium
Mass-Spectrometric Analysis of Lipids (Lipidomics)
 Mass-Spectrometric Analysis of Lipids (Lipidomics) 1. Identification 2. Quantification 3. Metabolism Why to do lipidomics? Biology: Functions of different lipids? Medicine: Diagnostics and Therapy Industry:
Mass-Spectrometric Analysis of Lipids (Lipidomics) 1. Identification 2. Quantification 3. Metabolism Why to do lipidomics? Biology: Functions of different lipids? Medicine: Diagnostics and Therapy Industry:
LC/MS Method for Comprehensive Analysis of Plasma Lipids
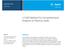 Application Note omics LC/MS Method for Comprehensive Analysis of Plasma s Authors Tomas Cajka and Oliver Fiehn West Coast Metabolomics Center, University of California Davis, 451 Health Sciences Drive,
Application Note omics LC/MS Method for Comprehensive Analysis of Plasma s Authors Tomas Cajka and Oliver Fiehn West Coast Metabolomics Center, University of California Davis, 451 Health Sciences Drive,
Impact of Chromatography on Lipid Profiling of Liver Tissue Extracts
 Impact of Chromatography on Lipid Profiling of Liver Tissue Extracts Application Note Clinical Research Authors Mark Sartain and Theodore Sana Agilent Technologies, Inc. Santa Clara, California, USA Introduction
Impact of Chromatography on Lipid Profiling of Liver Tissue Extracts Application Note Clinical Research Authors Mark Sartain and Theodore Sana Agilent Technologies, Inc. Santa Clara, California, USA Introduction
A Definitive Lipidomics Workflow for Human Plasma Utilizing Off-line Enrichment and Class Specific Separation of Phospholipids
 A Definitive Lipidomics Workflow for Human Plasma Utilizing Off-line Enrichment and Class Specific Separation of Phospholipids Jeremy Netto, 1 Stephen Wong, 1 Federico Torta, 2 Pradeep Narayanaswamy, 2
A Definitive Lipidomics Workflow for Human Plasma Utilizing Off-line Enrichment and Class Specific Separation of Phospholipids Jeremy Netto, 1 Stephen Wong, 1 Federico Torta, 2 Pradeep Narayanaswamy, 2
Phospholipids Metabolism
 Chapter VI: Phospholipids Metabolism Dr. Sameh Sarray Hlaoui Phospholipids Features: Amphipatic: - Hydrophobic head: fatty acids - Hydropholic head: P group+ alcohol Composed of alcohol attached by a phosphodiester
Chapter VI: Phospholipids Metabolism Dr. Sameh Sarray Hlaoui Phospholipids Features: Amphipatic: - Hydrophobic head: fatty acids - Hydropholic head: P group+ alcohol Composed of alcohol attached by a phosphodiester
Comparative Study of Fat (Total Cholestrol and Fatty acids) Profile in Farm cultivated and river water fishes communities of Labeo rohita
 International Journal of Scientific and Research Publications, Volume 7, Issue 7, July 2017 763 Comparative Study of Fat (Total Cholestrol and Fatty acids) Profile in Farm cultivated and river water fishes
International Journal of Scientific and Research Publications, Volume 7, Issue 7, July 2017 763 Comparative Study of Fat (Total Cholestrol and Fatty acids) Profile in Farm cultivated and river water fishes
ANSC (NUTR) 618 LIPIDS & LIPID METABOLISM Membrane Lipids and Sphingolipidsd
 ANSC (NUTR) 618 LIPIDS & LIPID METABOLISM Membrane Lipids and Sphingolipidsd I. Classes of membrane lipids A. Glycerolipids (quantitatively the most important of the three membrane lipids) B. Shingolipids
ANSC (NUTR) 618 LIPIDS & LIPID METABOLISM Membrane Lipids and Sphingolipidsd I. Classes of membrane lipids A. Glycerolipids (quantitatively the most important of the three membrane lipids) B. Shingolipids
: Overview of EFA metabolism
 Figure 1 gives an overview of the metabolic fate of the EFAs when consumed in the diet. The n-6 and n-3 PUFAs when consumed in the form of dietary triglyceride from various food sources undergoes digestion
Figure 1 gives an overview of the metabolic fate of the EFAs when consumed in the diet. The n-6 and n-3 PUFAs when consumed in the form of dietary triglyceride from various food sources undergoes digestion
PHOSPHOLIPIDS METABOLISM. BY Dr. Walid Said Zaki Dr. Marwa Ali LECTURER OF BIOCHEMISTRY AND MOLECULAR BIOLOGY
 PHOSPHOLIPIDS METABOLISM BY Dr. Walid Said Zaki Dr. Marwa Ali LECTURER OF BIOCHEMISTRY AND MOLECULAR BIOLOGY 1. State the definition and classification of Phospholipids. 2. Describe the general structure
PHOSPHOLIPIDS METABOLISM BY Dr. Walid Said Zaki Dr. Marwa Ali LECTURER OF BIOCHEMISTRY AND MOLECULAR BIOLOGY 1. State the definition and classification of Phospholipids. 2. Describe the general structure
MEMBRANE LIPIDS I and II: GLYCEROPHOSPHOLIPIDS AND SPHINGOLIPIDS
 December 6, 2011 Lecturer: Eileen M. Lafer MEMBRANE LIPIDS I and II: GLYCEROPHOSPHOLIPIDS AND SPHINGOLIPIDS Reading: Stryer Edition 6: Chapter 26 Images: All images in these notes were taken from Lehninger,
December 6, 2011 Lecturer: Eileen M. Lafer MEMBRANE LIPIDS I and II: GLYCEROPHOSPHOLIPIDS AND SPHINGOLIPIDS Reading: Stryer Edition 6: Chapter 26 Images: All images in these notes were taken from Lehninger,
Detection of Lipid Peroxidation Products From Free Radical and Enzymatic Processes. Jason D. Morrow M.D. Vanderbilt University School of Medicine
 Detection of Lipid Peroxidation Products From Free Radical and Enzymatic Processes Jason D. Morrow M.D. Vanderbilt University School of Medicine Question? Which one of the following is the most accurate
Detection of Lipid Peroxidation Products From Free Radical and Enzymatic Processes Jason D. Morrow M.D. Vanderbilt University School of Medicine Question? Which one of the following is the most accurate
Nafith Abu Tarboush DDS, MSc, PhD
 Nafith Abu Tarboush DDS, MSc, PhD natarboush@ju.edu.jo www.facebook.com/natarboush Lipids (cholesterol, cholesterol esters, phospholipids & triacylglycerols) combined with proteins (apolipoprotein) in
Nafith Abu Tarboush DDS, MSc, PhD natarboush@ju.edu.jo www.facebook.com/natarboush Lipids (cholesterol, cholesterol esters, phospholipids & triacylglycerols) combined with proteins (apolipoprotein) in
AOAC Official Method Determination of Labeled Fatty Acids Content in Milk Products and Infant Formula
 AOAC Official Method 2012.13 Determination of Labeled Fatty Acids Content in Milk Products and Infant Formula Capillary Gas Chromatography First Action 2012 A. Scope The method involves the quantification
AOAC Official Method 2012.13 Determination of Labeled Fatty Acids Content in Milk Products and Infant Formula Capillary Gas Chromatography First Action 2012 A. Scope The method involves the quantification
ANSC 619 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIES. Lipid Chemistry NO. OF CARBONS COMMON NAME GENEVA NAME STRUCTURE
 ANSC 619 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIES I. Common Saturated Fatty Acids NO. OF CARBONS COMMON NAME GENEVA NAME STRUCTURE 4 Butyric Tetranoic CH 3 (CH 2 ) 2 COOH 6 Caproic Hexanoic CH 3 (CH
ANSC 619 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIES I. Common Saturated Fatty Acids NO. OF CARBONS COMMON NAME GENEVA NAME STRUCTURE 4 Butyric Tetranoic CH 3 (CH 2 ) 2 COOH 6 Caproic Hexanoic CH 3 (CH
Lipids. Dr. Mamoun Ahram Summer semester, Resources This lecture Campbell and Farrell s Biochemistry, Chapter 8
 Lipids Dr. Mamoun Ahram Summer semester, 2017-2018 Resources This lecture Campbell and Farrell s Biochemistry, Chapter 8 Lipids Lipids are a heterogeneous class of naturally occurring organic compounds
Lipids Dr. Mamoun Ahram Summer semester, 2017-2018 Resources This lecture Campbell and Farrell s Biochemistry, Chapter 8 Lipids Lipids are a heterogeneous class of naturally occurring organic compounds
Chem 5 PAL Worksheet Lipids Smith text Chapter 15
 Chem 5 PAL Worksheet Lipids Smith text Chapter 15 Principle: Fatty acids are carboxylic acids with long (usually > 14) carbon chains which can be saturated (no carbon-carbon double bonds) are unsaturated
Chem 5 PAL Worksheet Lipids Smith text Chapter 15 Principle: Fatty acids are carboxylic acids with long (usually > 14) carbon chains which can be saturated (no carbon-carbon double bonds) are unsaturated
Thin layer absorption chromatography can achieve very good separation of small lipid samples
 Abbreviations Preface Acknowledgements Lipids: definition, isolation, separation and detection p. 1 Introduction p. 1 Definitions p. 1 Structural chemistry and nomenclature p. 1 Extraction of lipids from
Abbreviations Preface Acknowledgements Lipids: definition, isolation, separation and detection p. 1 Introduction p. 1 Definitions p. 1 Structural chemistry and nomenclature p. 1 Extraction of lipids from
Improving the Analysis of 37 Fatty Acid Methyl Esters
 Application Note Food Testing Improving the Analysis of 37 Fatty Acid Methyl Esters Using Three Types of Capillary GC columns Authors Yun Zou Agilent Technologies (Shanghai) Co.Ltd, Shanghai 200131 P.R.China
Application Note Food Testing Improving the Analysis of 37 Fatty Acid Methyl Esters Using Three Types of Capillary GC columns Authors Yun Zou Agilent Technologies (Shanghai) Co.Ltd, Shanghai 200131 P.R.China
Biochemistry. Classification of Lipids METABOLISM OF LIPIDS. Principal Investigator
 Paper : 05 Metabolism of Lipids Module: 04 Principal Investigator Paper Coordinator and Content Writer Content Reviewer Dr. Sunil Kumar Khare, Professor, Department of Chemistry, IIT-Delhi Dr. Suaib Luqman,
Paper : 05 Metabolism of Lipids Module: 04 Principal Investigator Paper Coordinator and Content Writer Content Reviewer Dr. Sunil Kumar Khare, Professor, Department of Chemistry, IIT-Delhi Dr. Suaib Luqman,
Introduction to Lipid Chemistry
 Introduction to Lipid Chemistry Benjamin Schwartz Ontario SCC Education Day September 18, 2018 Lipid knowledge for the personal care industry What is a Lipid? Lipids are fatty acids and their derivatives,
Introduction to Lipid Chemistry Benjamin Schwartz Ontario SCC Education Day September 18, 2018 Lipid knowledge for the personal care industry What is a Lipid? Lipids are fatty acids and their derivatives,
Column Selection for the Analysis of Fatty Acid Methyl Esters Application
 Column Selection for the Analysis of Fatty Acid Methyl Esters Application Food Analysis Authors Frank David Research Institute for Chromatography President Kennedy Park B- Kortrijk, Belgium Pat Sandra
Column Selection for the Analysis of Fatty Acid Methyl Esters Application Food Analysis Authors Frank David Research Institute for Chromatography President Kennedy Park B- Kortrijk, Belgium Pat Sandra
Poly-unsaturated phospholipids WE (FA18:1) A B C D OAHFA 18:1/24:0 OAHFA 18:1/30:2 PS 38:4 C18:1C23:0 OAHFA 18:1/25:0 OAHFA 18:1/30:1
 Figure S1, related to Figure 1. Correlation scatter plots illustrating individual lipid species from various classes that exhibited statistically significant correlations to age. (A-B) Various species
Figure S1, related to Figure 1. Correlation scatter plots illustrating individual lipid species from various classes that exhibited statistically significant correlations to age. (A-B) Various species
REPORT NO.2532 LIPID AND FATTY ACID COMPOSITION OF NEW ZEALAND GREENSHELL TM MUSSELS (GSM) FROM THREE FARMING SITES
 REPORT NO.2532 LIPID AND FATTY ACID COMPOSITION OF NEW ZEALAND GREENSHELL TM MUSSELS (GSM) FROM THREE FARMING SITES CAWTHRON INSTITUTE REPORT NO.2532 MAY 2014 LIPID AND FATTY ACID COMPOSITION OF NEW ZEALAND
REPORT NO.2532 LIPID AND FATTY ACID COMPOSITION OF NEW ZEALAND GREENSHELL TM MUSSELS (GSM) FROM THREE FARMING SITES CAWTHRON INSTITUTE REPORT NO.2532 MAY 2014 LIPID AND FATTY ACID COMPOSITION OF NEW ZEALAND
SelexION Technology for Lipid Analysis: Pushing the Boundaries of Lipidomics
 ANSWERS FOR SCIENCE. KNOWLEDGE FOR LIFE. SelexION Technology for Lipid Analysis: Pushing the Boundaries of Lipidomics Baljit Ubhi, Ph.D ASMS Baltimore, June 2014 Lipidomics Profiling Needs and Deliverables
ANSWERS FOR SCIENCE. KNOWLEDGE FOR LIFE. SelexION Technology for Lipid Analysis: Pushing the Boundaries of Lipidomics Baljit Ubhi, Ph.D ASMS Baltimore, June 2014 Lipidomics Profiling Needs and Deliverables
ANSC 689 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIDS General Chemistry of Fatty Acids and Triacylglycerols
 ANSC 689 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIDS General Chemistry of Fatty Acids and Triacylglycerols I. Common Saturated Fatty Acids NO. OF CARBONS COMMON NAME GENEVA NAME STRUCTURE 4 Butyric Tetranoic
ANSC 689 PHYSIOLOGICAL CHEMISTRY OF LIVESTOCK SPECIDS General Chemistry of Fatty Acids and Triacylglycerols I. Common Saturated Fatty Acids NO. OF CARBONS COMMON NAME GENEVA NAME STRUCTURE 4 Butyric Tetranoic
Fluorinated esters in a rapid GC analysis of very long chain fatty acids. Vyssotski, M, Svetashev, V, Lagutin, K
 Fluorinated esters in a rapid GC analysis of very long chain fatty acids Vyssotski, M, Svetashev, V, Lagutin, K Definition: "Fatty acids with greater than 22 carbon atoms (very long chain fatty acids,
Fluorinated esters in a rapid GC analysis of very long chain fatty acids Vyssotski, M, Svetashev, V, Lagutin, K Definition: "Fatty acids with greater than 22 carbon atoms (very long chain fatty acids,
COBISS: 1.01 Agris category code: Q04
 COBISS: 1.01 Agris category code: Q04 Variations in the fatty acid composition and nutritional value of Adriatic sardine (Sardina pilchardus Walb.) through the fishing season 1 Monika MARIN 2, Tomaž POLAK
COBISS: 1.01 Agris category code: Q04 Variations in the fatty acid composition and nutritional value of Adriatic sardine (Sardina pilchardus Walb.) through the fishing season 1 Monika MARIN 2, Tomaž POLAK
Chapter 8. Functions of Lipids. Structural Nature of Lipids. BCH 4053 Spring 2001 Chapter 8 Lecture Notes. Slide 1. Slide 2.
 BCH 4053 Spring 2001 Chapter 8 Lecture Notes 1 Chapter 8 Lipids 2 Functions of Lipids Energy Storage Thermal Insulation Structural Components of Membranes Protective Coatings of Plants and Insects Hormonal
BCH 4053 Spring 2001 Chapter 8 Lecture Notes 1 Chapter 8 Lipids 2 Functions of Lipids Energy Storage Thermal Insulation Structural Components of Membranes Protective Coatings of Plants and Insects Hormonal
Lipids and Membranes
 Lipids and Membranes Presented by Dr. Mohammad Saadeh The requirements for the Pharmaceutical Biochemistry I Philadelphia University Faculty of pharmacy Lipids and Membranes I. overview Lipids are related
Lipids and Membranes Presented by Dr. Mohammad Saadeh The requirements for the Pharmaceutical Biochemistry I Philadelphia University Faculty of pharmacy Lipids and Membranes I. overview Lipids are related
Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases
 Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases Avtor / Author Emina Hajdinjak 1, Andrej Markota 2, Alenka Strdin Košir 2, Simona Kirbiš 2,3
Prikaz dveh primerov zastrupitve z ogljikovim monoksidom Carbon monoxide intoxication: A report of two cases Avtor / Author Emina Hajdinjak 1, Andrej Markota 2, Alenka Strdin Košir 2, Simona Kirbiš 2,3
Antikoagulantno zdravljenje
 Antikoagulantno zdravljenje (novosti s kongresa ASH 2010) Irena Umek Bricman Oddelek za interno medicino SB Slovenj Gradec Podčetrtek, 15.04.2010 Trajanje antikoagulantne terapije Priporočila: 8th ACCP
Antikoagulantno zdravljenje (novosti s kongresa ASH 2010) Irena Umek Bricman Oddelek za interno medicino SB Slovenj Gradec Podčetrtek, 15.04.2010 Trajanje antikoagulantne terapije Priporočila: 8th ACCP
Lipids. OpenStax College
 OpenStax-CNX module: m44401 1 Lipids OpenStax College This work is produced by OpenStax-CNX and licensed under the Creative Commons Attribution License 3.0 By the end of this section, you will be able
OpenStax-CNX module: m44401 1 Lipids OpenStax College This work is produced by OpenStax-CNX and licensed under the Creative Commons Attribution License 3.0 By the end of this section, you will be able
FATTY ACID PROFILING BY GAS CHROMATOGRAPHY FOR THE SHERLOCK MIS
 FATTY ACID PROFILING BY GAS CHROMATOGRAPHY FOR THE SHERLOCK MIS Traditional gas chromatography of complex mixtures of compounds requires precision on the part of the chromatography equipment and considerable
FATTY ACID PROFILING BY GAS CHROMATOGRAPHY FOR THE SHERLOCK MIS Traditional gas chromatography of complex mixtures of compounds requires precision on the part of the chromatography equipment and considerable
ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE?
 ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE? SPECIALIZACIJA IZ DRUŽINSKE MEDICINE MODUL: NA DOKAZIH TEMELJEČA MEDICINA 16. SKUPINA AVTORJI: MIRJANA NINKOV MILA MRŠIĆ OLIVER ILIĆ OPIS
ALI SO PRIPRAVKI GLUKOZAMINA UČINKOVITI V TERAPIJI GONARTROZE? SPECIALIZACIJA IZ DRUŽINSKE MEDICINE MODUL: NA DOKAZIH TEMELJEČA MEDICINA 16. SKUPINA AVTORJI: MIRJANA NINKOV MILA MRŠIĆ OLIVER ILIĆ OPIS
MASS SPECTROMETRY STRATEGIES FOR COMPREHENSIVE LIPIDOME ANALYSIS OF COLORECTAL CANCER CELLS AND THEIR SECRETED EXOSOMES. Cassie J.
 MASS SPECTROMETRY STRATEGIES FOR COMPREHENSIVE LIPIDOME ANALYSIS OF COLORECTAL CANCER CELLS AND THEIR SECRETED EXOSOMES By Cassie J. Fhaner A DISSERTATION Submitted to Michigan State University in partial
MASS SPECTROMETRY STRATEGIES FOR COMPREHENSIVE LIPIDOME ANALYSIS OF COLORECTAL CANCER CELLS AND THEIR SECRETED EXOSOMES By Cassie J. Fhaner A DISSERTATION Submitted to Michigan State University in partial
Optimising. membranes
 Optimising Neuronal membranes Lipids are classified as 1. Simple lipids oils and fats 2. Complex lipids a) Phospholipids b) Glycosphingolipids containing a fatty acid, sphingosine and a CHO c) Lipoproteins
Optimising Neuronal membranes Lipids are classified as 1. Simple lipids oils and fats 2. Complex lipids a) Phospholipids b) Glycosphingolipids containing a fatty acid, sphingosine and a CHO c) Lipoproteins
Dr. Nafith Abu Tarboush
 4 Dr. Nafith Abu Tarboush June 24 th 2013 Ahmad Moayd 1 Definition and general properties refer to slide no. 2 Lipids: macromolecules made from Alcohol and Fatty acid bonded by ester linkage. Amphipathic
4 Dr. Nafith Abu Tarboush June 24 th 2013 Ahmad Moayd 1 Definition and general properties refer to slide no. 2 Lipids: macromolecules made from Alcohol and Fatty acid bonded by ester linkage. Amphipathic
GUTS Lecture Syllabus for Lipid Structure and Nomenclature
 GUTS Lecture Syllabus for Lipid Structure and Nomenclature For Questions or Assistance contact: Dr. Gwen Sancar, gsancar@ad.unc.edu Learning bjectives After completing the GUTS lecture and associated self-
GUTS Lecture Syllabus for Lipid Structure and Nomenclature For Questions or Assistance contact: Dr. Gwen Sancar, gsancar@ad.unc.edu Learning bjectives After completing the GUTS lecture and associated self-
