ELIQUIS. (apixaban) Príručka určená na predpisovanie
|
|
|
- Ashlynn McCoy
- 5 years ago
- Views:
Transcription
1 Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia. (apixaban) Príručka určená na predpisovanie Táto Príručka určená na predpisovanie nenahrádza Súhrn charakteristických vlastností lieku (SPC) ELIQUIS-u. Úplnú informáciu týkajúcu sa predpisovania lieku nájdete v SPC. Tento vzdelávací materiál sa poskytuje na ďalšiu minimalizáciu rizika krvácania a na usmernenie lekárov pri zvládaní tohto rizika. DÁTUM SCHVÁLENIA: júl 2018
2 Obsah Bezpečnostná karta pacienta... 3 Terapeutická indikácia: Prevencia mozgovej príhody a systémovej embólie u dospelých pacientov s nevalvulárnou fibriláciou predsiení (NVAF) s jedným alebo viacerými rizikovými faktormi Odporúčania pre dávkovanie... 4 Zníženie dávky... 4 Vynechanie dávky... 5 Pacienti s poruchou funkcie obličiek... 5 Pacienti s poruchou funkcie pečene... 6 Pacienti podstupujúci kardioverziu... 6 Pacienti s protetickými srdcovými chlopňami... 6 Terapeutická indikácia: Liečba hlbokej venóznej trombózy (DVT) a pľúcnej embólie (PE) a prevencia rekurentnej DVT a PE u dospelých Odporúčania pre dávkovanie... 7 Vynechanie dávky... 8 Pacienti s poruchou funkcie obličiek Pacienti s poruchou funkcie pečene Hemodynamicky nestabilní pacienti s PE alebo pacienti, u ktorých sa vyžaduje trombolýza alebo pľúcna embolektómia... 9 Pacienti s aktívnou formou rakoviny... 9 Terapeutická indikácia: Prevencia venóznych tromboembolických príhod (VTE) u dospelých pacientov, ktorí absolvovali elektívny chirurgický výkon na nahradenie bedrového alebo kolenného kĺbu Odporúčania pre dávkovanie...10 Vynechanie dávky Pacienti s poruchou funkcie obličiek Pacienti s poruchou funkcie pečene Zmena liečby na alebo z ELIQUIS-u Populácie s potenciálne vysokým rizikom krvácania Chirurgický zákrok a invazívne procedúry Dočasné prerušenie liečby Spinálna/epidurálna anestézia alebo punkcia Zvládnutie predávkovania a krvácania Použitie koagulačných testov Literatúra Dôležité kontaktné údaje Bezpečnostná karta pacienta Každému pacientovi, ktorému je predpísaný 2,5 mg alebo 5 mg, musí byť poskytnutá bezpečnostná karta pacienta a má byť vysvetlená dôležitosť a dôsledky antikoagulačnej liečby. Bezpečnostná karta pacienta je súčasťou balenia ELIQUIS-u 2,5 mg a 5 mg spolu s písomnou informáciou pre používateľa. Predpisujúci lekár sa má s pacientami porozprávať najmä o dôležitosti dodržiavania liečby, prejavoch alebo príznakoch krvácania a o tom, kedy vyhľadať lekársku pomoc. Táto bezpečnostná karta pacienta poskytuje lekárom, stomatológom a lekárnikom informácie o antikoagulačnej liečbe a obsahuje dôležité kontaktné údaje pre naliehavé prípady. Pacientom treba odporučiť, aby bezpečnostnú kartu pacienta nosili vždy so sebou a aby ju ukázali každému lekárovi aj lekárnikovi. Taktiež treba pacientom pripomenúť potrebu informovať lekárov o tom, že užívajú, ak sa u nich vyžaduje chirurgický alebo invazívny zákrok. 2 3
3 Terapeutická indikácia: Prevencia mozgovej príhody a systémovej embólie u dospelých pacientov s nevalvulárnou fibriláciou predsiení (non-valvular atrial fibrillation NVAF) s jedným alebo viacerými rizikovými faktormi 1, 2 Obrázok 2 Vek 80 rokov Kritériá pre dávku ELIQUIS-u 2,5 mg Rizikové faktory cievnej mozgovej príhody pri NVAF zahŕňajú prekonanú cievnu mozgovú príhodu alebo tranzitórny ischemický atak, vek 75 rokov, hypertenziu, diabetes mellitus a symptomatické srdcové zlyhanie (NYHA trieda II). Odporúčania pre dávkovanie Odporúčaná dávka ELIQUIS-u je 5 mg užívaná perorálne s vodou, jedlom alebo bez jedla. Liečba má pokračovať dlhodobo (obrázok 1). Obrázok 1 Pacienti, ktorí nedokážu prehltnúť celé tablety, môžu tablety ELIQUIS-u rozdrviť a rozpustiť vo vode, v 5 % roztoku glukózy alebo v jablkovom džúse alebo rozmiešať s jablkovým pyré a ihneď požiť. Alternatívne sa tablety ELIQUIS-u môžu rozdrviť a rozpustiť v 60 ml vody alebo v 5 % roztoku glukózy a ihneď podať cez nazogastrickú sondu. Rozdrvené tablety ELIQUIS-u sú stabilné vo vode, v 5 % roztoku glukózy, v jablkovom džúse a jablkovom pyré do 4 hodín. Zníženie dávky RÁNO VEČER U pacientov s minimálne dvomi nasledujúcimi charakteristikami: vek 80 rokov, telesná hmotnosť 60 kg alebo sérový kreatinín 1,5 mg/dl (133 μmol /l) je odporúčaná dávka ELIQUIS-u 2,5 mg užívaná perorálne (obrázok 2). Pacienti s preukázanými kritériami závažnej poruchy funkcie obličiek (klírens kreatinínu [CrCl] ml/min) majú tiež dostať 2,5 mg (obrázok 2). Telesná hmotnosť 60 kg Sérový kreatinín 1,5 mg/dl (133 µmol/l) Závažná porucha funkcie obličiek osamote (CrCl ml/min) Vynechanie dávky Ak sa vynechá dávka, pacient má ihneď užiť, a potom pokračovať v užívaní dvakrát denne ako predtým. Pacienti s poruchou funkcie obličiek Porucha funkcie obličiek Dialýza Zlyhanie obličiek (CrCl <15 ml/min) Závažná porucha funkcie obličiek (CrCl ml/min) Ľahká (CrCl ml/min) alebo stredne ťažká (CrCl ml/min) porucha funkcie obličiek Minimálne 2 charakteristiky 2 x 2,5 mg 2 x 2,5 mg Zníženie dávky na 2,5 mg 5 mg. Nie je potrebná úprava dávky pokiaľ pacient nespĺňa ďalšie kritériá pre zníženie dávky na 2,5 mg na základe veku, telesnej hmotnosti a/alebo sérového kreatinínu (pozri časť dávkovanie). 4 5
4 Pacienti s poruchou funkcie pečene Porucha funkcie pečene Ochorenie pečene spojené s rizikom koagulopatie a klinicky významného krvácania Ťažká porucha funkcie pečene Ľahká alebo stredne ťažká porucha funkcie pečene (Childovo - Pughovo skóre A alebo B) Kontraindikované Používať s opatrnosťou Nie je potrebná úprava dávky Pacienti so zvýšenou hladinou pečeňových enzýmov alanínaminotransferázy (ALT) /aspartátaminotransferázy (AST) > 2 x ULN, (ULN - upper limit of normal = horná hranica referenčného rozpätia) alebo celkového bilirubínu 1,5 x ULN boli vylúčení z klinických skúšaní. Preto sa má v tejto populácii používať s opatrnosťou. Pred začatím liečby ELIQUIS-om sa má uskutočniť vyšetrenie funkcie pečene. Pacienti podstupujúci kardioverziu sa môže začať užívať alebo sa v jeho užívaní môže pokračovať u pacientov s nevalvulárnou fibriláciou predsiení (NVAF-non-valvular atrial fibrillation), ktorí môžu vyžadovať kardioverziu. Stav pacienta Pacienti, ktorí predtým neužívali antikoagulačnú liečbu Pri nedostatku času užiť 5 dávok ELIQUIS-u pred kardioveziou Pacienti kvalifikovaní na Dávka zníženie dávky? Nie Pred kardioverziou podať najmenej 5 dávok ELIQUIS-u 5 mg Áno Pred kardioverziou podať najmenej 5 dávok ELIQUIS-u 2,5 mg Nie Áno Najmenej 2 hodiny pred kardioverziou podať 10 mg nasycovaciu dávku a po nej 5 mg Najmenej 2 hodiny pred kardioverziou podať 5 mg nasycovaciu dávku a po nej 2,5 mg Pred kardioverziou sa musí overiť, či pacient užíval podľa predpisu. Pacienti s protetickými srdcovými chlopňami Bezpečnosť a účinnosť ELIQUIS-u sa neskúmali u pacientov s protetickými srdcovými chlopňami s atriálnou fibriláciou alebo bez nej. Z tohto dôvodu sa u týchto pacientov použitie ELIQUIS-u neodporúča. Terapeutická indikácia: Liečba hlbokej venóznej trombózy (DVT) a pľúcnej embólie (PE) a prevencia rekurentnej DVT a PE u dospelých 1, 2 Odporúčania pre dávkovanie Odporúčaná dávka ELIQUIS-u pri liečbe akútnej DVT a liečbe PE je 10 mg ELIQUIS-u užívaných perorálne počas prvých 7 dní, po ktorej nasleduje 5 mg užívaných perorálne s vodou, jedlom alebo bez jedla. Na základe dostupných lekárskych odporúčaní sa má krátke trvanie liečby (minimálne 3 mesiace) zakladať na prítomnosti dočasných rizikových faktorov (napr. chirurgický zákrok v nedávnej minulosti, trauma, imobilizácia). Odporúčaná dávka ELIQUIS-u na prevenciu rekurentnej DVT a PE je 2,5 mg ELIQUIS-u užívaných perorálne s vodou, jedlom alebo bez jedla. Ak sa indikuje na prevenciu rekurentnej DVT a PE, dávka 2,5 mg sa má začať podávať po ukončení 6-mesačnej liečby ELIQUIS-om dávkou 5 mg alebo inou antikoagulačnou liečbou, ako je to vyznačené na obrázku 3 a v tabuľke 1. Obrázok 3 Liečba akútnej DVT alebo PE (minimálne 3 mesiace) deň 10 mg od 8. dňa 5 mg Prevencia rekurentnej DVT a/alebo PE po ukončení 6-mesačnej antikoagulačnej liečby 2,5 mg DÁVKA RÁNO VEČER 2,5 mg 2,5 mg MAXIMÁLNA DENNÁ DÁVKA 20 mg 10 mg 5 mg 6 7
5 Tabuľka 1 Liečba DVT alebo PE (minimálne 3 mesiace) Prevencia rekurentnej DVT a/ alebo PE po ukončení 6-mesačnej antikoagulačnej liečby DVT alebo PE Dĺžka trvania celkovej liečby má byť individuálne nastavená po starostlivom zhodnotení prínosu liečby oproti riziku krvácania. Pacienti, ktorí nedokážu prehltnúť celé tablety, môžu tablety ELIQUIS-u rozdrviť a rozpustiť vo vode, v 5 % roztoku glukózy alebo v jablkovom džúse alebo rozmiešať s jablkovým pyré a ihneď požiť. Alternatívne sa tablety ELIQUIS-u môžu rozdrviť a rozpustiť v 60 ml vody alebo v 5 % roztoku glukózy a ihneď podať cez nazogastrickú sondu. Rozdrvené tablety ELIQUIS-u sú stabilné vo vode, v 5 % roztoku glukózy, v jablkovom džúse a jablkovom pyré do 4 hodín. Vynechanie dávky Ak sa vynechá dávka, pacient má ihneď užiť, a potom pokračovať v užívaní dvakrát denne ako predtým. Pacienti s poruchou funkcie obličiek Dávkovací režim 10 mg počas prvých 7 dní po ktorých nasleduje 5 mg Maximálna denná dávka 20 mg 10 mg 2,5 mg 5 mg Pacienti s poruchou funkcie pečene Porucha funkcie pečene Ochorenie pečene spojené s rizikom koagulopatie a klinicky významného krvácania Ťažká porucha funkcie pečene Ľahká alebo stredne ťažká porucha funkcie pečene (Childovo Pughovo skóre A alebo B) Kontraindikované Používať s opatrnosťou Nie je potrebná úprava dávky Pacienti so zvýšenou hladinou pečeňových enzýmov ALT/AST > 2 x ULN alebo celkového bilirubínu 1,5 x ULN boli vylúčení z klinických skúšaní. Preto sa má v tejto populácii používať s opatrnosťou. Pred začatím liečby ELIQUIS-om sa má uskutočniť vyšetrenie funkcie pečene. Hemodynamicky nestabilní pacienti s PE alebo pacienti, u ktorých sa vyžaduje trombolýza alebo pľúcna embolektómia sa neodporúča ako alternatíva k nefrakcionovanému heparínu u pacientov s PE, ktorí sú hemodynamicky nestabilní alebo môžu podstúpiť trombolýzu alebo pľúcnu embolektómiu. Pacienti s aktívnou formou rakoviny Účinnosť a bezpečnosť lieku pri liečbe DVT, liečbe PE a na prevenciu rekurentnej DVT a PE u pacientov s aktívnou formou rakoviny neboli stanovené. Porucha funkcie obličiek Dialýza Zlyhanie obličiek (CrCl <15 ml/min) Závažná porucha funkcie obličiek (CrCl ml/min) Ľahká (CrCl ml/min) alebo stredne ťažká (CrCl ml/min) porucha funkcie obličiek Používať s opatrnosťou Žiadna úprava dávky 8 9
6 Terapeutická indikácia: Prevencia venóznych tromboembolických príhod (VTE) u dospelých pacientov, ktorí absolvovali elektívny chirurgický výkon na nahradenie bedrového alebo kolenného kĺbu 1 Pacienti s poruchou funkcie pečene Poškodenie funkcie pečene Ochorenie pečene spojené s rizikom koagulopatie a klinicky významného krvácania Kontraindikované Odporúčania pre dávkovanie Odporúčaná dávka ELIQUIS-u je 2,5 mg užívaná perorálne s vodou, jedlom alebo bez jedla. Začiatočná dávka sa má užiť 12 až 24 hodín po chirurgickom výkone. Pri rozhodovaní o vhodnom čase podania v rámci uvedeného časového intervalu môžu lekári zvážiť potenciálne prínosy skoršej antikoagulačnej liečby na profylaxiu VTE, ako aj riziko pooperačného krvácania. U pacientov, ktorí absolvovali chirurgický výkon na nahradenie bedrového kĺbu je odporúčaná dĺžka liečby 32 až 38 dní. U pacientov, ktorí absolvovali chirurgický výkon na nahradenie kolenného kĺbu je odporúčaná dĺžka liečby 10 až 14 dní. Pacienti, ktorí nedokážu prehltnúť celé tablety, môžu tablety ELIQUIS-u rozdrviť a rozpustiť vo vode, v 5 % roztoku glukózy alebo v jablkovom džúse alebo rozmiešať v jablkovom pyré a ihneď požiť. Alternatívne sa tablety ELIQUIS-u môžu rozdrviť a rozpustiť v 60 ml vody alebo v 5 % roztoku glukózy a ihneď podať cez nazogastrickú sondu. Rozdrvené tablety ELIQUIS-u sú stabilné vo vode, v 5 % roztoku glukózy, v jablkovom džúse a jablkovom pyré do 4 hodín. Vynechanie dávky Ak sa vynechá dávka, pacient má ihneď užiť, a potom pokračovať v užívaní dvakrát denne ako predtým. Ťažká porucha funkcie pečene Ľahká alebo stredne ťažká porucha funkcie pečene (Childovo Pughovo skóre A alebo B) Používať s opatrnosťou Nie je potrebná úprava dávky Pacienti so zvýšenou hladinou pečeňových enzýmov ALT/AST > 2 x ULN alebo celkového bilirubínu 1,5 x ULN boli vylúčení z klinických skúšaní. Preto sa má v tejto populácii používať s opatrnosťou. Pred začatím liečby ELIQUIS-om sa má uskutočniť vyšetrenie funkcie pečene. Zmena liečby na alebo z ELIQUIS-u 1, 2 Zmena liečby z parenterálnych antikoagulancií na (a naopak) sa môže uskutočniť pri ďalšej plánovanej dávke. Tieto liečivá sa nemajú podávať súbežne. Zmena liečby z antagonistu vitamínu K (VKA) na Pri zmene liečby z antagonistu vitamínu K (VKA) na prerušte liečbu warfarínom alebo inú liečbu VKA a liečbu liekom začnite vtedy, keď medzinárodný normalizovaný index (INR) je < 2,0 (obrázok 4). Obrázok 4 Prerušte liečbu warfarínom alebo inú liečbu VKA Pacienti s poruchou funkcie obličiek Poškodenie funkcie obličiek Sledujte INR v pravidelných intervaloch kým INR je < 2,0 Dialýza Zlyhanie obličiek (CrCl <15 ml/min) Ťažká porucha funkcie obličiek (CrCl ml/min) Ľahká (CrCl ml/min) alebo stredne ťažká (CrCl ml/min) porucha funkcie obličiek Používať s opatrnosťou Nie je potrebná úprava dávky Začnite podávať Zmena liečby z ELIQUIS-u na liečbu VKA Pri zmene liečby z ELIQUIS-u na liečbu VKA pokračujte v podávaní ELIQUIS-u minimálne 2 dni po začatí liečby VKA. Po 2 dňoch súčasného podávania ELIQUIS-u s liečbou VKA, vyšetrite INR pred ďalšou plánovanou dávkou ELIQUIS-u. Pokračujte v súčasnom podávaní ELIQUIS-u a liečby VKA, dokiaľ nedosiahnete hodnotu INR 2,
7 Populácie s potenciálne vysokým rizikom krvácania 1, 2 Niektoré podskupiny pacientov sú vystavené zvýšenému riziku krvácania a majú sa starostlivo sledovať pre znaky a príznaky krvácavých komplikácií. sa má používať opatrne za podmienok zvýšeného rizika krvácania. Podávanie ELIQUIS-u sa má prerušiť, ak sa objaví závažné krvácanie. Lézia alebo ochorenie považujúce sa za významný rizikový faktor závažného krvácania To zahřňa: Aktívne klinicky významné krvácanie Ochorenie pečene spojené s rizikom koagulopatie a klinicky významného krvácania Súčasná alebo nedávna gastrointestinálna ulcerácia Prítomnosť malígnych novotvarov s vysokým rizikom krvácania Nedávne poranenie mozgu alebo chrbtice Nedávny chirurgický zákrok na mozgu, mieche alebo očiach Nedávna intrakraniálna hemorágia Známe alebo suspektné ezofagálne varixy, artériovenózne malformácie, vaskulárne aneuryzmy alebo významné intraspinálne alebo intracerebrálne vaskulárne abnormality Interakcie s inými liekmi ovplyvňujúcimi hemostázu Antikoagulanciá Nefrakcionovaný heparín, heparíny s nízkou molekulárnou hmotnosťou (napr. enoxaparín), deriváty heparínu (napr. fondaparín) Perorálne antikoagulanciá (napr. warfarín, rivaroxaban, dabigatran) Inhibítory agregácie krvných doštičiek, SSRI/SNRI a NSAID Selektívne inhibítory spätného vychytávania sérotonínu (SSRI) alebo inhibítory spätného vychytávania sérotonínu a noradrenalínu (SNRI) Kyselina acetylsalicylová (ASA) Nesteroidné antiflogistiká (NSAID) Podmienky, za ktorých je kontraindikovaný Súbežná liečba ELIQUIS-om a akoukoľvek inou antikoagulačnou látkou je kontraindikovaná, s výnimkou špecifických okolností pri zmene antikoagulačnej liečby, alebo keď sa nefrakcionovaný heparín podáva v dávkach potrebných na udržanie permanentného centrálneho žilového alebo arteriálneho katétra Súbežné používanie ELIQUIS-u s protidoštičkovými liečivami zvyšuje riziko krvácania Opatrnosť je nutná, ak sú pacienti súbežne liečení s SSRI/SNRI alebo NSAID vrátane ASA Lieky spájané s ťažkým krvácaním sa neodporúčajú užívať súbežne s ELIQUIS-om : trombolytiká, antagonisty receptora GPIIb/IIIa, tienopyridíny (napr. klopidogrel), dipyridamol, dextrán a sulfinpyrazón. Faktory, ktoré môžu zvyšovať expozíciu ELIQUIS-u /zvyšovať plazmatické hladiny ELIQUIS-u Porucha funkcie obličiek Starší pacienti Nízka telesná hmotnosť 60 kg Súbežné použitie so silnými inhibítormi CYP3A4 aj P-gp Súbežné použitie s menej silnými inhibítormi CYP3A4 a/alebo P-gp Pozri časti o pacientoch s poruchou funkcie obličiek pod odporúčaniami pre dávkovanie pri každej separátnej indikácii Používanie sa neodporúča u pacientov s CrCl <15 ml/min alebo u pacientov podstupujúcich dialýzu U pacientov s ľahkou alebo stredne ťažkou poruchou funkcie obličiek nie je potrebná úprava dávky Pacienti s NVAF Pacienti s ťažkou poruchou funkcie obličiek (CrCl ml/min) majú dostávať nižšiu dávku ELIQUIS-u 2,5 mg Pacienti so sérovou hladinou kreatinínu 1,5 mg/dl (133 mikromol/l) súvisiacou s vekom 80 rokov alebo telesnou hmotnosťou 60 kg majú dostávať nižšiu dávku ELIQUIS-u 2,5 mg Nie je potrebná úprava dávky Pacienti s NVAF Nie je potrebná úprava dávky s výnimkou kombinácie s inými faktormi Nie je potrebná úprava dávky Pacienti s NVAF Nie je potrebná úprava dávky s výnimkou kombinácie s inými faktormi Použitie ELIQUIS-u sa neodporúča u pacientov súbežne užívajúcich systémovú liečbu azolovými antimykotikami (napr. ketokonazol, itrakonazol, vorikonazol, pozakonazol) a inhibítormi HIV proteáz (napr. ritonavir) Úprava dávky ELIQUIS-u sa nevyžaduje pri súbežnom podávaní s napr. diltiazemom, naproxénom, amiodaronom, verapamilom a chinidínom 12 13
8 Faktory, ktoré môžu znižovať expozíciu ELIQUIS-u /znižovať plazmatické hladiny ELIQUIS-u Súbežné použitie so silnými induktormi CYP3A4 a P-gp Súbežné použitie ELIQUIS-u so silnými induktormi CYP3A4 a P-gp* (napr. rifampicín, fenytoín, karbamazepín, fenobarbital alebo ľubovník bodkovaný) môže viesť k ~ 50 % zníženiu expozície ELIQUIS-u a má sa používať s opatrnosťou. Liečba DVT alebo PE sa neodporúča Stredné alebo vysoké riziko krvácania (zahŕňa zákroky, pre ktoré nemožno vylúčiť pravdepodobnosť klinicky významného krvácania alebo pre ktoré by bolo riziko krvácania neprípustné) Dočasné prerušenie liečby 1, 2 Najmenej 48 hodín pred elektívnym chirurgickým zákrokom alebo invazívnymi procedúrami (> 4 polčasy) *P - glykoproteín 1, 2, 3 Chirurgický zákrok a invazívne procedúry sa má vysadiť pred elektívnym chirurgickým zákrokom alebo invazívnymi procedúrami s rizikom krvácania (pozri tabuľku nižšie). Ak chirurgický zákrok alebo invazívne procedúry nie je možné odložiť, je potrebná primeraná opatrnosť s prihliadnutím na zvýšené riziko krvácania. Toto riziko krvácania sa má zvážiť oproti naliehavosti zákroku. Hoci liečba ELIQUIS-om nevyžaduje pravidelné monitorovanie expozície, kalibrovaný kvantitatívny test na aktivitu anti-faktora Xa môže byť užitočný vo výnimočných situáciách, kedy znalosť expozície ELIQUIS-u môže pomôcť kvalifikovanému klinickému rozhodnutiu, napr. predávkovanie a urgentný chirurgický výkon (pozri časť o používaní koagulačných testov). V prípade, že pacient liečený ELIQUIS-om vyžaduje elektívny zákrok, ako je chirurgický alebo invazívny zákrok spojený so zvýšeným rizikom krvácania, sa má vysadiť dostatočnú dobu pred zákrokom na zníženie rizika krvácania súvisiaceho s antikoaguláciou. Eliminačný polčas ELIQUIS-u je približne 12 hodín. Vzhľadom na to, že je reverzibilný inhibítor FXa, jeho antikoagulačná aktivita odoznie v rámci 24 až 48 hodín po poslednej podanej dávke. Vysadenie ELIQUIS-u pred elektívnym chirurgickým zákrokom Nízke riziko krvácania (procedúry, pri ktorých bude krvácanie, ak sa vyskytne, minimálne, nekritické vzhľadom na miesto výskytu a/alebo ľahko zvládnuteľné jednoduchou mechanickou hemostázou) Najmenej 24 hodín pred elektívnym chirurgickým zákrokom alebo invazívnymi procedúrami Prerušenie podávania antikoagulancií, vrátane ELIQUIS-u, pre aktívne krvácanie, elektívny chirurgický zákrok alebo invazívne procedúry, vystavuje pacientov zvýšenému riziku trombózy. Prerušeniam liečby sa má zabrániť a ak sa musí z akéhokoľvek dôvodu antikoagulácia liekom dočasne prerušiť, liečba sa má čo najskôr znovu nasadiť za podmienok, že klinická situácia umožňuje zaistenie primeranej hemostázy. Spinálna/epidurálna anestézia alebo punkcia 1 Pri použití neuraxiálnej anestézie (spinálna/epidurálna anestézia) alebo spinálnej/epidurálnej punkcie sú pacienti liečení antitrombotikami na prevenciu trombembolických komplikácií vystavení riziku epidurálneho alebo spinálneho hematómu, čo môže viesť k dlhodobej alebo permanentnej paralýze. Postoperačne zavedené epidurálne alebo intratekálne katétre sa musia odstrániť minimálne 5 hodín pred prvou dávkou ELIQUIS-u. Usmernenie týkajúce sa používania ELIQUIS-u u pacientov so zavedeným intratekálnymi a epidurálnymi katétrami Neexistujú žiadne klinické skúsenosti s používaním ELIQUIS-u spolu so zavedenými intratekálnymi alebo epidurálnymi katétrami. V prípade takejto potreby a vychádzajúc z farmakokinetických údajov ELIQUIS-u, musí uplynúť interval hodín (t. j. 2 x biologický polčas) medzi poslednou dávkou ELIQUIS-u a odstránením katétra a minimálne jedna dávka sa má vynechať pred odstránením katétra. Nasledujúca dávka ELIQUIS-u sa môže podať minimálne 5 hodín po odstránení katétra. Tak ako u všetkých nových antikoagulancií sú skúsenosti s neuraxiálnou blokádou obmedzené a preto sa odporúča veľká opatrnosť pri používaní ELIQUIS-u za prítomnosti neuraxiálnej blokády (pozri obrázok 5). U pacientov je nutné často sledovať znaky a príznaky neurologického poškodenia (napr. necitlivosť alebo slabosť nôh, dysfunkcia čriev alebo močového mechúra). Ak sa zaznamená neurologická porucha, je nevyhnutná urgentná diagnostika a liečba
9 Obrázok 5 Posledná tableta pred odstránením epidurálneho/intratekálneho katétra Počkajte hodín Odstráňte katéter preukázané zmenami v teste na tvorbu trombínu bolo zrejmé na konci infúzie a začiatočné hodnoty boli dosiahnuté v priebehu 4 hodín po začatí 30 minútovej infúzie 4-faktorového PCC u zdravých jedincov. Nie sú však žiadne klinické skúsenosti s použitím 4-faktorových PCCs na zastavenie krvácania u jednotlivcov, ktorí dostali. V súčasnosti nie sú žiadne skúsenosti s použitím rekombinantného faktora VIIa u jedincov užívajúcich. Môže sa zvážiť opätovné dávkovanie rekombinantného faktora VIIa a titrovať ho v závislosti od zlepšenia krvácania. V závislosti na lokálnej dostupnosti sa v prípade rozsiahleho krvácania môže zvážiť konzultácia experta na koaguláciu. Hemodialýza znížila AUC o 14 % u pacientov s terminálnym štádiom ochorenia obličiek, keď sa podávala jednorazová dávka ELIQUIS-u 5 mg perorálne. Preto je nepravdepodobné, že by hemodialýza bola účinným prostriedkom pri liečbe predávkovania ELIQUIS-om. Počkajte 5 hodín Prvá tableta po odstránení katétra Použitie koagulačných testov 1, 2 Liečba ELIQUIS-om nevyžaduje pravidelné monitorovanie expozície. Kalibrovaný kvantitatívny test na anti-fxa aktivitu môže byť užitočný vo výnimočných situáciách, kedy znalosť expozície ELIQUIS-u môže pomôcť kvalifikovanému klinickému rozhodnutiu, napr. predávkovanie a urgentný chirurgický zákrok. Zvládnutie predávkovania a krvácania 1, 2 Proti ELIQUIS-u neexistuje antidotum. Predávkovanie ELIQUIS-om môže viesť k zvýšenému riziku krvácania. V prípade komplikácií spôsobených krvácaním sa musí liečba ukončiť a vyšetriť zdroj krvácania. Je potrebné zvážiť začatie vhodnej liečby, napr. chirurgickej hemostázy alebo transfúzie čerstvej zmrazenej plazmy. V kontrolovaných klinických skúšaniach sa u zdravých jedincov, ktorým sa podával perorálne v dávkach do 50 mg denne počas 3 až 7 dní (25 mg počas 7 dní alebo 50 mg jedenkrát denne počas 3 dní), neprejavili žiadne klinicky významné nežiaduce účinky. U zdravých osôb znížilo podanie aktívneho uhlia 2 a 6 hodín po požití 20 mg dávky ELIQUIS-u priemernú AUC o 50 % a 27 %, v uvedenom poradí, a nemalo žiadny vplyv na Cmax. Keď bolo aktívne uhlie podané 2 a 6 hodín po ELIQUIS-e, priemerný polčas klesol z 13,4 hodín, kedy sa podal samostatne, na 5,3 hodín a 4,9 hodín v uvedenom poradí. Podávanie aktívneho uhlia môže byť teda užitočné pri zvládaní predávkovania ELIQUIS-om alebo náhodného požitia. Ak sa život ohrozujúce krvácanie nedá zvládnuť pomocou opatrení uvedených vyššie, možno zvážiť podanie koncentrátov protrombínového komplexu (prothrombin complex concentrates, PCCs) alebo rekombinantného faktora VIIa. Zrušenie farmakodynamických účinkov ELIQUIS-u Protrombínový čas (PT), INR a aktivovaný parciálny tromboplastínový čas (aptt) Zmeny pozorované v týchto testoch zrážanlivosti v očakávaných terapeutických dávkach sú malé a podliehajú vysokému stupňu variability. Neodporúčajú sa na hodnotenie farmakodynamických účinkov ELIQUIS-u. V teste na tvorbu trombínu znížil potenciál endogénneho trombínu, mieru tvorby trombínu v ľudskej plazme. Hodnotenie anti-fxa Stupeň antikoagulačného účinku meraný aktivitou anti-fxa vykazuje blízky priamy lineárny vzťah s plazmatickou koncentráciou ELIQUIS-u. Údaje z klinických skúšaní sú dostupné len z chromogénneho testu Rotachrom Heparin a výsledky sú uvedené nižšie. Anti-FXa aktivita vykazuje blízky priamy lineárny vzťah s plazmatickou koncentráciou ELIQUIS-u, s maximálnymi hodnotami v čase maximálnych koncentrácií ELIQUIS-u v plazme. Vzťah medzi plazmatickými koncentráciami ELIQUIS-u a anti-fxa aktivitou je približne lineárny v širokom rozpätí dávkovania ELIQUIS-u. Tabuľka 2 zobrazuje očakávanú expozíciu v rovnovážnom stave a anti-faktorovú Xa aktivitu pre každú indikáciu. U pacientov užívajúcich na prevenciu VTE po náhrade bedrového alebo kolenného kĺbu výsledky ukazujú menej než 1,6-násobnú fluktuáciu od maximálnej k minimálnej úrovni. U pacientov s NVAF užívajúcich na prevenciu cievnej mozgovej 16 17
10 príhody a systémovej embólie výsledky ukazujú menej ako 1,7-násobnú fluktuáciu od maximálnej k minimálnej úrovni. U pacientov užívajúcich na liečbu DVT a PE alebo na prevenciu rekurentnej DVT a PE, výsledky ukazujú menej ako 2,2-násobnú fluktuáciu od maximálnej k minimálnej úrovni. Tabuľka 2 Očakávaná expozícia lieku v rovnovážnom stave a anti-faktorová Xa aktivita C max (ng/ml) C max (ng/ml) anti-fxa aktivita, max. (IU/ml) Medián [5., 95. percentil] anti-fxa aktivita, min. (IU/ml) Prevencia VTE: elektívny chirurgický výkon na nahradenie bedrového alebo kolenného kĺbu 2,5 mg 77 [41; 146] 51 [23; 109] 1,3 [0,67; 2,4] 0,84 [0,37; 1,8] Prevencia cievnej mozgovej príhody a systémovej embólie NVAF 2,5 mg * 123 [69; 221] 79 [34; 162] 1,8 [1,0; 3,3] 1,2 [0,51; 2,4] 5 mg 171 [91; 321] 103 [41; 230] 2,6 [1,4; 4,8] 1,5 [0,61; 3,4] Liečba DVT, liečba PE a prevencia rekurentnej DVT a PE 2,5 mg 5 mg 10 mg 67 [30; 153] 32 [11; 90] 1,0 [0,46; 2,5] 0,49 [0,17; 1,4] 132 [59; 302] 63 [22; 177] 2,1 [0,91; 5,2] 1,0 [0,33; 2,9] 251 [111; 572] 120 [41; 335] 4,2 [1,8; 10,8] 1,9 [0,64; 5,8] * Dávka upravená na základe minimálne 2 z 3 kritérií zníženia dávky, ako je uvedené na obrázku 2 Literatúra: 1. Bristol-Myers Squibb/Pfizer EEIG. 2,5 mg filmom obalené tablety Súhrn charakteristických vlastností lieku. 2. Bristol-Myers Squibb/Pfizer EEIG. filmom obalené tablety Súhrn charakteristických vlastností lieku. 3. Chirurgické a invazívne zákroky u pacientov dlhodobo liečených perorálnymi antikoagulanciami: inhibítory trombínu alebo faktora Xa. Odporúčania pracovnej skupiny pre perioperačnú hemostázu apracovnej skupiny pre trombózu a hemostázu z Francúzska. Archives of cardiovascular diseases 2011; 104: Kontaktné údaje oddelenia bezpečnosti spoločnosti Pfizer: Fax: SVK.AEReporting@pfizer.com Akékoľvek podozrenie na nežiaduci účinok a iné skutočnosti závažné pre zdravie liečených osôb je nutné hlásiť Štátnemu ústavu pre kontrolu liečiv. Hlásenie nežiaducich účinkov Ak sa u Vášho pacienta vyskytne akýkoľvek nežiaduci účinok, nahláste ho ihneď priamo na Štátny ústav pre kontrolu liečiv, Sekcia klinického skúšania liekov a farmakovigilancie, Kvetná 11, Bratislava 26, tel: , internetová stránka: neziaduce.ucinky@sukl.sk, webový formulár: alebo spoločnosti Pfizer na SVK.AEReporting@pfizer.com. Ak máte akékoľvek otázky alebo potrebujete viac informácií, kontaktujte spoločnosť Pfizer na telef. číslach , alebo použite fax alebo prostredníctvom internetovej stránky vaspfizer@pfizer.com. Príručku určenú na predpisovanie nájdete aj na internetovej stránke Štátneho ústavu pre kontrolu liečiv: slovenska-verzia/bezpecnost-liekov/edukacne-materialy?page_id=4795. Dátum schválenia: júl
11 SKRÁTENÁ INFORMÁCIA O LIEKU Eliquis 2,5 mg filmom obalené tablety, Eliquis 5,0 mg filmom obalené tablety Každá filmom obalená tableta obsahuje 2,5 mg alebo 5 mg apixabanu. Charakteristika: Apixaban je silný, perorálny, reverzibilný, priamy a vysoko selektívny inhibítor faktora Xa. Farmakoterapeutická skupina: Antitrombotiká, priamy inhibítor faktora Xa, ATC kód: B01AF02. Indikácie: Prevencia venóznych tromboembolických príhod (VTE) u dospelých pacientov, ktorí absolvovali elektívny chirurgický výkon na nahradenie bedrového alebo kolenného kĺbu*. Prevencia mozgovej príhody a systémovej embólie u dospelých pacientov s nevalvulárnou fibriláciou predsiení (NVAF) s jedným alebo viacerými rizikovými faktormi, ako napríklad prekonaná cievna mozgová príhoda alebo tranzitórny ischemický atak (TIA); vek 75 rokov; hypertenzia, diabetes mellitus; symptomatické srdcové zlyhanie (NYHA trieda II). Liečba hlbokej venóznej trombózy (DVT) a pľúcnej embólie (PE) a prevencia rekurentnej DVT a PE u dospelých. Dávkovanie: Prevencia VTE (VTEp): 2,5 mg apixabanu perorálne, dĺžka liečby 32 až 38 dní po náhrade bedrového kĺbu a 10 až 14 dní po náhrade kolenného kĺbu. Prevencia mozgovej príhody a systémovej embólie u pacientov s NVAF: odporúčaná dávka apixabanu je 5 mg perorálne. Zníženie dávky: u pacientov s NVAF a s minimálne dvoma nasledujúcimi charakteristikami: vek 80 rokov, telesná hmotnosť 60 kg alebo sérový kreatinín 1,5 mg/dl (133 mikromol/l) je odporúčaná dávka apixabanu 2,5 mg užívaná perorálne. Pacienti s klírensom kreatinínu ml/min majú dostať dávku apixabanu 2,5 mg, a liečba sa má používať s opatrnosťou. Liečba má pokračovať dlhodobo. U pacientov s klírensom kreatinínu < 15 ml/min alebo u dialyzovaných pacientov sa apixaban neodporúča. Liečba DVT, liečba PE a prevencia rekurentnej DVT a PE (VTEt): odporúčaná dávka apixabanu na liečbu akútnej DVT a liečbu PE je 10 mg užívaných perorálne počas prvých 7 dní, po ktorých nasleduje 5 mg užívaných perorálne, minimálne 3 mesiace. Odporúčaná dávka apixabanu na prevenciu rekurentnej DVT a PE je 2,5 mg užívaných perorálne. Ak sa indikuje na prevenciu rekurentnej DVT a PE, dávka 2,5 mg sa má začať podávať po ukončení 6-mesačnej liečby apixabanom dávkou 5 mg dvakrát denne alebo iným antikoagulantom. Zmena liečby z parenterálnych antikoagulancií na Eliquis (a naopak) sa môže uskutočniť pri ďalšej plánovanej dávke. Zmena liečby antagonistom vitamínu K (VKA) na Eliquis: Pri zmene liečby z antagonistu vitamínu K (VKA) na Eliquis sa má prerušiť liečba warfarínom alebo iná liečba VKA a liečba Eliquisom sa má začať vtedy, keď je medzinárodný normalizovaný index (INR) < 2. Zmena liečby z Eliquisu na liečbu VKA: Pri zmene liečby z Eliquisu na liečbu VKA sa má pokračovať v podávaní Eliquisu minimálne 2 dni po začatí liečby VKA. Po 2 dňoch súčasného podávania Eliquisu s liečbou VKA, sa má vyšetriť INR pred ďalšou plánovanou dávkou Eliquisu. Súčasné podávanie Eliquisu a liečby VKA má pokračovať, pokiaľ sa nedosiahne hodnota INR 2. Kardioverzia (NVAF): Pacienti môžu apixaban užívať aj počas kardioverzie. Kontraindikácie: Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok. Klinicky významné aktívne krvácanie. Ochorenie pečene spojené s koagulopatiou a klinicky významným rizikom krvácania. Lézia alebo ochorenie s významným rizikom závažného krvácania ako je súčasná alebo nedávna gastrointestinálna ulcerácia, prítomnosť malígnych novotvarov s vysokým rizikom krvácania, nedávne poranenie mozgu alebo chrbtice, nedávny chirurgický zákrok na mozgu, mieche alebo očiach, nedávna intrakraniálna hemorágia, známe alebo suspektné ezofagálne varixy, artériovenózne malformácie, vaskulárne aneuryzmy alebo významné intraspinálne alebo intracerebrálne vaskulárne abnormality. Súbežná liečba s akoukoľvek inou antikoagulačnou látkou, napr. nefrakcionovaným heparínom, s heparínmi s nízkou molekulárnou hmotnosťou, derivátmi heparínu, perorálnymi antikoagulanciami (warfarín, rivaroxaban, dabigatran atď.) s výnimkou okolností prechodu liečby na apixaban alebo z apixabanu, alebo keď sa UFH podáva v dávkach potrebných na udržanie permanentného centrálneho žilového alebo arteriálneho katétra. Osobitné upozornenia: Riziko krvácania: pri podávaní Eliquisu je potrebné pacientov pozorne sledovať pre príznaky krvácania. V prípadoch, kde je zvýšené riziko krvácania sa odporúča opatrnosť. Ak sa objaví závažné krvácanie, podávanie Eliquisu sa má prerušiť. Liečba apixabanom nevyžaduje pravidelné monitorovanie expozície. Z dôvodu zvýšeného rizika krvácania je súbežná liečba inými antikoagulanciami kontraindikovaná. Súbežné používanie Eliquisu s protidoštičkovými liečivami zvyšuje riziko krvácania. Opatrnosť je nutná, ak sú pacienti súbežne liečení nesteroidnými antiflogistikami (NSAIDs), vrátane kyseliny acetylsalicylovej. Hemodialýza nie je účinný prostriedok pri liečbe predávkovania apixabanom. Použitie Eliquisu sa neodporúča u pacientov s protetickými srdcovými chlopňami. Interakcie: Použitie Eliquisu sa neodporúča u pacientov, ktorým sa súbežne podáva systémová liečba silnými inhibítormi CYP3A4 a Pgp, ako azolové antimykotiká a inhibítory HIV proteáz. Súbežné používanie apixabanu so silnými induktormi CYP3A4 a P-gp môže viesť k zníženiu plazmatických koncentrácií apixabanu, nevyžaduje sa úprava dávky apixabanu, avšak tieto lieky sa majú podávať s opatrnosťou. Antikoagulanciá, inhibítory agregácie trombocytov a NSAIDs: z dôvodu zvýšeného rizika krvácania je súbežná liečba inými antikoagulanciami kontraindikovaná. Po kombinovanom podaní enoxaparínu (v jednorazovej dávke 40 mg) s apixabanom (v jednorazovej dávke 5 mg) sa pozoroval aditívny účinok na aktivitu antifaktora Xa. Látky spájané s ťažkým krvácaním sa neodporúčajú užívať súbežne s Eliquisom: trombolytiká, antagonisty receptora GPIIb/IIIa, tienopyridíny (napr. klopidogrel), dipyridamol, dextrán a sulfinpyrazón. Gravidita a laktácia: užívať apixaban počas gravidity. Nežiaduce účinky: časté: anémia, epistaxa, kontúzia, hematúria, hematóm, krvácanie do oka, nauzea, rektálne, gingiválne a gastrointestinálne krvácanie. Uchovávanie: Tento liek nevyžaduje žiadne zvláštne podmienky na uchovávanie. Výdaj lieku je viazaný na lekársky predpis. Pred podaním lieku sa zoznámte s úplným znením Súhrnu charakteristických vlastností lieku (SPC). Dátum aktualizácie skrátenej informácie o lieku: Január Držiteľ rozhodnutia o registrácii: Bristol-Myers Squibb/Pfizer EEIG, Bristol-Myers Squibb House, Uxbridge Business Park, Sanderson Road,Uxbridge, Middlesex UB8 1DH, Veľká Británia. Miestne zastúpenie držiteľa rozhodnutia o registrácii: PFIZER Luxembourg SARL, o.z., tel.: Upravené podľa SPC schváleného agentúrou EMA: *týka sa iba Eliquisu 2,5 mg Dátum prípravy: September 2018 PFIZER Luxembourg SARL Pribinova 25, Bratislava, tel.: 02/ , fax: 02/ ,
Apixaban nové perorálne antikoagulancium
 27 Apixaban nové perorálne antikoagulancium MUDr. Zuzana Jedináková, doc. MUDr. Ján Staško, PhD., mim. prof., prof. MUDr. Peter Kubisz, DrSc. Národné centrum hemostázy a trombózy, Klinika hematológie a
27 Apixaban nové perorálne antikoagulancium MUDr. Zuzana Jedináková, doc. MUDr. Ján Staško, PhD., mim. prof., prof. MUDr. Peter Kubisz, DrSc. Národné centrum hemostázy a trombózy, Klinika hematológie a
XVII. SLOVENSKÝ GERIATRICKÝ KONGRES
 Slovenská gerontologická a geriatrická spoločnosť Univerzitná nemocnica s poliklinikou Milosrdní bratia, Bratislava usporiadajú XVII. SLOVENSKÝ GERIATRICKÝ KONGRES s medzinárodnou účasťou a 44. GRESSNEROVE
Slovenská gerontologická a geriatrická spoločnosť Univerzitná nemocnica s poliklinikou Milosrdní bratia, Bratislava usporiadajú XVII. SLOVENSKÝ GERIATRICKÝ KONGRES s medzinárodnou účasťou a 44. GRESSNEROVE
Apixaban v tromboprofylaxii u pacientov s nevalvulárnou fibriláciou predsiení spoločné odporúčania odborných spoločností
 Apixaban v tromboprofylaxii u pacientov s nevalvulárnou fibriláciou predsiení spoločné odporúčania odborných spoločností Odborné spoločnosti Slovenskej lekárskej spoločnosti: 1 Slovenská spoločnosť pre
Apixaban v tromboprofylaxii u pacientov s nevalvulárnou fibriláciou predsiení spoločné odporúčania odborných spoločností Odborné spoločnosti Slovenskej lekárskej spoločnosti: 1 Slovenská spoločnosť pre
Scylla a Charibdis: riziká
 Scylla a Charibdis: riziká tromboembolizmu a krvácania Ako bezpečne kormidlovať liečbu NOAK u fragilných pacientov s nevalvulárnou fibriláciou predsiení a žilovou tromboembolickou chorobou? doc. MUDr.
Scylla a Charibdis: riziká tromboembolizmu a krvácania Ako bezpečne kormidlovať liečbu NOAK u fragilných pacientov s nevalvulárnou fibriláciou predsiení a žilovou tromboembolickou chorobou? doc. MUDr.
Dávkovanie. Profylaxia a liečba. * HŽT - hĺbková žilová trombóza PE - pľúcna embólia
 Dávkovanie Profylaxia a liečba HŽT a PE* * HŽT - hĺbková žilová trombóza PE - pľúcna embólia Profylaxia HŽT a PE 1 všeobecná chirurgia ortopédia náhrada bedrového kĺbu Profylaxia s.c. Vysoké riziko* večer
Dávkovanie Profylaxia a liečba HŽT a PE* * HŽT - hĺbková žilová trombóza PE - pľúcna embólia Profylaxia HŽT a PE 1 všeobecná chirurgia ortopédia náhrada bedrového kĺbu Profylaxia s.c. Vysoké riziko* večer
Nové znenie informácií o lieku výňatky z odporúčaní výboru PRAC týkajúcich sa signálov
 25 January 2018 EMA/PRAC/35594/2018 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znenie informácií o lieku výňatky z odporúčaní výboru PRAC týkajúcich sa signálov Prijaté na zasadnutí
25 January 2018 EMA/PRAC/35594/2018 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znenie informácií o lieku výňatky z odporúčaní výboru PRAC týkajúcich sa signálov Prijaté na zasadnutí
Stručný peri-intervenčný manažment pacientov liečených
 Stručný peri-intervenčný manažment pacientov liečených NOAK Slovenský konsenzus odborných spoločností: Slovenská asociácia srdcových arytmií (SASA) Slovenská kardiologická spoločnosť (SKS) Slovenská spoločnosť
Stručný peri-intervenčný manažment pacientov liečených NOAK Slovenský konsenzus odborných spoločností: Slovenská asociácia srdcových arytmií (SASA) Slovenská kardiologická spoločnosť (SKS) Slovenská spoločnosť
dňa 01. apríla 2016 (piatok) o 9:00 v KONFERENČNÝCH PRIESTOROCH MZ SR, prof. MUDr. IVICA LAZÚROVÁ, DrSc., FRCP doc. MUDr. SOŇA KIŇOVÁ, PhD.
 SLOVENSKÁ LEKÁRSKA SPOLOČNOSŤ SLOVENSKÁ INTERNISTICKÁ SPOLOČNOSŤ 56. Dérerov Memoriál A Dérerov Deň dňa 01. apríla 2016 (piatok) o 9:00 v KONFERENČNÝCH PRIESTOROCH MZ SR, Limbová 2, Bratislava Kramáre
SLOVENSKÁ LEKÁRSKA SPOLOČNOSŤ SLOVENSKÁ INTERNISTICKÁ SPOLOČNOSŤ 56. Dérerov Memoriál A Dérerov Deň dňa 01. apríla 2016 (piatok) o 9:00 v KONFERENČNÝCH PRIESTOROCH MZ SR, Limbová 2, Bratislava Kramáre
Odporúčania odborných spoločností Zuzana Pribulová
 Odporúčania odborných spoločností Zuzana Pribulová Mnohé odborné spoločnosti sa zaoberajú prevenciou a liečbou VTE IUA (International Union of Angiology), 2007 ASCO (American Society of Clinical Oncology),
Odporúčania odborných spoločností Zuzana Pribulová Mnohé odborné spoločnosti sa zaoberajú prevenciou a liečbou VTE IUA (International Union of Angiology), 2007 ASCO (American Society of Clinical Oncology),
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Lipertance 10 mg/5 mg/5 mg Lipertance 20 mg/5 mg/5 mg Lipertance 20 mg/10 mg/5 mg Lipertance 20 mg/10 mg/10 mg Lipertance 40 mg/10 mg/10 mg filmom
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Lipertance 10 mg/5 mg/5 mg Lipertance 20 mg/5 mg/5 mg Lipertance 20 mg/10 mg/5 mg Lipertance 20 mg/10 mg/10 mg Lipertance 40 mg/10 mg/10 mg filmom
XIII. SLOVENSKÝ GERIATRICKÝ KONGRES
 Slovenská gerontologická a geriatrická spoločnosť Fakultná nemocnica Trenčín Fakulta zdravotníctva Trenčianskej univerzity Alexandra Dubčeka Spolok lekárov v Trenčíne usporiadajú pod záštitou predsedu
Slovenská gerontologická a geriatrická spoločnosť Fakultná nemocnica Trenčín Fakulta zdravotníctva Trenčianskej univerzity Alexandra Dubčeka Spolok lekárov v Trenčíne usporiadajú pod záštitou predsedu
Prečo pouţiť rivaroxaban v liečbe HŢT? MUDr. Ivan Čupka
 Prečo pouţiť rivaroxaban v liečbe HŢT? MUDr. Ivan Čupka HŢT Hlboká ţilová trombóza L.SK.MA.02.2016.1974 Potenciálny konflikt záujmov MUDr. Ivan Čupka Konzultant farmaceutických spoločností Člen Advisory
Prečo pouţiť rivaroxaban v liečbe HŢT? MUDr. Ivan Čupka HŢT Hlboká ţilová trombóza L.SK.MA.02.2016.1974 Potenciálny konflikt záujmov MUDr. Ivan Čupka Konzultant farmaceutických spoločností Člen Advisory
Antikoagulačná liečba u pacientov s fibriláciou predsiení
 rehľadové články 55 ntikoagulačná liečba u pacientov s fibriláciou predsiení Doc. MUDr. Ján Kmec, hd., MH Kardiocentrum FNs J.. Reimana a FZO U v rešove Fibrilácia predsiení (F) je častou arytmiou, ktorej
rehľadové články 55 ntikoagulačná liečba u pacientov s fibriláciou predsiení Doc. MUDr. Ján Kmec, hd., MH Kardiocentrum FNs J.. Reimana a FZO U v rešove Fibrilácia predsiení (F) je častou arytmiou, ktorej
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Clopidogrel MYLAN Pharma 75 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Clopidogrel MYLAN Pharma 75 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Votrient 200 mg filmom obalené tablety Votrient 400 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Votrient 200
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Votrient 200 mg filmom obalené tablety Votrient 400 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Votrient 200
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Schválený text k rozhodnutiu o registrácii, ev. č.: 2014/07280-REG, 2014/07281-REG SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Sertraline Accord 50 mg filmom obalené tablety Sertraline Accord
Schválený text k rozhodnutiu o registrácii, ev. č.: 2014/07280-REG, 2014/07281-REG SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Sertraline Accord 50 mg filmom obalené tablety Sertraline Accord
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU. Liek s ukončenou platnosťou registrácie
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Clopidogrel Teva Generics B.V. 75 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Clopidogrel Teva Generics B.V. 75 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Myclausen 500 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje 500 mg mofetilmykofenolátu.
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Myclausen 500 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje 500 mg mofetilmykofenolátu.
Peter Kubisz, Ján Staško, Daniela Kotuličová Národné centrum hemostázy a trombózy, Klinika hematológie a transfuziológie JLF UK a MFN, Martin
 NOVÉ MOŽNOSTI PREVENCIE A LIEČBY VENÓZNEHO TROMBOEMBOLIZMU PRI ARTROPLASTIKE KOLENA A BEDRA V ORTOPEDICKEJ CHIRURGII Peter Kubisz, Ján Staško, Daniela Kotuličová Národné centrum hemostázy a trombózy, Klinika
NOVÉ MOŽNOSTI PREVENCIE A LIEČBY VENÓZNEHO TROMBOEMBOLIZMU PRI ARTROPLASTIKE KOLENA A BEDRA V ORTOPEDICKEJ CHIRURGII Peter Kubisz, Ján Staško, Daniela Kotuličová Národné centrum hemostázy a trombózy, Klinika
Nízkomolekulové heparíny
 Nízkomolekulové heparíny Prof. MUDr. Jan Kvasnička, DrSc. Trombotické centrum, Ústav lékařské biochemie a laboratorní diagnostiky VFN, Praha Súhrn Kvasnička J. Nízkomolekulové heparíny. Farmakoterapia
Nízkomolekulové heparíny Prof. MUDr. Jan Kvasnička, DrSc. Trombotické centrum, Ústav lékařské biochemie a laboratorní diagnostiky VFN, Praha Súhrn Kvasnička J. Nízkomolekulové heparíny. Farmakoterapia
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Bondronat 2 mg infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka s obsahom 2 ml infúzneho koncentrátu obsahuje
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Bondronat 2 mg infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka s obsahom 2 ml infúzneho koncentrátu obsahuje
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU. TRIPLIXAM 5 mg/1,25 mg/10 mg: jedna filmom obalená tableta obsahuje 3,395 mg perindoprilu, čo
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU TRIPLIXAM 5 mg/1,25 mg/5 mg TRIPLIXAM 5 mg/1,25 mg/10 mg TRIPLIXAM 10 mg/2,5 mg/5 mg TRIPLIXAM 10 mg/2,5 mg/10 mg filmom obalené tablety 2. KVALITATÍVNE
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU TRIPLIXAM 5 mg/1,25 mg/5 mg TRIPLIXAM 5 mg/1,25 mg/10 mg TRIPLIXAM 10 mg/2,5 mg/5 mg TRIPLIXAM 10 mg/2,5 mg/10 mg filmom obalené tablety 2. KVALITATÍVNE
Antikoagulačná liečba venózneho tromboembolizmu v špecifických situáciách
 Antikoagulačná liečba venózneho tromboembolizmu v špecifických situáciách Juraj Maďarič Klinika kardiológie a angiológie NÚSCH, a LF SZU Bratislava Agenda Onkologickí pacienti Renálna insuficiencia Gravidita
Antikoagulačná liečba venózneho tromboembolizmu v špecifických situáciách Juraj Maďarič Klinika kardiológie a angiológie NÚSCH, a LF SZU Bratislava Agenda Onkologickí pacienti Renálna insuficiencia Gravidita
Funkčná urológia program. - Multidisciplinárne sympózium. november. Hotel Chopok, Jasná
 Funkčná urológia - Multidisciplinárne sympózium Hotel Chopok, Jasná 10.-11. november 2017 program príhovor Vážené kolegyne a kolegovia. Prvý ročník konferencie Funkčná urológia multidiscliplinárne sympózium
Funkčná urológia - Multidisciplinárne sympózium Hotel Chopok, Jasná 10.-11. november 2017 program príhovor Vážené kolegyne a kolegovia. Prvý ročník konferencie Funkčná urológia multidiscliplinárne sympózium
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Zavesca 100 mg kapsuly 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá kapsula obsahuje 100 mg miglustatu. Úplný zoznam pomocných látok,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Zavesca 100 mg kapsuly 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá kapsula obsahuje 100 mg miglustatu. Úplný zoznam pomocných látok,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU. Liek s ukončenou platnosťou registrácie
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Angiox 250 mg prášok na prípravu koncentrátu pre injekčný alebo infúzny roztok. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Angiox 250 mg prášok na prípravu koncentrátu pre injekčný alebo infúzny roztok. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná
Diagnostika a liečba relabovaného a refraktérneho DLBCL
 Diagnostika a liečba relabovaného a refraktérneho DLBCL Miriam Ladická Národný onkologický ústav Vysoká účinnosť Akceptovateľná Liečba ochorenia toxicita Minimálne neskoré NÚ cca 1/3 pacientov s DLBCL
Diagnostika a liečba relabovaného a refraktérneho DLBCL Miriam Ladická Národný onkologický ústav Vysoká účinnosť Akceptovateľná Liečba ochorenia toxicita Minimálne neskoré NÚ cca 1/3 pacientov s DLBCL
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Cholib 145 mg/20 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna filmom obalená tableta obsahuje 145 mg fenofibrátu
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Cholib 145 mg/20 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna filmom obalená tableta obsahuje 145 mg fenofibrátu
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Levemir 100 jednotiek/ml injekčný roztok v náplni. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE 1 ml roztoku obsahuje 100 jednotiek inzulínu
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Levemir 100 jednotiek/ml injekčný roztok v náplni. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE 1 ml roztoku obsahuje 100 jednotiek inzulínu
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
LIEKOVÉ RIZIKO. ČÍSLO 44 Október Používanie vysokých dávok ibuprofénu a kardiovaskulárne riziko
 LIEKOVÉ RIZIKO ČÍSLO 44 Október 2015 VYDÁVA: Štátny ústav pre kontrolu liečiv Bratislava ako neperiodickú publikáciu. Reg. č. 1884/98. KONTAKTNÁ ADRESA: Štátny ústav pre kontrolu liečiv, MUDr. P. Gibala
LIEKOVÉ RIZIKO ČÍSLO 44 Október 2015 VYDÁVA: Štátny ústav pre kontrolu liečiv Bratislava ako neperiodickú publikáciu. Reg. č. 1884/98. KONTAKTNÁ ADRESA: Štátny ústav pre kontrolu liečiv, MUDr. P. Gibala
Vplyv rizikových faktorov trombózy na výskyt trombotických komplikácií u pacientov s esenciálnou trombocytémiou
 116 Pôvodné články & kazuistiky Vplyv rizikových faktorov trombózy na výskyt trombotických komplikácií u pacientov s esenciálnou trombocytémiou Prof. MUDr. Mikuláš Hrubiško, CSc. 1, 2, prof. MUDr. Elena
116 Pôvodné články & kazuistiky Vplyv rizikových faktorov trombózy na výskyt trombotických komplikácií u pacientov s esenciálnou trombocytémiou Prof. MUDr. Mikuláš Hrubiško, CSc. 1, 2, prof. MUDr. Elena
{edocs}pdf/2011_farmaceuticky-obzor-03-pazopanib.pdf,800,1280{/edocs}
 Článok Pazopanib v PDF (načítanie môže chvíľu trvať). Trvanie testu do 6. júna 2011 {edocs}pdf/2011_farmaceuticky-obzor-03-pazopanib.pdf,800,1280{/edocs} - Juraj SÝKORA - Pazopanib nový inhibítor tyrozínkinázy
Článok Pazopanib v PDF (načítanie môže chvíľu trvať). Trvanie testu do 6. júna 2011 {edocs}pdf/2011_farmaceuticky-obzor-03-pazopanib.pdf,800,1280{/edocs} - Juraj SÝKORA - Pazopanib nový inhibítor tyrozínkinázy
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Tolucombi 40 mg/12,5 mg tablety Tolucombi 80 mg/12,5 mg tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Tolucombi 40 mg/12,5 mg tablety
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Tolucombi 40 mg/12,5 mg tablety Tolucombi 80 mg/12,5 mg tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Tolucombi 40 mg/12,5 mg tablety
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Schválený text k rozhodnutiu o zmene, ev.č.: 2011/03098, 2012/06792 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Depakine Chrono 500 mg 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŢENIE 333 mg valproátu
Schválený text k rozhodnutiu o zmene, ev.č.: 2011/03098, 2012/06792 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Depakine Chrono 500 mg 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŢENIE 333 mg valproátu
Slovenská spoločnosť pre hemostázu a trombózu
 Slovenská spoločnosť pre hemostázu a trombózu Slovak Society of Hemostasis and Thrombosis ODPORÚČANIA PRE PREVENCIU A LIEČBU VENÓZNEHO TROMBOEMBOLIZMU U PACIENTOV S MALIGNITOU 2011 Chudej J., Ornst P.,
Slovenská spoločnosť pre hemostázu a trombózu Slovak Society of Hemostasis and Thrombosis ODPORÚČANIA PRE PREVENCIU A LIEČBU VENÓZNEHO TROMBOEMBOLIZMU U PACIENTOV S MALIGNITOU 2011 Chudej J., Ornst P.,
Appendix IV - Prescribing Guidance for Apixaban
 Appendix IV - Prescribing Guidance for Apixaban Patient Factors Dose of Apixaban If your patient has any of the following MAJOR risk factors: Hypersensitivity to the active substance or to any of the excipients
Appendix IV - Prescribing Guidance for Apixaban Patient Factors Dose of Apixaban If your patient has any of the following MAJOR risk factors: Hypersensitivity to the active substance or to any of the excipients
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Bonviva 150 mg, filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje 150 mg kyseliny
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Bonviva 150 mg, filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá filmom obalená tableta obsahuje 150 mg kyseliny
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Prestilol 5 mg/10 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna filmom obalená tableta obsahuje 5 mg bisoprololiumfumarátu
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Prestilol 5 mg/10 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna filmom obalená tableta obsahuje 5 mg bisoprololiumfumarátu
Hotel Yasmin. Tyršovo nábrežie 1 Košice apríla 2017 XIII. PROGRAM OSTEO FÓRUM
 Hotel Yasmin Tyršovo nábrežie 1 Košice 21. - 22. apríla 2017 PROGRAM XIII. OSTEO FÓRUM XIII. OSTEO FÓRUM 21.- 22. apríla 2017 Hotel Yasmin Tyršovo nábrežie 1 Košice Usporiadateľ Slovenská lekárska spoločnosť
Hotel Yasmin Tyršovo nábrežie 1 Košice 21. - 22. apríla 2017 PROGRAM XIII. OSTEO FÓRUM XIII. OSTEO FÓRUM 21.- 22. apríla 2017 Hotel Yasmin Tyršovo nábrežie 1 Košice Usporiadateľ Slovenská lekárska spoločnosť
Kde uskutočniť testy na prítomnosť trombofilného stavu:
 54 Hlavná téma Trombofilné stavy MUDr. Lucia Stančiaková, PhD., MUDr. Miroslava Dobrotová, PhD., MUDr. Pavol Hollý, PhD., RNDr. Jela Ivanková, MUDr. Ivana Plameňová, PhD., prof. MUDr. Ján Staško, PhD.,
54 Hlavná téma Trombofilné stavy MUDr. Lucia Stančiaková, PhD., MUDr. Miroslava Dobrotová, PhD., MUDr. Pavol Hollý, PhD., RNDr. Jela Ivanková, MUDr. Ivana Plameňová, PhD., prof. MUDr. Ján Staško, PhD.,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU LEMTRADA 12 mg infúzny koncentrát. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 12 mg alemtuzumabu v 1,2
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU LEMTRADA 12 mg infúzny koncentrát. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 12 mg alemtuzumabu v 1,2
Comparison of novel oral anticoagulants (NOACs)
 Comparison of novel oral anticoagulants (NOACs) For guidance for full information refer to individual SPCs available at www.medicines.org.uk Licensed indications for NOACs Prevention of stroke and systemic
Comparison of novel oral anticoagulants (NOACs) For guidance for full information refer to individual SPCs available at www.medicines.org.uk Licensed indications for NOACs Prevention of stroke and systemic
Prescriber Guide Date of preparation: January 2018
 Prescriber Guide Date of preparation: January 2018 Table of Contents Patient Information Booklet 2 Patient Alert Card 2 Assessing stroke risk CHA 2DS 2-VASc 3 Assessing bleeding risk HAS-BLED 3 Therapeutic
Prescriber Guide Date of preparation: January 2018 Table of Contents Patient Information Booklet 2 Patient Alert Card 2 Assessing stroke risk CHA 2DS 2-VASc 3 Assessing bleeding risk HAS-BLED 3 Therapeutic
Profil tromboembolického
 Originálny článok * Original article Cardiology Lett. 2012;21(2):98 110 Profil tromboembolického rizika u pacientov s fibriláciou predsiení v ambulantnej praxi internistov a kardiológov na Slovensku: údaje
Originálny článok * Original article Cardiology Lett. 2012;21(2):98 110 Profil tromboembolického rizika u pacientov s fibriláciou predsiení v ambulantnej praxi internistov a kardiológov na Slovensku: údaje
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS
 ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
Hlavný vzdelávací materiál pre krajiny EÚ Atomoxetine Actavis 10 mg, 18 mg, 25 mg, 40 mg, 60 mg tvrdé kapsuly
 Hlavný vzdelávací materiál pre krajiny EÚ Atomoxetine Actavis 10 mg, 18 mg, 25 mg, 40 mg, 60 mg tvrdé kapsuly Obsah 1. Úvodný list 2. Príloha 1 Súhrn charakteristických vlastností lieku 3. Príloha 2 Príručka
Hlavný vzdelávací materiál pre krajiny EÚ Atomoxetine Actavis 10 mg, 18 mg, 25 mg, 40 mg, 60 mg tvrdé kapsuly Obsah 1. Úvodný list 2. Príloha 1 Súhrn charakteristických vlastností lieku 3. Príloha 2 Príručka
Clinical issues which drug for which patient
 Anticoagulants - a matter of heart! Towards a bright future? Clinical issues which drug for which patient Sabine Eichinger Dept. of Medicine I Medical University of Vienna/Austria Conflicts of interest
Anticoagulants - a matter of heart! Towards a bright future? Clinical issues which drug for which patient Sabine Eichinger Dept. of Medicine I Medical University of Vienna/Austria Conflicts of interest
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS
 ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
MUDr. Silvia Babothyová II. Interná klinika SZU FNsP FDR Banská Bystrica
 MUDr. Silvia Babothyová II. Interná klinika SZU FNsP FDR Banská Bystrica 28.3. 3018 Pre každého pacienta v každom medicínskom odbore: Skórovacie systémy Caprini chirurgické odbory Padua internistické odbory
MUDr. Silvia Babothyová II. Interná klinika SZU FNsP FDR Banská Bystrica 28.3. 3018 Pre každého pacienta v každom medicínskom odbore: Skórovacie systémy Caprini chirurgické odbory Padua internistické odbory
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Ibandronic Acid Accord 2 mg infúzny koncentrát Ibandronic Acid Accord 6 mg infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Ibandronic Acid Accord 2 mg infúzny koncentrát Ibandronic Acid Accord 6 mg infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Krvácanie v kardiochirurgii a manažment pooperačného krvácania
 45 Krvácanie v kardiochirurgii a manažment pooperačného krvácania MUDr. Jozefína Cocherová 1, doc. MUDr. Pavol Török, CSc. 1, MUDr. František Sabol, PhD. 2 1 Klinika anestéziológie a intenzívnej medicíny,
45 Krvácanie v kardiochirurgii a manažment pooperačného krvácania MUDr. Jozefína Cocherová 1, doc. MUDr. Pavol Török, CSc. 1, MUDr. František Sabol, PhD. 2 1 Klinika anestéziológie a intenzívnej medicíny,
Anestézia a ischemická choroba srdca
 Richard Koyš Úvod Anestéziológ sa s pacientami s ischemickou chorobou srdca stretáva každodenne. Rozsah ochorenia srdca, vek, pridružené ochorenia a operačný výkon, ktorý majú podstúpiť, môžu výrazne varírovať
Richard Koyš Úvod Anestéziológ sa s pacientami s ischemickou chorobou srdca stretáva každodenne. Rozsah ochorenia srdca, vek, pridružené ochorenia a operačný výkon, ktorý majú podstúpiť, môžu výrazne varírovať
PROGRAM apríla XXXIII. Kongres Slovenskej hypertenziologickej spoločnosti. Hotel Holiday Inn Žilina.
 počet kreditov SLK 16 Slovenská hypertenziologická spoločnosť Slovenská kardiologická spoločnosť XXXIII. Kongres Slovenskej hypertenziologickej spoločnosti a KONFERENCIA PRACOVNEJ SKUPINY PREVENTÍVNEJ
počet kreditov SLK 16 Slovenská hypertenziologická spoločnosť Slovenská kardiologická spoločnosť XXXIII. Kongres Slovenskej hypertenziologickej spoločnosti a KONFERENCIA PRACOVNEJ SKUPINY PREVENTÍVNEJ
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Vidaza 25 mg/ml prášok na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 100 mg azacitidínu.
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Vidaza 25 mg/ml prášok na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 100 mg azacitidínu.
Nové perspektívy boja proti diabetu 2. typu inhibítory sodíkovo glukózového transportéra 2
 Nové perspektívy boja proti diabetu 2. typu inhibítory sodíkovo glukózového transportéra 2 D. Skripová Súhrn Inhibítory sodíkovo glukózového transportéra 2 (SGLT2) sú novou skupinou antidiabetík, ktorých
Nové perspektívy boja proti diabetu 2. typu inhibítory sodíkovo glukózového transportéra 2 D. Skripová Súhrn Inhibítory sodíkovo glukózového transportéra 2 (SGLT2) sú novou skupinou antidiabetík, ktorých
PREHĽADOVÝ ČLÁNOK. Boris Šteňo 1, Emőke Šteňová 2, Róbert Brnka 2 1. II. ortopedicko-traumatologická klinika LFUK a FNsP, Bratislava 2
 PREHĽADOVÝ ČLÁNOK OSTEOARTRÓZA KOMPLEXNÁ KONZERVATÍVNA LIEČBA Boris Šteňo 1, Emőke Šteňová 2, Róbert Brnka 2 1 II. ortopedicko-traumatologická klinika LFUK a FNsP, Bratislava 2 I. interná klinika LFUK
PREHĽADOVÝ ČLÁNOK OSTEOARTRÓZA KOMPLEXNÁ KONZERVATÍVNA LIEČBA Boris Šteňo 1, Emőke Šteňová 2, Róbert Brnka 2 1 II. ortopedicko-traumatologická klinika LFUK a FNsP, Bratislava 2 I. interná klinika LFUK
Žiadosť o podmienené zaradenie lieku do zoznamu kategorizovaných liekov a úradné určenie ceny lieku. Typ žiadosti A1P
 Žiadosť o podmienené zaradenie lieku do zoznamu kategorizovaných liekov a úradné určenie ceny lieku Typ žiadosti A1P Časť A Údaje o žiadateľovi 1. Držiteľ registrácie: Meno a priezvisko alebo obchodné
Žiadosť o podmienené zaradenie lieku do zoznamu kategorizovaných liekov a úradné určenie ceny lieku Typ žiadosti A1P Časť A Údaje o žiadateľovi 1. Držiteľ registrácie: Meno a priezvisko alebo obchodné
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS
 ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAME OF THE MEDICINAL PRODUCT Eliquis 2.5 mg film-coated tablets 2. QUALITATIVE AND QUANTITATIVE COMPOSITION Each film-coated tablet contains 2.5 mg apixaban.
Onkologický pacient a riziko vzniku venózneho tromboembolizmu (VTE) MUDr. Viliam Bugáň
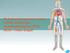 Onkologický pacient a riziko vzniku venózneho tromboembolizmu (VTE) MUDr. Viliam Bugáň V EU v nasledujúcich 30 minútach: 3 4 5 31 V dôsledku VTE zomrie v EU viac ako 2-násobok súčtu obetí: dopravných nehôd,
Onkologický pacient a riziko vzniku venózneho tromboembolizmu (VTE) MUDr. Viliam Bugáň V EU v nasledujúcich 30 minútach: 3 4 5 31 V dôsledku VTE zomrie v EU viac ako 2-násobok súčtu obetí: dopravných nehôd,
Získaná hemofília A. Hlavná téma. Doc. MUDr. Mária Hulíková, PhD. Centrum hemostázy a trombózy, HEMO MEDIKA, s. r. o., Košice. Acquired hemophilia A
 107 Získaná hemofília A Doc. MUDr. Mária Hulíková, PhD. Centrum hemostázy a trombózy, HEMO MEDIKA, s. r. o., Košice Získaná hemofília A (ZHA) je vzácne autoimunitné ochorenie spôsobené produkciou autoprotilátok,
107 Získaná hemofília A Doc. MUDr. Mária Hulíková, PhD. Centrum hemostázy a trombózy, HEMO MEDIKA, s. r. o., Košice Získaná hemofília A (ZHA) je vzácne autoimunitné ochorenie spôsobené produkciou autoprotilátok,
Drug Use Criteria: Direct Oral Anticoagulants
 Texas Vendor Drug Program Drug Use Criteria: Oral Anticoagulants Publication History 1. Developed March 2017. 2. Revised February 2018. Notes: Information on indications for use or diagnosis is assumed
Texas Vendor Drug Program Drug Use Criteria: Oral Anticoagulants Publication History 1. Developed March 2017. 2. Revised February 2018. Notes: Information on indications for use or diagnosis is assumed
Ivan Gogolák Neurologická klinika SZU, FN Ružinov, Bratislava
 PREVENCIA CIEVNYCH MOZGOVÝCH PRÍHOD Ivan Gogolák Neurologická klinika SZU, FN Ružinov, Bratislava Via pract., 2008, roč. 5 (S4): 6 11 Úvod Najdôležitejším prostriedkom na zníženie závažných následkov a
PREVENCIA CIEVNYCH MOZGOVÝCH PRÍHOD Ivan Gogolák Neurologická klinika SZU, FN Ružinov, Bratislava Via pract., 2008, roč. 5 (S4): 6 11 Úvod Najdôležitejším prostriedkom na zníženie závažných následkov a
Southern Trust Anticoagulant Team
 CLINICAL GUIDELINES ID TAG Title: Author: Speciality / Division: Directorate: Anticoagulation- Primary Care Guidance for reviewing patients on DOACs Southern Trust Anticoagulant Team Haematology Acute
CLINICAL GUIDELINES ID TAG Title: Author: Speciality / Division: Directorate: Anticoagulation- Primary Care Guidance for reviewing patients on DOACs Southern Trust Anticoagulant Team Haematology Acute
Edoxaban For preventing stroke and systemic embolism in people with non-valvular atrial fibrillation (NICE TA 355)
 Rationale for Initiation, Continuation and Discontinuation (RICaD) Edoxaban For preventing stroke and systemic embolism in people with non-valvular atrial fibrillation (NICE TA 355) This document supports
Rationale for Initiation, Continuation and Discontinuation (RICaD) Edoxaban For preventing stroke and systemic embolism in people with non-valvular atrial fibrillation (NICE TA 355) This document supports
Prehľad. III. Riadená hypotermia (RH) I. Hypoxia ischémia (HI) II. Patofyziológia HI
 Prehľad I. Hypoxia ischémia (HI) II. Patofyziológia HI III. Riadená hypotermia (RH) 1. účinky a metódy 2. metaanalýzy 3. podmienky a prístroje 4. indikácie 5. aeeg 6. kontraindikácie a prerušenie 7. PRINCÍPY
Prehľad I. Hypoxia ischémia (HI) II. Patofyziológia HI III. Riadená hypotermia (RH) 1. účinky a metódy 2. metaanalýzy 3. podmienky a prístroje 4. indikácie 5. aeeg 6. kontraindikácie a prerušenie 7. PRINCÍPY
PROGRAMME Venue: Crowne Plaza Hotel
 PROGRAMME Venue: Crowne Plaza Hotel Obesitology Section of the Slovakian Diabetes Society Slovakian Diabetes Society in association with Biomedical Research Center Slovak Academy of Sciences organize 6
PROGRAMME Venue: Crowne Plaza Hotel Obesitology Section of the Slovakian Diabetes Society Slovakian Diabetes Society in association with Biomedical Research Center Slovak Academy of Sciences organize 6
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Vidaza 25 mg/ml prášok na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 100 mg azacitidínu.
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Vidaza 25 mg/ml prášok na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá injekčná liekovka obsahuje 100 mg azacitidínu.
Príloha III. Zmeny príslušných častí informácie o lieku
 Príloha III Zmeny príslušných častí informácie o lieku Poznámka: Tieto zmeny príslušných častí Súhrnu charakteristických vlastností lieku a Písomnej informácie pre používateľa sú výsledkom Referral procedúry.
Príloha III Zmeny príslušných častí informácie o lieku Poznámka: Tieto zmeny príslušných častí Súhrnu charakteristických vlastností lieku a Písomnej informácie pre používateľa sú výsledkom Referral procedúry.
PRODUCT INFORMATION. ELIQUIS apixaban NAME OF THE MEDICINE DESCRIPTION PHARMACOLOGY
 PRODUCT INFORMATION ELIQUIS apixaban NAME OF THE MEDICINE, a selective inhibitor of the coagulation Factor Xa (FXa), is chemically described as 1-(4-Methoxyphenyl)-7-oxo-6-[4-(2-oxopiperidin-1-yl)phenyl]-4,5,6,7-tetrahydro-1Hpyrazolo[3,4-c]pyridine-3-carboxamide.
PRODUCT INFORMATION ELIQUIS apixaban NAME OF THE MEDICINE, a selective inhibitor of the coagulation Factor Xa (FXa), is chemically described as 1-(4-Methoxyphenyl)-7-oxo-6-[4-(2-oxopiperidin-1-yl)phenyl]-4,5,6,7-tetrahydro-1Hpyrazolo[3,4-c]pyridine-3-carboxamide.
Písomná informácia pre používateľa. BCG-medac, prášok a disperzné prostredie na intravezikálnu suspenziu (Bacillus Calmette-Guérin)
 Písomná informácia pre používateľa BCG-medac, prášok a disperzné prostredie na intravezikálnu suspenziu (Bacillus Calmette-Guérin) Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Písomná informácia pre používateľa BCG-medac, prášok a disperzné prostredie na intravezikálnu suspenziu (Bacillus Calmette-Guérin) Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Medical Policy An independent licensee of the Blue Cross Blue Shield Association
 Oral Anticoagulants Page 1 of 7 Medical Policy An independent licensee of the Blue Cross Blue Shield Association Title: Oral Anticoagulant - Bevyxxa (betrixaban), Eliquis (apixaban), Pradaxa (dabigatran),
Oral Anticoagulants Page 1 of 7 Medical Policy An independent licensee of the Blue Cross Blue Shield Association Title: Oral Anticoagulant - Bevyxxa (betrixaban), Eliquis (apixaban), Pradaxa (dabigatran),
È possibile cambiare posologia o farmaco sulla base dei test di laboratorio?
 È possibile cambiare posologia o farmaco sulla base dei test di laboratorio? Armando D Angelo Servizio di Coagulazione ed Unità Ricerca Trombosi, IRCCS Ospedale San Raffaele, Milano XXVI CONGRESSO NAZIONALE
È possibile cambiare posologia o farmaco sulla base dei test di laboratorio? Armando D Angelo Servizio di Coagulazione ed Unità Ricerca Trombosi, IRCCS Ospedale San Raffaele, Milano XXVI CONGRESSO NAZIONALE
Nové hormonálne preparáty v liečbe karcinómu prostaty. Ján Kliment Urologická klinika JLFUK a UNM Martin
 Nové hormonálne preparáty v liečbe karcinómu prostaty Ján Kliment Urologická klinika JLFUK a UNM Martin Kastračne rezistentný karcinóm prostaty Za progresiu onemocnenia je zodpovedná reaktivácia androgennej
Nové hormonálne preparáty v liečbe karcinómu prostaty Ján Kliment Urologická klinika JLFUK a UNM Martin Kastračne rezistentný karcinóm prostaty Za progresiu onemocnenia je zodpovedná reaktivácia androgennej
BMS Project ID: 432US /16
 The Bristol-Myers Squibb/Pfizer Medical Alliance would like to inform you that the following sections of the prescribing information for ELIQUIS (apixaban) have been updated and the underlined text denotes
The Bristol-Myers Squibb/Pfizer Medical Alliance would like to inform you that the following sections of the prescribing information for ELIQUIS (apixaban) have been updated and the underlined text denotes
3/19/2012. What is the indication for anticoagulation? Has the patient previously been on warfarin? If so, what % of the time was the INR therapeutic?
 Abigail E. Miller, PharmD, BCPS Clinical Specialist, Cardiology University of North Carolina Hospitals I have no personal financial relationships with the manufacturers of the products to disclose. Boehringer
Abigail E. Miller, PharmD, BCPS Clinical Specialist, Cardiology University of North Carolina Hospitals I have no personal financial relationships with the manufacturers of the products to disclose. Boehringer
Apixaban for Atrial Fibrillation in Patients with End-Stage Renal Disease on Dialysis
 Apixaban for Atrial Fibrillation in Patients with End-Stage Renal Disease on Dialysis Caitlin Reedholm, PharmD PGY1 Pharmacy Resident St. David s South Austin Medical Center November 2, 2018 Abbreviations
Apixaban for Atrial Fibrillation in Patients with End-Stage Renal Disease on Dialysis Caitlin Reedholm, PharmD PGY1 Pharmacy Resident St. David s South Austin Medical Center November 2, 2018 Abbreviations
Reziduálne kardiovaskulárne riziko závažný problém, ktorý si bude vyžadova nové liečebné prístupy
 PREHĽADNÉ ČLÁNKY * REVIEW ARTICLES Reziduálne kardiovaskulárne riziko závažný problém, ktorý si bude vyžadova nové liečebné prístupy ANDREJ DUKÁT Bratislava, Slovenská republika DUKÁT A. Reziduálne kardiovaskulárne
PREHĽADNÉ ČLÁNKY * REVIEW ARTICLES Reziduálne kardiovaskulárne riziko závažný problém, ktorý si bude vyžadova nové liečebné prístupy ANDREJ DUKÁT Bratislava, Slovenská republika DUKÁT A. Reziduálne kardiovaskulárne
Xarelto (rivaroxaban) Prescriber Guide
 Xarelto (rivaroxaban) Prescriber Guide October 2018 PP-XAR-IE-0031 Contents Patient Alert Card 4 Dosing Recommendations 4 Stroke prevention in adult patients with non-valvular atrial fibrillation 4 Patients
Xarelto (rivaroxaban) Prescriber Guide October 2018 PP-XAR-IE-0031 Contents Patient Alert Card 4 Dosing Recommendations 4 Stroke prevention in adult patients with non-valvular atrial fibrillation 4 Patients
What s new with DOACs? Defining place in therapy for edoxaban &
 What s new with DOACs? Defining place in therapy for edoxaban & Use of DOACs in cardioversion Caitlin M. Gibson, PharmD, BCPS Assistant Professor, Department of Pharmacotherapy University of North Texas
What s new with DOACs? Defining place in therapy for edoxaban & Use of DOACs in cardioversion Caitlin M. Gibson, PharmD, BCPS Assistant Professor, Department of Pharmacotherapy University of North Texas
Predanestetické vyšetrenie kardiaka pre nekardiálnu operáciu Štefan Trenkler
 Predanestetické vyšetrenie kardiaka pre nekardiálnu operáciu Štefan Trenkler I. klinika AIM UPJŠ LF Košice CEEA Košice 2016 Program 1. Úvod 2. MICA incidencia, mechanizmus 3. Odporúčania pre nekardiálnu
Predanestetické vyšetrenie kardiaka pre nekardiálnu operáciu Štefan Trenkler I. klinika AIM UPJŠ LF Košice CEEA Košice 2016 Program 1. Úvod 2. MICA incidencia, mechanizmus 3. Odporúčania pre nekardiálnu
Miroslav Brozman Neurologická klinika FN, Nitra
 ÚVOD DO PROBLEMATIKY CIEVNYCH MOZGOVÝCH OCHORENÍ Miroslav Brozman Neurologická klinika FN, Nitra Cerebrovaskulárne ochorenia (CVO) predstavujú dlhodobo jeden z najzávažnejších zdravotníckych problémov
ÚVOD DO PROBLEMATIKY CIEVNYCH MOZGOVÝCH OCHORENÍ Miroslav Brozman Neurologická klinika FN, Nitra Cerebrovaskulárne ochorenia (CVO) predstavujú dlhodobo jeden z najzávažnejších zdravotníckych problémov
New Anticoagulants Therapies
 New Anticoagulants Therapies Rachel P. Rosovsky, MD, MPH October 22, 2015 Conflicts of Interest No disclosures 2 Agenda 3 Historical perspective Novel oral anticoagulants Stats Trials Approval Concerns/Limitations
New Anticoagulants Therapies Rachel P. Rosovsky, MD, MPH October 22, 2015 Conflicts of Interest No disclosures 2 Agenda 3 Historical perspective Novel oral anticoagulants Stats Trials Approval Concerns/Limitations
The clinical relevance of AMPLIFY programme
 Venice October 16th 2015 The clinical relevance of AMPLIFY programme Francesco Dentali Department of Clinical Medicine Insubria University Varese Disclosures Bayer Bristol-Myers Squibb/Pfizer Boehringer
Venice October 16th 2015 The clinical relevance of AMPLIFY programme Francesco Dentali Department of Clinical Medicine Insubria University Varese Disclosures Bayer Bristol-Myers Squibb/Pfizer Boehringer
Edoxaban Treatment and secondary prevention of deep vein thrombosis and/or pulmonary embolism (NICE TA354)
 Rationale for Initiation, Continuation and Discontinuation (RICaD) Edoxaban Treatment and secondary prevention of deep vein thrombosis and/or pulmonary embolism (NICE TA354) This document supports the
Rationale for Initiation, Continuation and Discontinuation (RICaD) Edoxaban Treatment and secondary prevention of deep vein thrombosis and/or pulmonary embolism (NICE TA354) This document supports the
Tromboembolická choroba
 Vladimír Kollárik Chorobný proces, označovaný ako tromboembolická choroba (TECH), predstavuje komplexnú nozologickú jednotku. Vzniká ako následok prítomnosti trombu vo venóznom riečisku a/alebo embolizácie
Vladimír Kollárik Chorobný proces, označovaný ako tromboembolická choroba (TECH), predstavuje komplexnú nozologickú jednotku. Vzniká ako následok prítomnosti trombu vo venóznom riečisku a/alebo embolizácie
Direct Oral Anticoagulants (DOACs). Dr GM Benson Director NI Haemophilia Comprehensive Care Centre and Thrombosis Unit BHSCT
 Direct Oral Anticoagulants (DOACs). Dr GM Benson Director NI Haemophilia Comprehensive Care Centre and Thrombosis Unit BHSCT OAC WARFARIN Gold standard DABIGATRAN RIVAROXABAN APIXABAN EDOXABAN BETRIXABAN
Direct Oral Anticoagulants (DOACs). Dr GM Benson Director NI Haemophilia Comprehensive Care Centre and Thrombosis Unit BHSCT OAC WARFARIN Gold standard DABIGATRAN RIVAROXABAN APIXABAN EDOXABAN BETRIXABAN
XXXIII. Červeňanského dni
 1 2 L.SK.12.2012.0589 3 4 Vážené kolegyne, kolegovia, milí priatelia, v mene výboru Slovenskej ortopedickej a traumatologickej spoločnosti si Vás dovoľujem pozvať na národný kongres SOTS, ktorý sa bude
1 2 L.SK.12.2012.0589 3 4 Vážené kolegyne, kolegovia, milí priatelia, v mene výboru Slovenskej ortopedickej a traumatologickej spoločnosti si Vás dovoľujem pozvať na národný kongres SOTS, ktorý sa bude
Množstvo aktívnej látky. GLUSCAN MBq/mL v čase kalibrácie. GLUSCAN MBq/mL v čase kalibrácie. GLUSCAN PL 500 MBq/mL v čase kalibrácie
 PRÍLOHA I ZOZNAM NÁZVOV, FARMACEUTICKÝCH FORIEM, MNOŽSTVÁ ÚČINNÝCH LÁTOK V LIEKU, SPÔSOB PODÁVANIA, UCHÁDZAČ, DRŽITEĽ ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 Členský štát EU/EHP Držiteľ rozhodnutia
PRÍLOHA I ZOZNAM NÁZVOV, FARMACEUTICKÝCH FORIEM, MNOŽSTVÁ ÚČINNÝCH LÁTOK V LIEKU, SPÔSOB PODÁVANIA, UCHÁDZAČ, DRŽITEĽ ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 Členský štát EU/EHP Držiteľ rozhodnutia
Hodnotenie a obmedzovanie rizika kardiovaskulárneho ochorenia u žien
 Kontrolný zoznam pre efektívne hodnotenie rizika kardiovaskulárneho ochorenia ESC Task Force on Gender Úvodná konzultácia Rodinná anamnéza Počet cigariet za deň Konzumácia alkoholu Menopauzálny status
Kontrolný zoznam pre efektívne hodnotenie rizika kardiovaskulárneho ochorenia ESC Task Force on Gender Úvodná konzultácia Rodinná anamnéza Počet cigariet za deň Konzumácia alkoholu Menopauzálny status
Updates in Anticoagulation for Atrial Fibrillation and Venous Thromboembolism
 Disclosures Updates in Anticoagulation for Atrial Fibrillation and Venous Thromboembolism No financial conflicts of interest Member of the ABIM Focused- Practice in Hospital Medicine Self Examination Process
Disclosures Updates in Anticoagulation for Atrial Fibrillation and Venous Thromboembolism No financial conflicts of interest Member of the ABIM Focused- Practice in Hospital Medicine Self Examination Process
Akútne koronárne syndrómy
 Braunwald E et al. J Am Coll Cardiol 2000;36:970 1062. Akútne koronárne syndrómy Akútny koronárny syndróm Bez elevácie ST segm. Elevácia ST segm. IM bez elevácie ST Nestabilná AP Infarkt myokardu bez Q
Braunwald E et al. J Am Coll Cardiol 2000;36:970 1062. Akútne koronárne syndrómy Akútny koronárny syndróm Bez elevácie ST segm. Elevácia ST segm. IM bez elevácie ST Nestabilná AP Infarkt myokardu bez Q
ŠTANDARDNÝ DIAGNOSTICKÝ A TERAPEUTICKÝ POSTUP
 Ročník 13 Júl 2009 Číslo 3 4 ŠTANDARDNÝ DIAGNOSTICKÝ A TERAPEUTICKÝ POSTUP 47. Metodický list racionálnej farmakoterapie Racionálna farmakoterapia bolesti pri vertebrogénnych ochoreniach 1 Úvod Bolesť
Ročník 13 Júl 2009 Číslo 3 4 ŠTANDARDNÝ DIAGNOSTICKÝ A TERAPEUTICKÝ POSTUP 47. Metodický list racionálnej farmakoterapie Racionálna farmakoterapia bolesti pri vertebrogénnych ochoreniach 1 Úvod Bolesť
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS
 ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 This medicinal product is subject to additional monitoring. This will allow quick identification of new safety information. Healthcare professionals are asked
ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS 1 This medicinal product is subject to additional monitoring. This will allow quick identification of new safety information. Healthcare professionals are asked
Klinické skúsenosti s VELCADE v liečbe chorých s mnohopočetným myelómom v SR Elena Tóthová, Košice, KHaOH LF UPJS a FNLP
 Klinické skúsenosti s VELCADE v liečbe chorých s mnohopočetným myelómom v SR Elena Tóthová, Košice, KHaOH LF UPJS a FNLP Fáza I a II trialov u mnohopočetného myelómu Myelómové bunky sú závislé na transkripcii
Klinické skúsenosti s VELCADE v liečbe chorých s mnohopočetným myelómom v SR Elena Tóthová, Košice, KHaOH LF UPJS a FNLP Fáza I a II trialov u mnohopočetného myelómu Myelómové bunky sú závislé na transkripcii
New Antithrombotic Agents DISCLOSURE
 New Antithrombotic Agents DISCLOSURE Relevant Financial Relationship(s) Speaker Bureau None Research Alexion (PNH) delought@ohsu.edu Tom DeLoughery, MD FACP FAWM Oregon Health and Sciences University What
New Antithrombotic Agents DISCLOSURE Relevant Financial Relationship(s) Speaker Bureau None Research Alexion (PNH) delought@ohsu.edu Tom DeLoughery, MD FACP FAWM Oregon Health and Sciences University What
Akútne hematologické komplikácie u onkologických pacientov
 14 Akútne hematologické komplikácie u onkologických pacientov MUDr. Ľudmila Krištof Oddelenie klinickej hematológie a transfuziológie, Národný onkologický ústav, Bratislava Samotné onkologické ochorenie,
14 Akútne hematologické komplikácie u onkologických pacientov MUDr. Ľudmila Krištof Oddelenie klinickej hematológie a transfuziológie, Národný onkologický ústav, Bratislava Samotné onkologické ochorenie,
Králičí antitymocytový globulín (Thymoglobuline) použitie v hematológii
 profily liekov Králičí antitymocytový globulín (Thymoglobuline) použitie v hematológii MUDr. Eva Bojtárová, PhD. Klinika hematológie a transfuziológie, Univerzitná nemocnica Bratislava Súhrn Bojátrová
profily liekov Králičí antitymocytový globulín (Thymoglobuline) použitie v hematológii MUDr. Eva Bojtárová, PhD. Klinika hematológie a transfuziológie, Univerzitná nemocnica Bratislava Súhrn Bojátrová
MEDICAL ASSISTANCE HANDBOOK PRIOR AUTHORIZATION OF PHARMACEUTICAL SERVICES. A. Prescriptions That Require Prior Authorization
 MEDICAL ASSISTANCE HBOOK PRI AUTHIZATION OF PHARMACEUTICAL SERVICES I. Requirements for Prior Authorization of Anticoagulants A. Prescriptions That Require Prior Authorization Prescriptions for Anticoagulants
MEDICAL ASSISTANCE HBOOK PRI AUTHIZATION OF PHARMACEUTICAL SERVICES I. Requirements for Prior Authorization of Anticoagulants A. Prescriptions That Require Prior Authorization Prescriptions for Anticoagulants
Smernice Verzia november 2012
 Smernice Verzia 6.1 - november 2012 Európska klinická spoločnosť AIDS (EACS) je neziskové združenie európskych lekárov a výskumných pracovníkov v oblasti HIV/AIDS. Združenie spája vedeckých pracovníkov
Smernice Verzia 6.1 - november 2012 Európska klinická spoločnosť AIDS (EACS) je neziskové združenie európskych lekárov a výskumných pracovníkov v oblasti HIV/AIDS. Združenie spája vedeckých pracovníkov
